Kísérletek jóddal és termékekkel. A nyál amilázának hatása a keményítőre. Kémiai reakciók asztali sóval
Az anyag célja, hogy felkeltse a gyermekek érdeklődését a kognitív és kísérleti tevékenységek iránt. A kísérlet során a gyermek önállóan von le következtetéseket a keményítőről, annak szükségességéről és fontosságáról az emberi életben. Fejlődik az elemző képesség, a kognitív tevékenység, a megszerzett ismeretek rendszerezésének képessége.
Letöltés:
Előnézet:
A tanulmány célja:kíváncsiság fejlesztése - keményítő keresése az élelmiszerekben és tulajdonságainak tanulmányozása.
Feladatok: a keményítővel kapcsolatos ismeretek tisztázása és bővítése; megtanulják, hogyan kell keményítőt készíteni burgonyából; bemutatja tulajdonságait; fejleszteni kell a kísérleti munka iránti kognitív érdeklődést, érvelési készségeket; kitartó figyelem fejlesztése, kíváncsiság fejlesztése.
Keményítőkutatási terv:
1) keményítőt nyerni a burgonyagumóból;
2) kísérletesen, jódoldat segítségével ellenőrizze a keményítő jelenlétét vagy hiányát az élelmiszerekben;
3) mutasd meg gyakorlati módokon keményítő használata a mindennapi életben.
Anyagok: KEMÉNYÍTŐ, kanál, közönséges burgonya, reszelt burgonya, egy csésze víz, egy száraz csésze, jód pipettával, 2 egyforma pohár víz, egy tányér étel, egy tál víz, 2 szett baba ágynemű, egy pohár zselé.
Hello, a nevem Gleb. Nagyon szeretem a zselét – olyan finom és egészséges, és mindig is érdekelt, hogy miből készül a zselé. A recept szerint „adj hozzá keményítőt”. Mi a keményítő? Megpróbálom kideríteni.
Hogyan nyerik a keményítőt? Azt hallottam, hogy a keményítő sok növényben megtalálható, de leginkább a burgonyában.
A gyermek veszi a burgonyát, és elkezdi szemrevételezéssel megvizsgálni: ránéz, megforgatja a kezében.
Homályos. Próbálunk keményítőt nyerni belőle. Anya burgonyát reszelt nekem, én pedig beletettem a vízbe.
A kísérlet menete: a gyermek a burgonyát vízbe engedi, és többször rányomja. Ezután óvatosan átteszi a burgonyát egy másik tálba, és néhány másodperc múlva leengedi a vizet, de nem teljesen.
Tehát azt látjuk, hogy üledék van az alján. Ez keményítő. Most adjunk időt, hogy megszáradjon.
A gyermek vesz egy darab száraz keményítőt, és elkezdi megvizsgálni, kimondja érzéseit, ezáltal megnevezi a keményítő tulajdonságait.
A keményítő tapintásra csikorog
Nincs szaga
Nincs íze
Anya azt mondja, hogy a jód segítségével meghatározhatja a keményítő jelenlétét a termékben. PRÓBÁLJUK MEG. Lássuk, mi történik a keményítővel, ha hozzáadunk egy csepp jódot. Nézd, milyen színű a jód? (jóddal festett pipetta látható). Most igyunk két pohár vizet. Az egyikhez keményítőt adunk és keverjük, a másikhoz csak vizet. Cseppents jódot mindkét pohárba.
Az egyik pohárban a víz megsárgult, a keményítős pohárban pedig a színe lettsötét lila).
A jód keményítővel megváltoztatta a víz színét.
Kíváncsi vagyok, milyen egyéb élelmiszerek tartalmaznak jódot? (tányér burgonyával, sajttal, sütivel, kukoricával, kolbásszal és zsemlével). Ne feledje, hogy a jód a keményítőt színezi Kék szín.
A gyermek egyenként jódot csepegtet minden termékre, majd megvizsgálja, következtetéseket von le.
A jód kékre színezte a burgonyát, a kekszeket, a kenyeret és a kukoricát. Ez azt jelenti, hogy ezek a termékek keményítőt tartalmaznak. Kíváncsi vagyok, használnak-e máshol keményítőt? Például: amikor apám munkába készül, megkérdezi anyámat, hogy keményítette-e az ingét. Ennek nekem sincs értelme. Vegyük a ruhákat, és tegyük keményítős vízbe.
A baba ruháját a gyermek többször kiöblíti, és felakasztja egy madzagra. Aztán veszi a munkadarabot, és „leteszi” az asztalra.
Ezt jelenti a keményített!
Keményítőből is készítenek ragasztót. Úgy hívják, hogy paszta, és a tanárommal mi magunk készítjük az óvodában!
Annyit tanultam ma: a keményítő megtalálható különféle zöldségekben és gyümölcsökben, és otthon is beszerezhető. Szagtalan és íztelen. A jód segítségével meghatározhatja a keményítő jelenlétét az élelmiszerekben. A főzéshez is szükséges: szószok, sütemények, joghurtok, kenyér, tészta egyszerűen nem készülhet el nélküle. A keményítőt szövetfeldolgozásra, valamint papírtermékek előállítására is használják. De a legfontosabb, hogy nélküle nem készült volna el a kedvenc KISSEL-em!
Rendkívüli keményítő
előkészítő csoport
„A legjobb felfedezés az
amit a gyerek maga csinál"
Ralph Waldo Emerson
Cél: Fogyatékos gyermekek kognitív érdeklődésének fejlesztése ép elemzőkre (auditív, szagló, tapintható, vizuális elemzők) alapuló kísérleti tevékenységekkel. A látássérült gyermekek motivációjának megteremtése a kísérleti tevékenységek használatára.
Feladatok:
- A fogyatékkal élő gyermekek készségeinek fejlesztése, tárgyak és jelenségek ép elemzőkkel történő vizsgálata, minták azonosítása.
- A játéktechnológián keresztül segítse a gyerekeket konkrét elképzelések felhalmozódásában tárgyakról és tulajdonságaikról.
- Fejlessze a mentális műveleteket, a hipotézisek felállításának és a következtetések levonásának képességét.
- Bátorítsa a gyerekeket, hogy legyenek aktívak a problémás helyzet megoldása érdekében.
- Hozzájárulni az önállóság és a kommunikációs készségek fejlesztéséhez.
Valószínűleg sokan egyetértenek velem abban, hogy mi lehet szebb az érintésnél? Amikor érintést érzel, könnyedséget vagy nehézséget, érdességet és lágyságot, plaszticitást, keménységet, áramlást érez. Ezek a hihetetlen érzések azok az információk, amelyeket testünk nyújt számunkra.
Természetesen és szép képek, és kellemes hangzású, finom aromái vannak nagyon fontos, de pontosan tapintási érzések a legerősebb és legjelentősebb, mert nem hiába az emberi bőr a legtöbb nagy orgona. A tapintható megismeréssel kezdődik egy kis ember megismerkedése a világgal.
Relevancia
- A kísérleti tevékenységek valódi ötleteket adnak a gyerekeknek különböző oldalak a vizsgált objektumról, más tárgyakkal való kapcsolatairól. Ennek az az oka, hogy az óvodáskorú gyermekek vizuálisan hatékony és vizuálisan fantáziadús gondolkodásúak, és a kísérletezés, mint semmi más módszer, ezeknek felel meg. életkori jellemzők. BAN BEN óvodás korúő a vezető, és az élet első három évében - gyakorlatilag az egyetlen módja a világ ismerete. Minél változatosabb és intenzívebb a keresési tevékenység, annál több új információ a gyerek megkapja. Minél gyorsabban és teljesebben fejlődik.
- A kísérleti munka fejleszti a gyermekek kognitív tevékenységét, érdeklődést kelt a keresési tevékenységek iránt, ösztönzi az új ismeretek megszerzését. Bővül a horizont, különösen a természettel és a benne előforduló összefüggésekkel kapcsolatos ismeretek gazdagodnak; a különféle anyagok tulajdonságairól, az emberek tevékenységük során történő felhasználásáról
- Különös társadalmi és pedagógiai jelentősége van a gyermekeknek nyújtott aktív, differenciált segítségnyújtásnak.fogyatékkal élőkkel.
- Korlátozott lehetőségek az egészségi állapot befolyásolja a gyermek társadalmi helyzetét, az őt körülvevő világhoz való hozzáállását, ami csökkenti a tevékenységi motivációt, a mozgással és kommunikációval kapcsolatos félelmeket, valamint a társadalmi kapcsolatok korlátozásának vágyát.
Hogyan képzeled el a folyadékot? Milyen tulajdonságokkal kell rendelkeznie? Először is valószínűleg folynia, szétterülnie és így tovább, és semmiképpen sem bírja el egy személy súlyát vagy nem foglal el. függőleges helyzet, de a mi világunkban nem minden ilyen egyszerű, vannak speciális folyadékok, amelyek kicsit furcsán viselkednek - nem newtoni folyadékok.
Érdekelne szokatlan tulajdonságok ilyen folyadékokat és több kísérletet is végzett gyerekekkel.
Hipotézis: Feltételezem, hogy a nem-newtoni folyadék olyan keverék, amely a folyadékok tulajdonságaival, valamint néhány „speciális” tulajdonsággal rendelkezik.
Dióhéjban a nem newtoni folyadék egy szokatlan folyadék, amely a rá gyakorolt hatástól függően eltérően viselkedik.
Ez egy nagyon érdekes anyag a gyermekek kísérleteihez. Ha összenyomod, szilárd, ha nem csinálsz semmit, akkor folyékony. Ha eldobod, széthasad, de csak pislog, és egy folyékony tócsa van előtted. Ideális a gyerekek tapasztalataihoz és világunk megismeréséhez.
A természetben ilyen folyadékra példa egy közönséges mocsár vagy futóhomok.
Észrevettük az első szokatlan dolgokata folyadékkeverési szakaszban.Megjelenésében és állagában hasonló a palacsintatésztához. De elég nehéz megkeverni - minden erejével a kezeden nyugszik. Úgy tűnik, hogy a keményítő soha nem fog feloldódni vízben. És valóban, nem fog feloldódni. Ezért van a folyadékban ilyen érdekes tulajdonságok. Szuszpenziót kapunk - ennek a folyadéknak a részecskéi elkülönülnek egymástól és a víztől.
De amint abbahagytuk a keményítő keverését, láttuk, hogy a folyadék már összekeveredett, sőt nagyon homogénnek bizonyult. Most már játszhatsz vele, és tanulmányozhatod a tulajdonságait. Aztán miegyszerűen tapintással tanulmányoztuk.Ha gyorsan összegyúrod az ujjaiddal, egy marékba kanalazod, és csomókat csinálsz belőle, akkor keménynek tűnik. De amint abbahagyja, az összes csomó szó szerint átfolyik az ujjain. Ha erőt alkalmazol rá, pl. ütni, szorítani, nyomni - kemény lesz, aminek köszönhetően akár futni is lehet rajta. Semmi bonyolult! Minden igazán zseniális az egyszerűségig. Így viselkedik a keményítő vízzel keverve. Tehát az ilyen kísérletek biztonságosak bármilyen korú gyermekek számára! Az egyetlen veszély egy nem newtoni folyadékÉdesanyám konyhájának tisztaságát képviseli, ez már önmagában is egy nagyon szokatlan jelenség, amivel sokáig lehet bütykölni!Egy ilyen kísérlet elvégzése után a gyerekek önállóan végezhetik el, és hangosan elmagyarázhatják cselekedeteiket. És ez nagyon fontos a fejlődési fogyatékos gyerekek számára.
Te is az órajátékok folyadékba ragadnak. Ha élesen „taposod” őket a felszínen, könnyen „átszaladnak” a tálon a vízen, mintha a szárazföldön lennének. De ha tétováznak egy helyen, azonnal megfulladnak. És néhány másodpercen belül teljesen elmerülnek egy ingoványban, ahonnan aztán nagyon nehéz kihúzni őket.
Saját tapasztalatunkból éreztük, mi történik, ha egy mocsár vagy futóhomok beszippant minket. Így alakul!
A srácoknak sok benyomásuk és új szenzációik vannak!Ezt nem lehet képekkel vagy szavakkal átadni. Csak hígítsa fel a keményítőt vízzel, és mindent meg fog érteni!
Ezt követően úgy döntöttünk, hogy egy újabb transzformációs kísérletet végzünk. A vízhez egy kanál keményítőt adtak és jódoldatot csepegtettek bele, és a gyerekek szeme láttára a folyadék megkékült, majd a jódszínű keményítőhöz aszkorbinsavat adtak és elszíneződött.
Kísérletet végeztünk, hogy kiderítsük a keményítő jelenlétét a termékekben. Ha egy csepp jód esik a keményítőt tartalmazó élelmiszerekre, azok kék színűvé válnak. A gyerekasztalokon termékek: alma, nyers burgonya, uborka, hagyma, kenyér. A gyerekek jódot csepegtetnek, és meghatározzák, hogy mely élelmiszerek tartalmaznak keményítőt.
Öntsön keményítőt egy léggömbbe, és kösse össze egy tölcsér segítségével.
A labda eléri a kívánt hangerőt. A benne lévő keményítő miatt bármilyen formát felvehet. Vicces arcot rajzoltunk a játékra.Elkészült a cuki "mnushka"!
KÖVETKEZTETÉS
„Tudni akarok”, „Akarom tudni”, „Érdekel” - egy ilyen kognitív szükséglet, amelynek megnyilvánulása a kognitív érdekek, nagymértékben meghatározza az egyén fejlődését.
A nem hagyományos kísérleti tevékenységek értéke a gyermekek számára vizuális patológia annyiban, hogy lehetőséget biztosít a fogyatékos gyerekeknek a hozzájuk közel álló és természetes gyakorlati cselekvések révén, ép elemzőkre alapozva, hogy bővítsék az őket körülvevő világ megértését.
A konyha a családunk életének központja. Itt teát isznak és megbeszélik utolsó hírés persze vegyszereket használnak.
Vladik és én kémiázunk, sok könyvet olvastunk, Makarka pedig a saját programja szerint kémiázik - vagy sót önt a teába, vagy megkóstolja a mosogatószert. Jó móka a konyhánkban.
A téma folytatása mutatók a konyhában Egy csodálatos anyagról fogok írni, amellyel csodálatos kísérleteket végezni gyermekével. Ez a szokásos burgonyakeményítő. Fantasztikus kísérleteket is végezhet kukoricával, de ma nem erről beszélünk.
Kísérletek keményítővel és jóddal
Jóddal kékre színezheti a burgonyát.
A jód a keményítő kék színűvé válik - ez egy olyan anyag, amely nagyon bőséges a burgonyában. Ezért gyakran végeznek kísérleteket kék burgonyával. Úgy döntöttünk, hogy megnézzük a hűtőszekrényben talált élelmiszereket keményítő jelenlétére. Jódot csepegtettünk citromra, daikonra, almára, nyers burgonya, főtt krumpli, főtt sárgarépa, fokhagyma, kolbász, disznózsír, kenyér, gabonafélék.
A kenyér és a burgonya élénk színű, míg a főtt burgonya, a zabpehely és a sárgarépa aktívabban reagált. Megállapíthatjuk, hogy ezek a termékek keményítőt tartalmaznak, míg a többiben vagy nincs, vagy elenyésző a mennyisége.
Felhívjuk figyelmét, hogy a főtt burgonya színe világosabb, mint a nyers. Egy könyvben találtam egy ilyen magyarázatot a gyerekeknek. Keményítő található benne nyers zöldségek mintha dobozokban lennének, és főzéskor a dobozok megsemmisülnek, és könnyebben jut a jód a keményítőhöz és reagál vele.
Ebben a témában egy másik kísérletet is végeztek.
Keményítőből pasztát készítettünk. Vegyünk egy evőkanál keményítőt egy bögre vízhez. Tehát csészékben (balról jobbra):
- paszta + 2 csepp jód,
- keményítő vízben + 2 csepp jód,
- csak vizet jóddal.
A jód egyébként olajban jobban oldódik, mint vízben (ha valakinek jól jön).

Gyönyörűen sikerült! És nagyon jól látható, hogy a jód aktívabban reagált a pasztában lévő keményítővel.
Kísérletezzünk tovább!
Próbáljuk meg elszínezni a keményítőt – jódlilára!


Fekete lett! Külön elkészítjük 60 ml vízből és 1000 mg-ból álló oldatot C-vitamin. A gyógyszertárban vettünk aszkorbinsav tablettát (egyenként 50 mg), és 20 darabot összetörtünk. Csak az elején hatalmasat rontott a matematikám, és nem 20 darabot zúztam, hanem 200 darabot.
Aszkorbin oldat harcolni kezd a jóddal és legyőzi őt! Az oldat szinte elszíneződött.
Valószínűleg sokan megfeledkeztek róla egyszerű recept keményítő paszta. Ha igen, akkor szívesen segítünk. Barátaim, megpróbáljuk megmutatni nektek, hogy a tudomány szórakoztató. Ha pedig érdekes kérdései vannak, amelyekre szakértő választ szeretne kapni, írjon nekünk. A „PocheMuk” rovat következő számaiban válaszolunk rájuk. Csináljunk együtt szórakoztató tudományt. +100500 a karmához azok számára, akik cikkeket osztanak meg weboldalunkról a közösségi hálózatokonés mesél rólunk a barátainak. Hamarosan találkozunk, barátaim.
Jó kísérletezést! A tudomány szórakoztató!
Az ön Galina Kuzmina
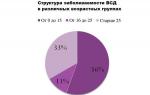
A jód kémiai elem D. I. Mengyelejev táblázatában az 53. számú, a nem radioaktív nemfémek közé tartozik. Ez kémiai elem nagyon fontos az ember életében. A testben lévő jódhiány miatt a fizikai és szellemi fejlődés késik, és az ember növekedése visszamarad. A jódhiány miatt endemikus golyva is kialakul. Bár a szervezet jódtartalma alacsony (25 mg), jelentősége a szervezet számára nem csökken. Részt vesz az anyagcsere folyamatokban is. A jód főként a szervezetben található pajzsmirigy. Ezért nagyon fontos, hogy további jódot fogyasszunk az élelmiszerekben. A jód a természetben is megtalálható, például az algákban. Bizonyos reakciók során kémiailag is előállítható.
A jód felfedezésének története
A felfedezések során mindig minden egyszerűnek és véletlennek bizonyul. Mindez a macska miatt volt, aki elkapta az oldatokat a lombikokban. Az egyik lombik tartalmazott maradványokat jodid sók nitrát előállítása után, a másikban - kénsav. A macska gazdája, Bernard Courtois francia kémikus heves reakciót észlelt e két komponens összekeverésekor ibolyagőzök felszabadulásával, amely nélkül nem tudjuk elképzelni az életet.
Kísérletek jóddal
A jód nagyon jó indikátor, így bármilyen reakció ezzel az elemmel nagyon könnyen megfigyelhető. A kísérletek egyszerűek és tanulságosak, otthon is könnyen elvégezhetők, és megmutatják, milyen érdekes a kémia tudománya. Kattintson ide, ha megtudja, hogyan készíthet ujjlenyomatokat jóddal.
Tapasztalja meg a „Keményítő keresését”
Ezzel a kísérlettel vizuálisan láthatjuk, hogy mely élelmiszerek tartalmaznak jódot és milyen mennyiségben. Szükségünk lesz: jódoldat (5%); keményítő; 3) pipetta; 4) eldobható üveg; 5) keményítőt tartalmazó és keményítő nélküli termékek.

Még egy gyermek is elvégezheti ezt a kísérletet. Először jódoldatot készítünk: veszünk egy poharat, öntsünk bele vizet, és csepegtessünk bele pár csepp jódot. Kész a megoldás! Most vesszük az ételt és tányérra tesszük: kenyér, zabpehely, nyers krumpli, főtt krumpli, citrom, retek, sárgarépa, uborka. Cseppentsünk néhány csepp jódoldatot a tetejére, és figyeljük a reakciót. Kék lett a kenyér, a zabpehely, a nyers és a főtt krumpli. Következtetésünk: ezek a termékek keményítőt tartalmaznak. Főtt burgonyában sokkal több van belőle, hiszen telítettebb a színe. De a retekben, citromban és uborkában nincs keményítő. Ezzel az egyszerű kísérleti módszerrel egyértelműen ellenőriztük a termékek jódtartalmát.
Kísérlet „Keményítő kölcsönhatása jóddal”
 A búzakeményítő granulátum jóddal reagált
A búzakeményítő granulátum jóddal reagált
A jóddal végzett kísérlethez szükségünk lesz:
1) keményítő; 2) 3 pohár; 3) víz; 4) jód.
Keményítőből pasztát készítünk. Fogunk 3 poharat, és felöntjük: az első pohárba paszta, a másodikba keményítő és víz, a harmadikba csak víz. És cseppentsen néhány cseppet minden tartályba. Nézzük az eredményt. Az első üvegben mélykék színű oldatot látunk, a másodikban - világoskék, a harmadikban - világosbarna. Megállapítható, hogy a reakció legaktívabban a pasztával ment végbe. A hőkezelt gyorsabb reakciót adott.
Kísérlet „A jód színtelenítése”
Jól látható a reakció a jód és az aszkorbinsav között. Szükségünk lesz:
- jód oldat;
- 2 pohár;
- aszkorbinsav oldat;
- víz.
Az aszkorbinsav oldatához 20 tablettára és 60 ml vízre van szükségünk. Ezután öntsünk jódot a keményítős vízbe. Gazdag kék színt kapunk. Ezután keverje össze az aszkorbinsav-oldatot a jódoldattal. Az oldat azonnal elszíneződik. Ez olyan "varázslat"! A kémia csodákra képes! Ilyen vizuális kísérletek Ezt jóddal megteheti gyermekével, ha szabad. Az ilyen oktatási kísérletekre gyermekei sokáig emlékezni fognak.
Miért feketülnek a gyümölcskések??!
Miért feketülnek a gyümölcskések?
Ha valamilyen gyümölcsléhez vassóoldatot adunk (egy vassóoldatot otthon is könnyen lehet kapni, ha például egy szöget vagy több gombot vagy gemkapcsot fél órára réz-szulfátba mártunk), a folyadék azonnal elsötétül. . Gyenge tinta oldatot kapunk. A gyümölcsök tartalmaznak csersav, amely vassóval tintát képez. A vassóoldat otthoni elkészítéséhez mártson egy szöget az oldatba rézszulfátés várj tíz percet. Ezután engedjük le a zöldes oldatot. A keletkező vas-szulfát oldat (FeSO 4) felhasználható reakciókban.
A tea csersavat is tartalmaz. A gyenge teaoldathoz hozzáadott vassó-oldat a tea színét feketére változtatja. Éppen ezért nem ajánlott fém teáskannában teát főzni!
Kémiai reakciók Val vel asztali só
Néha az asztali sót speciálisan jódozzák, azaz nátrium- vagy kálium-jodidot adnak hozzá. Ez azért van így, mert a jód a szervezet különböző enzimeinek része, hiányával pedig a pajzsmirigy működése romlik.
 Réz-szulfát konyhasó oldatai ( Zöld szín)
Réz-szulfát konyhasó oldatai ( Zöld szín)
Az adalékanyag nagyon könnyen felismerhető. Meg kell főzni a keményítőpasztát: egy pohárban hígítson fel negyed teáskanál keményítőt hideg víz, forraljuk fel, forraljuk öt percig, majd hűtsük le. A paszta sokkal érzékenyebb a jódra, mint a száraz keményítő. Ezután egy teáskanál só harmadát feloldjuk egy teáskanál vízben, és néhány cseppet adunk a kapott oldathoz. ecet esszencia(vagy fél teáskanál ecet), fél teáskanál hidrogén-peroxid és két-három perc múlva - néhány csepp paszta. Ha a sót jódozták, akkor a hidrogén-peroxid kiszorítja a szabad jódot:
2I-+H2O2+2CH3COOH→I2+2H2O+2CH3COO-,
amitől kék lesz a keményítő. (A kísérlet nem fog működni, ha KI helyett KClO 3-at használtunk a só jódozására). Végre lehet hajtani kísérletezzen réz-szulfáttal és konyhasóval. A fenti reakciók egyike sem lép fel itt. De a reakció gyönyörű... Vitriol és só keverésekor figyeljük meg a nátrium-tetraklór-kuprát Na 2 gyönyörű zöld oldatának képződését
Szórakoztató kísérletek kálium-permanganáttal:
Oldjunk fel néhány kristály kálium-permanganátot vízben, és várjunk egy kicsit. Észre fogja venni, hogy az oldat bíbor színe (amit az oldatban lévő permanganátionok jelenléte magyaráz) fokozatosan halványabb lesz, majd teljesen eltűnik. barna bevonat mangán(IV)-oxid:
4KMnO4+2H2O→4MnO2+4KOH+3O2
Azokat az edényeket, amelyekben a kísérletet végezte, könnyen megtisztíthatja a lerakódásoktól citrom- vagy oxálsavoldattal. Ezek az anyagok a mangánt +2 oxidációs állapotra redukálják és vízoldható komplex vegyületekké alakítják. A kálium-permanganát oldatok sötét palackokban évekig tárolhatók. Sokan azt hiszik, hogy a kálium-permanganát jól oldódik vízben. Valójában ennek a sónak az oldhatósága at szobahőmérséklet(20 °C) csak 6,4 g/100 g víz. Az oldat azonban olyan intenzív színű, hogy töménynek tűnik.
Ha a kálium-permanganátot 200 0 C-ra melegítjük, akkor a kálium-permanganát sötétzöld kálium-manganáttá (K 2 MnO 4) alakul. Ugyanakkor kiemelkedik nagyszámú tiszta oxigén, amely összegyűjthető és felhasználható más kémiai reakciókhoz. A kálium-permanganát oldat különösen gyorsan romlik (szétbomlik) redukálószerek jelenlétében. Például egy redukálószer etanol C2H5OH. A kálium-permanganát reakciója alkohollal a következőképpen zajlik:
2KMnO4 +3C 2H 5OH→ 2KOH+2MnO2 +3CH 3 CHO+2H 2O.
Kálium-permanganát mosószer:
Hogy házi készítésűt készítsek" mosószer“, össze kell keverni a kálium-permanganátot savval. Persze nem mindenkivel. Egyes savak maguk is oxidálódhatnak; különösen, ha vesszük sósav, mérgező klór szabadul fel belőle:
2KMnO4+16HCl → 2MnCl2+5Cl2+2KCl+8H2O.
Sokszor így kapják meg laboratóriumi körülmények. Ezért céljainkra jobb, ha hígított (körülbelül 5 százalékos) kénsavat használunk. BAN BEN utolsó lehetőségként helyettesíthető hígított ecetsavval - asztali ecettel. Vegyünk körülbelül 50 ml (negyed csésze) savas oldatot, adjunk hozzá 1-2 g kálium-permanganátot (egy kés hegyével) és alaposan keverjük össze. fa bot. Ezután folyó víz alatt leöblítjük, és a végére kötünk egy darab habszivacsot. Ezzel az „ecsettel” gyorsan, de óvatosan eloszlatjuk az oxidáló keveréket a mosogató szennyezett felületén. Hamarosan a folyadék színe sötét meggyre, majd barnára változik. Ez azt jelenti, hogy az oxidációs reakció javában zajlik. Itt meg kell tenni néhány pontot. Nagyon óvatosan kell dolgoznia, hogy a keverék ne kerüljön a kezére és a ruhájára; Jó lenne olajszövet kötényt viselni. És ne habozzon, mivel az oxidáló keverék nagyon maró hatású, és idővel még a habgumit is „megeszi”. Használat után a hab „kefét” be kell meríteni egy korábban előkészített vízbe, öblíteni és eldobni. A mosogató ilyen tisztítása során megjelenhet rossz szag, amelyet a cserépedényeken és önmagán lévő szerves szennyeződések nem teljes oxidációjának termékei állítanak elő ecetsav, ezért a helyiséget szellőztetni kell. 15-20 perc elteltével a megbarnult keveréket vízsugárral mossuk le. És bár a mosogató borzalmas formában fog megjelenni - mindezt barna foltok borítják, aggodalomra semmi ok: a kálium-permanganát - mangán-dioxid MnO 2 redukciójának terméke könnyen eltávolítható az oldhatatlan mangán (IV) mennyiségének csökkentésével. vízben jól oldódó mangánsó.
De amikor a kálium-permanganát tömény kénsavval reagál, mangán-oxid (VII) Mn 2 O 7 képződik - olajos sötétzöld folyadék. Ez az egyetlen folyadék normál körülmények között fém-oxid (olvadáspont: 5,9 °C). Nagyon instabil és enyhe melegítés hatására (hőmérséklet=55°C) vagy ütés hatására könnyen felrobban. A Mn 2 O 7 még a KMnO 4-nél is erősebb oxidálószer. Ha érintkezik vele, sok szerves anyag, például etil-alkohol meggyullad. Egyébként ez az egyik módja annak, hogy gyufa nélkül gyújtsunk szellemlámpát!
Szórakoztató kísérletek hidrogén-peroxiddal
A hidrogén-peroxid lehet oxidálószer (ez a tulajdonság széles körben ismert) és redukálószer is! Ez utóbbi esetben oxidáló anyagokkal reagál:
H 2O 2 -2e → 2H + +O 2. A mangán-dioxid éppen ilyen anyag. A vegyészek az ilyen reakciókat „a hidrogén-peroxid reduktív bomlásának” nevezik. A gyógyszerészeti peroxid helyett használhat hidroperit tablettákat - hidrogén-peroxid vegyületet karbamiddal, amelynek összetétele CO (NH 2) 2 H 2 O 2. Nem kémiai vegyület, mivel a karbamid és a hidrogén-peroxid molekulák között nincsenek kémiai kötések; A H 2 O 2 molekulák a karbamidkristályok hosszú, keskeny csatornáiban vannak, és nem távozhatnak onnan, amíg az anyag fel nem oldódik vízben. Ezért az ilyen kapcsolatokat bekapcsolási csatornakapcsolatoknak nevezzük. Egy hidroperit tabletta 15 ml (evőkanál) 3%-os H 2 O 2 oldatnak felel meg. A H 2 O 2 1%-os oldatának elkészítéséhez vegyen be két hidroperit tablettát és 100 ml vizet. Ha mangán-dioxidot használ a hidrogén-peroxid oxidálószereként, ismernie kell egy finomságot. A MnO 2 jó katalizátor a H 2 O 2 vízzé és oxigénné történő lebomlásához:
2H 2O 2 → 2H 2O+O 2.
És ha egyszerűen kezeli a mosogatót H 2 O 2 oldattal, akkor azonnal „forr”, oxigént szabadít fel, és a barna lerakódás megmarad, mert a katalizátort nem szabad elfogyasztani a reakció során. A H 2 O 2 katalitikus bomlásának elkerülése érdekében szükséges savas környezet. Itt az ecet is beválik. A gyógyszertári peroxidot erősen hígítjuk vízzel, adjunk hozzá egy kis ecetet, és ezzel a keverékkel töröljük át a mosogatót. Valóságos csoda fog történni: a piszkosbarna felület fehéren csillog és olyan lesz, mint az új. És a csoda a reakcióval teljes összhangban történt
MnO 2 + H 2 O 2 + 2H + → Mn 2+ + 2 H 2 O + O 2.
Nem marad más hátra, mint egy vízsugárral lemosni a jól oldódó mangánsót. Ugyanígy megpróbálhatja megtisztítani a piszkos alumínium serpenyőt: erős oxidálószerek jelenlétében ennek a fémnek a felületén erős védő oxidfilm képződik, amely megvédi a savban való feloldódástól. A zománcozott termékeket (edényeket, fürdőkádakat) azonban nem szabad ezzel a módszerrel tisztítani: a savas környezet lassan tönkreteszi a zománcot. Vizes oldatok is használhatók a MnO 2 lerakódások eltávolítására. szerves savak: oxálsav, citromsav, borkősav, stb. Sőt, nincs szükség speciális savanyításukra – a savak maguk is meglehetősen savas környezetet hoznak létre vizes oldatban.
Szórakoztató kísérletek

"Arany" lombikban
Persze az arany nem az igazi, de az élmény gyönyörű! A kémiai reakcióhoz szükségünk van egy oldható ólomsóra (kék acetát (CH 3 COO) 2 Pb - az ólom ecetsavban való feloldásával keletkezett só) és egy jódsóra (például kálium-jodid KI). Az ólom-acetátot házilag is beszerezhetjük, ha egy darab ólmot ecetsavba mártunk. A kálium-jodidot néha elektronikus áramköri lapok maratására használják
Kálium-jodid és ecetsav az ólomban - kettő tiszta folyadékok, Által kinézet nem különbözik a víztől.
Kezdjük el a reakciót: adjunk ólom-acetát oldatot kálium-jodid oldathoz. Két átlátszó folyadék kombinálásával figyeljük meg az aranysárga csapadék képződését - ólom-jodid PbI 2 - látványos! A reakció a következőképpen megy végbe:
(CH 3 COO) 2 Pb+KI→ CH 3 FŐZÉS+PbI 2
Szórakoztató kísérletek írószer ragasztóval
Az írószer ragasztó nem más, mint a folyékony ill kémiai név"nátrium-szilikát" Na 2 SiO 3 Azt is mondhatjuk - ez a kovasav nátriumsója. Ha ecetsav oldatot ad a szilikát ragasztóhoz, az oldhatatlan kovasav - hidratált szilícium-oxid - kicsapódik:
Na 2 SiO 3 + 2CH 3 COOH → 2CH 3 COONa + H 2 SiO 3 .
A keletkezett H 2 SiO 3 csapadék szárítószekrényben szárítható és hígított vízoldható tinta oldattal hígítható. Ennek eredményeként a tinta leülepedik a szilícium-oxid felületén, és nem mosható le. Ezt a jelenséget adszorpciónak nevezik (a latin ad – „on” és a sorbeo – „elszívom” szóból).
Még egy gyönyörű szórakoztató élmény folyékony üveg . Szükségünk lesz réz-szulfátra CuSO 4-re, nikkel-szulfátra NiS0 4-re, vas-kloridra FeCl 3-ra. Készítsünk vegyi akváriumot. Magas üveg korsó vízzel felére hígított szilikát ragasztóval nikkel-szulfát és vas-klorid hígított vizes oldatát egyszerre öntik két pohárból. A tégelyben fokozatosan nőnek a sárga-zöld szilikát „algák”, amelyek összefonódva felülről lefelé ereszkednek. Most cseppenként csepegtessünk réz-szulfát oldatot az edénybe, és töltsük be az akváriumot „tengeri csillaggal”. Az algák növekedése a vas-, réz- és nikkel-hidroxidok és -szilikátok kristályosodásának eredménye, amelyek cserereakciók eredményeként keletkeznek.
Érdekes kísérletek jóddal
Adjunk néhány csepp hidrogén-peroxidot H 2 O 2 a jódotinktúrához, és keverjük össze. Egy idő után fekete fényes csapadék válik ki az oldatból. Ez kristályos jód- vízben rosszul oldódó anyag. A jód gyorsabban kicsapódik, ha az oldatot kissé felmelegítjük forró víz. Peroxidra van szükség a tinktúrában található kálium-jodid KI oxidálásához (a jód oldhatóságának növelésére adják hozzá). A jód egy másik képessége, hogy a nem poláris molekulákból álló folyadékok (olaj, benzin stb.) vízből vonják ki a jódot, szintén a jód vízben való gyenge oldhatóságával függ össze. Adjunk hozzá néhány cseppet egy teáskanál vízhez napraforgóolaj. Keverjük össze, és nézzük meg, hogy az olaj és a víz ne keveredjen. Ha most két-három csepp jódotinktúrát csepegtetünk bele, és erőteljesen felrázzuk, az olajréteg sötétbarna színű lesz, a vízréteg pedig halványsárgává, i.e. a legtöbb a jód olajba kerül.
A jód nagyon maró hatású anyag. Ennek ellenőrzésére helyezzen néhány csepp jódotinktúrát egy fémfelületre. Egy idő után a folyadék elszíneződik, és folt marad a fém felületén. A fém jóddal reagálva sót, jodidot képez. A feliratok fémre történő felvitelének egyik módja a jód ezen tulajdonságán alapul.
Színes szórakoztató élmény ammóniával
Az "ammónia" alatt azt értjük vizes oldat ammónia (ammónia). Valójában az ammónia egy gáz, amely vízben oldva képződik új osztály kémiai vegyületek - "bázisok". Az alappal fogunk kísérletezni. Látványos kísérletet lehet végezni ammóniaoldattal ( ammónia). Az ammónia rézionokkal színes vegyületet képez. Vegyünk elő egy bronz vagy réz érmét sötét bevonatés töltsük meg ammóniával. Azonnal vagy néhány perc múlva az oldat kék színűvé válik. A légköri oxigén hatására a réz összetett vegyületet képezett - ammóniát:
2Cu+8NH3 +3H2O+O2 → 2(OH)
Szórakoztató kísérletek: mész oltás
A mészoltás a kalcium-oxid (CaO – égetett mész) és a víz közötti kémiai reakció. A következőképpen zajlik: