Продукти на окисляване на мастни киселини. Има специфичен път за окисление на мастни киселини. Образуване на ацетил-КоА и АТФ, използвайки примера на окисление на палмитоил-КоА
За да се преобразува енергията, съдържаща се в мастните киселини, в енергията на АТФ връзките, има метаболитен път за окисление на мастните киселини до CO 2 и вода, който е тясно свързан с цикъла на трикарбоксилната киселина и дихателната верига. Този път се нарича β-окисление, защото настъпва окисление на 3-тия въглероден атом на мастната киселина (β-позиция) в карбоксилна група и в същото време ацетилната група, включително С1 и С2 на оригиналната мастна киселина, се отцепва от киселината.
Елементарна схема на β-окисление
Реакциите на β-окисление протичат в митохондриитеповечето клетки в тялото (с изключение на нервните клетки). Мастните киселини, които навлизат в цитозола от кръвта или се появяват по време на липолизата на техните собствени вътреклетъчни TAG, се използват за окисляване. Общото уравнение за окисляването на палмитинова киселина е както следва:
Палмитоил-SCoA + 7FAD + 7NAD + + 7H 2 O + 7HS-KoA → 8Acetyl-SCoA + 7FADH 2 + 7NADH
Етапи на окисление на мастни киселини
1. Преди да проникне в митохондриалната матрица и да се окисли, мастната киселина трябва да активиратев цитозола. Това се постига чрез добавяне на коензим А към него, за да се образува ацил-SCoA. Acyl-SCoA е високоенергийно съединение. Необратимостта на реакцията се постига чрез хидролиза на дифосфат в две молекули фосфорна киселина.
Ацил-SCoA синтетазите се намират в ендоплазмения ретикулум, върху външната мембрана на митохондриите и вътре в тях. Има широка гама от синтетази, специфични за различни мастни киселини.
Реакция на активиране на мастни киселини
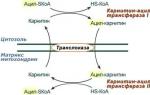
2. Acyl-SCoA не може да премине през митохондриалната мембрана, така че има начин да се транспортира в комбинация с витаминоподобно вещество карнитин. На външната мембрана на митохондриите има ензим карнитин ацилтрансфераза I.

Карнитин-зависим транспорт на мастни киселини в митохондриите
Карнитинът се синтезира в черния дроб и бъбреците и след това се транспортира до други органи. в вътрематочнопериод и в ранните годиниВ живота значението на карнитина за организма е изключително голямо. Снабдяване на нервната система с енергия на децататялото и по-специално мозъка се осъществява поради два паралелни процеса: карнитин-зависимо окисление на мастни киселини и аеробно окисление на глюкоза. Карнитинът е необходим за растежа на главния и гръбначния мозък, за взаимодействието на всички части на нервната система, отговорни за движението и мускулното взаимодействие. Има проучвания, свързващи дефицита на карнитин церебрална парализаи феномен" смърт в люлката".
Малките деца, недоносените бебета и децата с ниско тегло при раждане са особено чувствителни към дефицит на карнитин. Техните ендогенни резерви бързо се изчерпват при различни стресови ситуации (инфекциозни заболявания, стомашно-чревни разстройства, хранителни разстройства). Биосинтезата на карнитин е рязко ограничена поради ниската мускулна маса и приемът от обикновените храни не е в състояние да поддържа достатъчни нива в кръвта и тъканите.
3. След свързване с карнитина, мастната киселина се транспортира през мембраната чрез транслоказа. Тук, от вътрешната страна на мембраната, ензимът карнитин ацилтрансфераза II отново образува ацил-SCoA, който влиза в пътя на β-окислението.
4. Самият процес β-окислениесе състои от 4 реакции, повтарящи се циклично. Те се случват последователно окисление(ацил-SCoA дехидрогеназа), хидратация(еноил-SCoA хидратаза) и отново окисление 3-ти въглероден атом (хидроксиацил-SCoA дехидрогеназа). В последната, трансферазна реакция, ацетил-SCoA се отцепва от мастната киселина. HS-CoA се добавя към останалата (съкратена с два въглерода) мастна киселина и тя се връща към първата реакция. Това се повтаря, докато последният цикъл произведе две ацетил-SCoA.

Последователност от реакции на β-окисление на мастни киселини
Изчисляване на енергийния баланс на β-окисление
Преди това при изчисляване на ефективността на окисление коефициентът P/O за NADH беше приет равен на 3,0, за FADH 2 - 2,0.
По съвременни данни стойността на коефициента P/O за NADH съответства на 2,5, за FADH 2 – 1,5.
При изчисляване на количеството АТФ, образуван по време на β-окислението на мастни киселини, е необходимо да се вземе предвид:
- количеството образуван ацетил-SCoA се определя чрез обичайното разделяне на броя на въглеродните атоми в мастната киселина на 2.
- номер β-окислителни цикли. Броят на β-окислителните цикли е лесен за определяне въз основа на концепцията за мастната киселина като верига от двувъглеродни единици. Броят на прекъсванията между единиците съответства на броя на β-окислителните цикли. Същата стойност може да се изчисли с помощта на формулата (n/2 -1), където n е броят на въглеродните атоми в киселината.
- брой на двойните връзки в мастна киселина. При първата реакция на β-окисление се образува двойна връзка с участието на FAD. Ако двойна връзка вече присъства в мастната киселина, тогава няма нужда от тази реакция и FADN 2 не се образува. Броят на загубените FADN 2 съответства на броя на двойните връзки. Останалите реакции от цикъла протичат без промени.
- количеството ATP енергия, изразходвано за активиране (винаги съответства на две високоенергийни връзки).
Пример. Окисляване на палмитинова киселина
- тъй като има 16 въглеродни атома, β-окислението произвежда 8 ацетил-SCoA молекули. Последният влиза в цикъла TCA; когато се окислява в един оборот на цикъла, се образуват 3 молекули NADH (7,5 ATP), 1 молекула FADH 2 (1,5 ATP) и 1 молекула GTP, което е еквивалентно на 10 молекули на АТФ. И така, 8 молекули ацетил-SCoA ще осигурят образуването на 8 × 10 = 80 АТФ молекули.
- за палмитинова киселина броят на β-окислителните цикли е 7. Във всеки цикъл се произвеждат 1 молекула FADH 2 (1,5 ATP) и 1 молекула NADH (2,5 ATP). Влизайки в дихателната верига, те „дават“ общо 4 молекули АТФ. Така за 7 цикъла се образуват 7 × 4 = 28 молекули АТФ.
- двойни връзки в палмитинова киселина Не.
- 1 молекула АТФ се използва за активиране на мастната киселина, която обаче се хидролизира до АМФ, т.е. 2 макроергични връзкиили два ATP.
Така, обобщавайки, получаваме 80+28-2 =106 Молекулите на АТФ се образуват при окисляването на палмитинова киселина.
Биологичното окисление на мастните киселини може да се сравни с изгарянето на въглеводороди: и в двата случая се наблюдава най-висок добив на свободна енергия. По време на биологичното b-окисление на въглеводородната част на мастните киселини се образуват двувъглеродни активирани компоненти, които се окисляват допълнително в TCA цикъла и голям брой редуциращи еквиваленти, които водят до синтеза на АТФ в дихателната верига . Повечето аеробни клетки са способни на пълно окисляване на мастни киселини до въглероден диоксид и вода.
Източникът на мастни киселини са екзогенни или ендогенни липиди. Последните най-често са представени от триацилглицериди, които се отлагат в клетките като резервен източник на енергия и въглерод. В допълнение, клетките също използват липиди на полярната мембрана, чието метаболитно обновяване се извършва постоянно. Липидите се разграждат от специфични ензими (липази) до глицерол и свободни мастни киселини.
b-окисление на мастни киселини. Този основен процес на окисление на мастни киселини протича при еукариотите в митохондриите. Транспортът на мастни киселини през митохондриалните мембрани се улеснява от карнитин(g-триметиламино-b-хидроксибутират), който свързва молекулата на мастната киселина по специален начин, в резултат на което положителните (на азотния атом) и отрицателните (на кислородния атом на карбоксилната група) заряди се сближават заедно и взаимно се неутрализират.
След транспортиране в митохондриалната матрица, мастните киселини се активират от CoA в АТФ-зависима реакция, катализирана от ацетат тиокиназа (фиг. 9.1). След това производното на ацил-КоА се окислява с участието на ацил дехидрогеназа. В клетката има няколко различни ацил дехидрогенази, които са специфични за CoA производни на мастни киселини с различна дължина на въглеводородна верига. Всички тези ензими използват FAD като простетична група. FADH 2, образуван в реакцията като част от ацил дехидрогеназата, се окислява от друг флавопротеин, който пренася електрони към дихателната верига като част от митохондриалната мембрана.
Продуктът на окисление, еноил-КоА, се хидратира от еноил хидратаза до образуване на b-хидроксиацил-КоА (фиг. 9.1). Съществуват еноил-КоА хидратази, специфични за цис- и транс-формите на еноил-КоА производни на мастни киселини. В този случай транс-еноил-CoA се хидратира стереоспецифично в L-b-хидроксиацил-CoA, а цис-изомерите в D-стереоизомери на -b-хидроксиацил-CoA естери.
Последният етап в реакциите на b-окисление на мастни киселини е дехидрогенирането на L-b-хидроксиацил-CoA (фиг. 9.1). b-Въглеродният атом на молекулата претърпява окисление, поради което целият процес се нарича b-окисление. Реакцията се катализира от b-хидроксиацил-CoA дехидрогеназа, която е специфична само за L-формите на b-хидроксиацил-CoA. Този ензим използва NAD като коензим. Дехидрогенирането на D-изомерите на b-хидроксиацилКоА се извършва след допълнителен етап на изомеризация в L-b-хидроксиацил-КоА (ензим b-хидроксиацил-КоА епимераза). Продуктът от този етап от реакциите е b-кетоацил-CoA, който лесно се разцепва от тиолаза на 2 производни: ацил-CoA, който е по-къс от оригиналния активиран субстрат с 2 въглеродни атома, и ацетил-CoA двувъглероден компонент , отцепен от веригата на мастната киселина (фиг. 9.1) . Производното на ацил-КоА претърпява допълнителен цикъл от реакции на b-окисление и ацетил-КоА може да влезе в цикъла на трикарбоксилната киселина за по-нататъшно окисление.
Така всеки цикъл на b-окисление на мастни киселини се придружава от отделяне от субстрата на двувъглероден фрагмент (ацетил-CoA) и две двойки водородни атоми, редуциращи 1 молекула NAD + и една молекула FAD. Процесът продължава до пълното разграждане на веригата на мастната киселина. Ако мастната киселина се състои от нечетен брой въглеродни атоми, тогава b-окислението завършва с образуването на пропионил-CoA, който в хода на няколко реакции се превръща в сукцинил-CoA и в тази форма може да влезе в цикъла на TCA.
Повечето мастни киселини, които изграждат клетките на животни, растения и микроорганизми, съдържат неразклонени въглеводородни вериги. В същото време липидите на някои микроорганизми и растителни восъци съдържат мастни киселини, чиито въглеводородни радикали имат точки на разклонение (обикновено под формата на метилови групи). Ако има малко разклонения и всички те се срещат на четни позиции (при въглеродни атоми 2, 4 и т.н.), тогава процесът на b-окисление протича по обичайната схема с образуването на ацетил- и пропионил-CoA. Ако метиловите групи са разположени при нечетни въглеродни атоми, процесът на b-окисление се блокира на етапа на хидратация. Това трябва да се има предвид при производството на синтетични детергенти: за да се гарантира бързото им и пълно биоразграждане в околната среда, само версиите с прави въглеводородни вериги трябва да бъдат разрешени за масова употреба.
Окисляване на ненаситени мастни киселини. Този процес се извършва в съответствие с всички закони на b-окислението. Въпреки това, повечето естествено срещащи се ненаситени мастни киселини имат двойни връзки на места във въглеводородната верига, така че последователното отстраняване на двувъглеродни части от карбоксилния край произвежда ацил-CoA производно, в което двойната връзка е в позиция 3-4. В допълнение, двойните връзки на естествените мастни киселини имат цис конфигурация. За да се осъществи етапът на дехидрогениране с участието на b-хидроксиацил-CoA дехидрогеназа, специфична за L-формите на b-хидроксиацил-CoA, е необходим допълнителен етап на ензимна изомеризация, по време на който двойната връзка в получената от CoA молекула на мастна киселина се премества от позиция 3-4 в позиция 2-3 и конфигурацията на двойната връзка се променя от цис- на транс-. Този метаболит служи като субстрат за еноил хидратаза, която превръща транс-еноил-КоА в L-b-хидроксиацил-КоА.
В случаите, когато прехвърлянето и изомеризацията на двойна връзка са невъзможни, такава връзка се възстановява с участието на NADPH. Последващото разграждане на мастната киселина става чрез обичайния механизъм на b-окисление.
Второстепенни пътища на окисление на мастни киселини. b-окислението е основният, но не единствен път на катаболизъм на мастни киселини. Така в растителните клетки е открит процесът на а-окисление на мастни киселини, съдържащи 15-18 въглеродни атома. Този път включва първоначалната атака на мастна киселина от пероксидаза в присъствието на водороден пероксид, което води до отстраняване на карбоксилния въглерод като CO 2 и окисляване на въглерода в а-позиция до алдехидна група. След това алдехидът се окислява с участието на дехидрогеназа във висша мастна киселина и процесът се повтаря отново (фиг. 9.2). Този път обаче не може да осигури пълно окисляване. Използва се само за скъсяване на веригите на мастни киселини, а също и като байпас, когато β-окислението е блокирано поради наличието на метилови странични групи. Процесът не изисква участието на CoA и не е придружен от образуването на ATP.
Някои мастни киселини също могат да претърпят окисление при w-въглеродния атом (w-окисление). В този случай СН3 групата претърпява хидроксилиране под действието на монооксигеназа, по време на което се образува w-хидрокси киселина, която след това се окислява до дикарбоксилна киселина. Дикарбоксилната киселина може да бъде скъсена от двата края чрез b-окислителни реакции.

По същия начин в клетките на микроорганизмите и някои животински тъкани се случва разграждането на наситените въглеводороди. На първия етап, с участието на молекулярен кислород, молекулата се хидроксилира до образуване на алкохол, който последователно се окислява до алдехид и карбоксилна киселина, активира се чрез добавяне на CoA и влиза в b-окислителния път.
Както вече беше посочено, животинското тяло получава значителна част от енергията, извлечена по време на процеса на окисление, от мастни киселини, които се разграждат чрез окисление при β-въглеродния атом.
β-окислението на мастни киселини е изследвано за първи път през 19004 г. от F. Knoop. По-късно беше установено, че β-окислението се извършва само в митохондриите. Благодарение на работата на Ф. Линен и неговите колеги (1954-1958) са изяснени основните ензимни процеси на окисление на мастни киселини. В чест на учените, открили този път на окисляване на мастни киселини, процесът на β-окисление се нарича Цикъл на Кнуп-Ленен.
β-окисление- специфичен път на катаболизъм на мастна киселина, при който 2 въглеродни атома се отделят последователно от карбоксилния край на мастната киселина под формата на ацетил-КоА. Метаболитният път - β-окисление - е наречен така, защото реакциите на окисляване на мастни киселини протичат при β-въглеродния атом. Реакциите на β-окисление и последващо окисление на ацетил-КоА в цикъла на ТСА (цикъл на трикарбоксилната киселина) служат като един от основните източници на енергия за синтеза на АТФ чрез механизма на окислителното фосфорилиране. β-окислението на мастните киселини се извършва само при аеробни условия.
Всички многостепенни окислителни реакции се ускоряват от специфични ензими. β-окислението на висшите мастни киселини е универсален биохимичен процес, който се среща във всички живи организми. При бозайниците този процес протича в много тъкани, най-вече в черния дроб, бъбреците и сърцето. Окисляването на мастни киселини се случва в митохондриите. Ненаситените висши мастни киселини (олеинова, линолова, линоленова и др.) се редуцират предварително до наситени киселини.
Проникването на мастни киселини в митохондриалната матрица се предхожда от тяхното активиранечрез образуване на връзка с коензим А(HS~CoA), съдържаща високоенергийна връзка. Последното очевидно допринася за по-плавното протичане на окислителните реакции на полученото съединение, което се нарича ацил коензим А(ацил-КоА).
Взаимодействието на висшите мастни киселини с CoA се ускорява от специфични лигази - ацил-КоА синтетазитри типа, специфични съответно за киселини с къси, средни и дълги въглеводородни радикали. Те са локализирани в мембраните на ендоплазмения ретикулум и във външната мембрана на митохондриите. Всички ацил-КоА синтетази изглеждат мултимери; Така ензимът от чернодробните микрозоми има молекулно тегло 168 kDa и се състои от 6 идентични субединици. Реакцията на активиране на мастните киселини протича в 2 етапа:
а) първо, мастната киселина реагира с АТФ, за да образува ациладенилат:
RCOOH + ATP → RCO~AMP + FF
б) тогава настъпва образуването на активирана форма на ацил-КоА:
RCO~AMФ + NS~KoA → RCO~SKoA + AMF
Пирофосфатът (PP) се хидролизира бързо от пирофосфатаза, в резултат на което цялата реакция е необратима: PP + H 2 O → 2P
Обобщено уравнение:
RCOOH + ATP+ HS~CoA→ RCO~SKoA + AMF + 2P
Мастните киселини с къса и средна дължина на веригата (от 4 до 12 въглеродни атома) могат да проникнат в митохондриалната матрица чрез дифузия, където се извършва тяхното активиране. Дълговерижните мастни киселини, които преобладават в човешкото тяло (12 до 20 въглеродни атома), се активират от ацил-КоА синтетази, разположени върху външната мембрана на митохондриите.
Вътрешната митохондриална мембрана е непропусклива за образуваните в цитоплазмата ацил-КоА с дълга верига. Служи като носител на активирани мастни киселини карнитин (витамин Bt), който идва от храната или се синтезира от незаменимите аминокиселини лизин и метионин.
Външната мембрана на митохондриите съдържа ензим карнитин ацилтрансфераза I(карнитин палмитоилтрансфераза I), катализираща реакцията с образуването на ацилкарнитин:
RCO~SKoA + H 3 C- N + -CH 2 -CH-CH 2 -COOH ↔ H 3 C- N + -CH 2 -CH-CH 2 -COOH + HS~KoA
Ацил-КоА карнитин (B t) Ацилкарнитин коензим А
Този ензим е регулаторен, той регулира скоростта на навлизане на ацилни групи в митохондриите и следователно скоростта на окисление на мастни киселини.
Полученият ацилкарнитин преминава през междумембранното пространство до външната страна на вътрешната мембрана и се транспортира от карнитин ацилкарнитин транслоказа до вътрешната повърхност на вътрешната митохондриална мембрана, където ензимът карнитин ацилтрансфераза IIкатализира прехвърлянето на ацил към интрамитохондриален CoA, т.е. обратната реакция (фиг. 9).

Фиг.9. Трансфер на мастни киселини с дълги въглеводородни радикали през митохондриалните мембрани
По този начин ацил-КоА става достъпен за β-окислителните ензими. Свободният карнитин се връща в цитозолната страна на вътрешната митохондриална мембрана от същата транслоказа. След това ацил-КоА се включва в реакциите на β-окисление.
В митохондриалната матрица катаболизмът (разграждането) на ацил-КоА възниква в резултат на повтаряща се последователност от четири реакции.
1) Първата реакция във всеки цикъл е неговото окисление от ензима ацил-КоА дехидрогеназа, чийто коензим е FAD. Дехидрогенирането възниква между β и α въглеродните атоми, което води до образуването на двойна връзка във въглеродната верига и продуктът на тази реакция е еноил-CoA:
R-CH 2 -CH 2 CO~SKoA + FAD → R-CH=CHCO~SKoA + FADN 2
Ацил-КоА Еноил-КоА
2) Във втория етап от цикъла на окисляване на мастни киселини двойната връзка еноил-КоА се хидратира, което води до образуването на β-хидроксиацил-КоА. Реакцията се катализира от ензим еноил-КоА хидратаза:
R-CH=CHCO~SKoA +H 2 O → R-CH-CH 2 CO~SKoA
Еноил-КоА β-хидроксиацил-КоА
3) На третия етап от цикъла β-хидроксиацил-КоА претърпява дехидрогениране (второ окисление) с участието на ензима β-хидроксиацил-КоА дехидрогеназа, чийто коензим е НАД+. Продуктът от тази реакция е β-кетоацил-КоА:
R-CH-CH 2 CO~SKoA + NAD + → R-CОCH 2 CO~SKoA + NADH + H +
β-хидроксиацил-CoA β-кетоацил-CoA
4) Крайната реакция на цикъла на окисляване на мастни киселини се катализира от ацетил-КоА ацилтрансфераза (тиолаза). На този етап β-кетоацил-CoA реагира със свободен CoA и се разцепва, за да образува, първо, двувъглероден фрагмент, съдържащ двата крайни въглеродни атома на изходната мастна киселина под формата на ацетил-CoA, и второ, CoA естер на мастна киселина, сега съкратен с два въглеродни атома. По аналогия с хидролизата тази реакция се нарича тиолиза:
R-COCH 2 CO~SKoA + HS~KoA → CH 3 CO~SKoA + R 1 CO~SKoA
β-кетоацил-КоА Ацетил-КоА Ацил-КоА,
съкратен от
2 въглеродни атома
Съкратеният ацил-CoA след това претърпява следващия цикъл на окисление, започвайки с реакция, катализирана от ацил-CoA дехидрогеназа (окисляване), последвана от реакция на хидратация, втора реакция на окисление, реакция на тиолаза, т.е. този процес се повтаря многократно (фиг. 10).
β- Окисляването на висшите мастни киселини се извършва в митохондриите. В тях също са локализирани ензими на дихателния цикъл, което води до прехвърляне на водородни атоми и електрони към кислород в условията на окислително фосфорилиране на ADP, следователно β-окислението на висшите мастни киселини е източник на енергия за синтеза на АТФ.

Фиг. 10. Окисление на мастни киселини
Крайният продукт на β-окисление на висши мастни киселини с четен брой въглеродни атомие ацетил-КоА, А с нечетни- пропионил-КоА.
Ако ацетил-КоАнатрупани в тялото, тогава запасите от HS~KoA скоро ще бъдат изчерпани и окислението на висшите мастни киселини ще спре. Но това не се случва, тъй като CoA бързо се освобождава от ацетил-CoA. Редица процеси водят до това: ацетил-КоА се включва в цикъла на трикарбоксилните и дикарбоксилните киселини или глиоксилния цикъл, който е много близък до него, или ацетил-КоА се използва за синтеза на стероли и съединения, съдържащи изопреноидни групи, и т.н.
пропионил-КоА,който е крайният продукт на β-окислението на висши мастни киселини с нечетен брой въглеродни атоми, се превръща в сукцинил-КоА, който се използва чрез цикъла на трикарбоксилните и дикарбоксилните киселини.
Около половината от мастните киселини в човешкото тяло ненаситени .
β-окислението на тези киселини протича по обичайния начин, докато двойната връзка е между третия и четвъртия въглероден атом. След това ензимът еноил-КоА изомеразапремества двойната връзка от позиция 3-4 в позиция 2-3 и променя цис към транс конформация на двойната връзка, което е необходимо за β-окисление. В този цикъл на β-окисление не възниква първата реакция на дехидрогениране, тъй като двойната връзка в радикала на мастната киселина вече е налице. Освен това циклите на β-окисление продължават, не се различават от обичайния път. Основните пътища на метаболизма на мастни киселини са показани на фигура 11.

Фиг. 11. Основни пътища на метаболизма на мастни киселини
Наскоро беше открито, че в допълнение към β-окислението, основният път на катаболизъм на мастни киселини, мозъчната тъкан α-окисление на мастни киселинис броя на въглеродните атоми (C 13 -C 18), т.е. последователното елиминиране на едновъглеродни фрагменти от карбоксилния край на молекулата.
Този тип окисление е най-разпространено в растителните тъкани, но може да се появи и в някои животински тъкани. α-Окислението е циклично по природа и цикълът се състои от две реакции.
Първата реакция се състои от окисление на мастна киселина с водороден пероксид в съответния алдехид и CO 2 с участието на специфичен пероксидази:

В резултат на тази реакция въглеводородната верига се скъсява с един въглероден атом.
Същността на втората реакция е хидратацията и окислението на получения алдехид в съответната карбоксилна киселина под въздействието на алдехид дехидрогеназасъдържащи окислената форма на коензима NAD:
След това цикълът на α-окисление се повтаря отново. В сравнение с β-окислението, този тип окисление е енергийно по-неблагоприятен.
ω-Окисление на мастни киселини.В черния дроб на животните и някои микроорганизми има ензимна система, която осигурява ω-окисление на мастни киселини, т.е. окисление в крайната CH3 група, обозначена с буквата ω. Първо под влияние монооксигеназипротича хидроксилиране до образуване на ω-хидрокси киселина:

След това ω-хидрокси киселината се окислява до ω-дикарбоксилна киселина чрез действието на съответния дехидрогенази:
Така получената ω-дикарбоксилна киселина се скъсява от двата края чрез реакции на β-окисление.
Хидролиза триглицериди извършва се от панкреатична липаза. Оптималното му pH = 8, той хидролизира TG предимно в позиции 1 и 3, с образуването на 2 свободни мастни киселини и 2-моноацилглицерол (2-MG). 2-MG е добър емулгатор. 28% от 2-MG се превръща в 1-MG чрез изомераза. Повечето от 1-MG се хидролизира от панкреатична липаза до глицерол и мастна киселина.В панкреаса панкреатичната липаза се синтезира заедно с протеиновата колипаза. Колипазата се образува в неактивна форма и се активира в червата от трипсин чрез частична протеолиза. Колипазата, със своя хидрофобен домен, се свързва с повърхността на липидната капка, а хидрофилният му домен помага да се доближи активният център на панкреатичната липаза възможно най-близо до TG, което ускорява тяхната хидролиза.
|
Кафява мастна тъкан |
|
|
Количество |
Малък при възрастен, висок при новородено |
|
Локализация |
В чист вид: близо до бъбреците и щитовидната жлеза. Смесена мастна тъкан: между лопатките, на гърдите и раменете. |
|
Кръвоснабдяване |
Много добре |
|
Структурата на адипоцитите |
В цитоплазмата има много малки капчици мазнини, ядрото и органелите са разположени в центъра на клетката, има много митохондрии и цитохроми. |
|
термогенеза |
|
Окисляването настъпва в митохондриалната матрица. Първо се активира мастната киселина: 1 .В цитоплазмата на всяка киселина се активира с помощта на CoA-8H и ATP енергия. 2. Активната мастна киселина, ацил-КоА, се транспортира от цитозола в митохондриалната матрица (МС). CoA-8H остава в цитозола, а остатъкът от мастна киселина - ацил - се свързва с карнитин (от латински - карнитин - месо - карнитинът се изолира от мускулната тъкан) и образува ацил-карнитин, който навлиза в междумембранното пространство на митохондриите. От междумембранното пространство на митохондриите комплексът ацил-карнитин се прехвърля в митохондриалната матрица. В този случай карнитинът остава в междумембранното пространство. В матрицата ацилът се комбинира с CoA-8H. 3. Окисляване. В MC матрицата се образува активна мастна киселина, която впоследствие претърпява окислителни реакции до крайни продукти. При бета окисление СН2- групата в бета позицията на мастната киселина се окислява до С- групата. В този случай дехидрогенирането протича на два етапа: с участието на ацил дехидрогеназа (флавинов ензим, водородът се прехвърля към убихинон) и бета-хидроксиацил дехидрогеназа (водороден акцептор NAD+). Тогава бета-кетоацил-КоА, под действието на ензима тиолаза, се разпада на ацетил-КоА и ацил-КоА, съкратени с 2 въглеродни атома в сравнение с оригинала. Този ацил-КоА отново претърпява бета-окисление. Многократното повторение на този процес води до пълно разграждане на мастната киселина до ацил-КоА. Окисляване на мастни киселини. Включва 2 етапа: 1. последователно разцепване на двувъглероден фрагмент под формата на ацетил-КоА от С-края на киселината; 2. окисление на ацетил-КоА в цикъла на Кребс до CO2 и H2O. Енергийна стойност на окисление на мастни киселини. Стеаринова киселина (C 18) претърпява 8 цикъла на окисление с образуването на 9 ацетил-CoA.Във всеки цикъл на окисление се образува 8 * 5 ATP = 40 ATP, ацетил-CoA произвежда 9 * 12 ATP = 108 ATP. Общо: 148 ATP, но 1 ATP се изразходва за активиране на мастни киселини в цитозола, така че общата сума е 147 ATP
β - окисление на висши мастни киселини (HFA). Енергийна ефективност на процеса (за наситени и ненаситени мастни киселини). Влиянието на тъканното окисление на IVFA върху използването на глюкоза от тъканите.
β-окисление - специфичен път на катаболизъм на мастни киселини с неразклонени средни и къси въглеводородни вериги. β-окислението възниква в митохондриалната матрица, по време на което 2 С атома се отделят последователно от С края на FA под формата на ацетил-КоА. β-окислението на FA се извършва само при аеробни условия и е източник на големи количества енергия.β-окислението на FA се извършва активно в червените скелетни мускули, сърдечния мускул, бъбреците и черния дроб. FA не служат като източник на енергия за нервните тъкани, тъй като FA не преминават през кръвно-мозъчната бариера, като други хидрофобни вещества.β-окислението на FA се увеличава в периода след абсорбция, по време на гладуване и физическа работа. В същото време концентрацията на ФК в кръвта се повишава в резултат на мобилизирането на ФК от мастната тъкан.
LCD активиране
Активирането на FA възниква в резултат на образуването на високоенергийна връзка между FA и HSCoA с образуването на Acyl-CoA. Реакцията се катализира от ензима Acyl-CoA синтетаза:
RCOOH + HSKoA + ATP → RCO~SCoA + AMP+ PPn
Пирофосфатът се хидролизира от ензима пирофосфатаза: H 4 P 2 O 7 + H 2 O → 2H 3 PO 4
Ацил-КоА синтетазите се намират както в цитозола (на външната мембрана на митохондриите), така и в митохондриалния матрикс. Тези ензими се различават по своята специфичност за ФК с различна дължина на въглеводородна верига.
Транспорт LCD. Транспортирането на ФК в митохондриалната матрица зависи от дължината на въглеродната верига.
ФК с къса и средна дължина на веригата (от 4 до 12 С атома) могат да проникнат в митохондриалната матрица чрез дифузия. Активирането на тези FA се извършва от ацил-CoA синтетази в митохондриалния матрикс Дълговерижните FA първо се активират в цитозола (от ацил-CoA синтетази на външната митохондриална мембрана) и след това се прехвърлят в митохондриалния матрикс чрез специална транспортна система използване на карнитин. карнитин идва от храната или се синтезира от лизин и метионин с участието на витамин С.
Във външната мембрана на митохондриите ензимът карнитин ацилтрансфераза I (карнитин палмитоилтрансфераза I) катализира прехвърлянето на ацил от CoA към карнитин, за да се образува ацилкарнитин;
Ацилкарнитинът преминава през междумембранното пространство до външната страна на вътрешната мембрана и се транспортира от карнитин ацилкарнитин транслоказа до вътрешната повърхност на вътрешната митохондриална мембрана;
Ензимът карнитин ацилтрансфераза II катализира трансфера на ацил от карнитин към интрамитохондриален HSCoA, за да се образува Acyl-CoA;
Свободният карнитин се връща в цитозолната страна на вътрешната митохондриална мембрана от същата транслоказа.
Реакции β-окисление на FA
1. β-окислението започва с дехидрогениране на ацил-CoA от FAD-зависима ацил-CoA дехидрогеназа, образувайки двойна връзка (транс) между α- и β-C атомите на Enoyl-CoA. Редуцираният FADN 2, окисляващ се в CPE, осигурява синтеза на 2 ATP молекули;
2. Enoyl-CoA хидратазата добавя вода към двойната връзка на Enoyl-CoA, за да образува β-хидроксиацил-CoA;
3. β-хидроксиацил-CoA се окислява от NAD-зависима дехидрогеназа до β-кетоацил-CoA. Редуцираният NADH 2, окислявайки се в CPE, осигурява синтеза на 3 ATP молекули;
4. Тиолаза с участието на НСоА разцепва ацетил-КоА от β-кетоацил-КоА. В резултат на 4 реакции се образува Acyl-CoA, който е по-къс от предишния Acyl-CoA с 2 въглерода. Образуваният ацетил-КоА, окислен в TCA цикъла, осигурява синтеза на 12 ATP молекули в CPE.
След това Acyl-CoA отново влиза в реакции на β-окисление. Циклите продължават, докато Acyl-CoA се превърне в ацетил-CoA с 2 C атома (ако FA има четен брой C атоми) или Butyryl-CoA с 3 C атома (ако FA има нечетен брой C атоми).
Енергиен баланс на окисление на наситени мастни киселини с четен брой въглеродни атоми
Когато FA се активира, се изразходват 2 макроергични връзки на АТФ.
По време на окислението на наситена FA с четен брой С атоми се образуват само FADH 2, NADH 2 и ацетил-КоА.
По време на 1 цикъл на β-окисление се образуват 1 FADH 2 , 1 NADH 2 и 1 Acetyl-CoA, които при окисление произвеждат 2 + 3 + 12 = 17 ATP.
Брой цикли по време на β-окисление на FA = брой С атоми в (FA/2)-1. По време на β-окисление палмитиновата киселина претърпява (16/2)-1 = 7 цикъла. За 7 цикъла се образува 17*7=119 АТФ.
Последният цикъл на β-окисление е придружен от образуването на допълнителен ацетил-КоА, който при окисление произвежда 12 ATP.
Така при окисляването на палмитинова киселина се получава: -2+119+12=129 ATP.
Обобщено уравнение за β-окисление, палмитоил-CoA:
C 15 H 31 CO-CoA + 7 FAD + 7 NAD + + 7 HSKoA → 8 CH 3 -CO-KoA + 7 FADH 2 + 7 NADH 2
Енергиен баланс на окисление на наситени мастни киселини с нечетен брой въглеродни атоми
β-окислението на наситена FA с нечетен брой С атоми в началото протича по същия начин, както при четен брой. 2 макроергични връзки на АТФ се изразходват за активиране.
FA със 17 С атоми претърпява β-окисление 17/2-1 = 7 цикъла. В 1 цикъл се образува 2+3+12=17 АТФ от 1 FADN 2, 1 NADH 2 и 1 ацетил-КоА. За 7 цикъла се образува 17*7=119 АТФ.
Последният цикъл на β-окисление е придружен от образуването не на ацетил-КоА, а на пропионил-КоА с 3 С атома.
Пропионил-CoA се карбоксилира на цената на 1 ATP от пропионил-CoA карбоксилаза, за да образува D-метилмалонил-CoA, който след изомеризация се превръща първо в L-метилмалонил-CoA и след това в сукцинил-CoA. Сукцинил-КоА е включен в цикъла на ТСА и при окисляване произвежда PCA и 6 ATP. PIKE може да влезе в глюконеогенезата за синтез на глюкоза. Дефицитът на витамин В12 води до натрупване на метилмалонил в кръвта и екскреция в урината. При окислението на ФК се образува: -2+119-1+6=122 АТФ.
Общото уравнение за β-окисление на ФК със 17 С атоми:
C 16 H 33 CO-CoA + 7 FAD + 7 NAD + + 7 HSKoA → 7 CH 3 -CO-KoA + 1 C 2 H 5 -CO-KoA + 7 FADH 2 + 7 NADH 2
Енергиен баланс на окисление на ненаситени мастни киселини с четен брой въглеродни атоми
Около половината от мастните киселини в човешкото тяло са ненаситени. β-окислението на тези киселини протича по обичайния начин, докато двойната връзка е между С атоми 3 и 4. След това ензимът еноил-КоА изомераза премества двойната връзка от позиция 3-4 в позиция 2-3 и променя цис конформацията на двойната връзка към транс, която е необходима за β-окисление. В този цикъл на β-окисление, тъй като двойната връзка вече присъства в FA, първата реакция на дехидрогениране не настъпва и FADH 2 не се образува. Освен това циклите на β-окисление продължават, не се различават от обичайния път.
Енергийният баланс се изчислява по същия начин, както при наситени FA с четен брой С атоми, само за всяка двойна връзка липсват 1 FADN 2 и съответно 2 ATP.
Общото уравнение за β-окисление на палмитолейл-CoA е:
C 15 H 29 CO-CoA + 6 FAD + 7 NAD + + 7 HSKoA → 8 CH 3 -CO-KoA + 6 FADH 2 + 7 NADH 2
Енергиен баланс на β-окисление на палмитолеиновата киселина: -2+8*12+6*2+7*3=127 ATP.
Глад, физическа активност → глюкагон, адреналин → TG липолиза в адипоцитите → FA в кръвта → β-оксидация при аеробни условия в мускулите, черния дроб → 1) ATP; 2) ATP, NADH 2, Acetyl-CoA, (FA) → ↓ гликолиза → спестявания на глюкоза, необходими за нервната тъкан, червените кръвни клетки и др.
Храна → инсулин → гликолиза → Ацетил-CoA → синтез на малонил-CoA и FA
Синтез на malonyl-CoA → malonyl-CoA → ↓ карнитин ацилтрансфераза I в черния дроб → ↓ транспорт на FAs в митохондриалния матрикс → ↓ FAs в матрицата → ↓ β-окисление на FAs
Биосинтез на IVFA. Структура на палмитат синтазния комплекс. Химия и регулиране на процеса.
Синтез на палмитинова киселина
Образуване на малонил-КоА
Първата реакция в синтеза на ФК е превръщането на ацетил-КоА в малонил-КоА. Тази регулаторна реакция в синтеза на FA се катализира от ацетил-СоА карбоксилаза.
Ацетил-КоА карбоксилазата се състои от няколко субединици, съдържащи биотин.
Реакцията протича на 2 етапа:
1) CO 2 + биотин + ATP → биотин-COOH + ADP + Fn
2) ацетил-КоА + биотин-СООН → малонил-КоА + биотин
Ацетил-КоА карбоксилазата се регулира по няколко начина:
3) Асоцииране/дисоциация на комплекси от ензимни субединици. В своята неактивна форма ацетил-КоА карбоксилазата е комплекс, състоящ се от 4 субединици. Цитратът стимулира обединяването на комплексите, в резултат на което се повишава ензимната активност. Palmitoyl-CoA причинява дисоциация на комплексите и намаляване на ензимната активност;
2) Фосфорилиране/дефосфорилиране на ацетил-КоА карбоксилаза. Глюкагонът или адреналинът чрез аденилатциклазната система стимулира фосфорилирането на субединиците на ацетил-КоА карбоксилазата, което води до нейното инактивиране. Инсулинът активира фосфопротеин фосфатазата, ацетил-КоА карбоксилазата се дефосфорилира. След това под въздействието на цитрата настъпва полимеризация на протомерите на ензима и той става активен;
3) Продължителната консумация на храни, богати на въглехидрати и бедни на липиди, води до повишаване на секрецията на инсулин, който индуцира синтеза на ацетил-КоА карбоксилаза, палмитат синтаза, цитрат лиаза, изоцитрат дехидрогеназа и ускорява синтеза на FA и TG. Гладуването или диетата, богата на мазнини, води до намаляване на синтеза на ензими и съответно на FA и TG.
Образуване на палмитинова киселина
След образуването на малонил-КоА, синтезът на палмитинова киселина продължава в мултиензимния комплекс - синтаза на мастни киселини (палмитоил синтетаза) .
Палмитоил синтазата е димер, състоящ се от две идентични полипептидни вериги. Всяка верига има 7 активни места и ацил трансферен протеин (ACP). Всяка верига има 2 SH групи: едната SH група принадлежи на цистеина, другата принадлежи на остатъка на фосфопантеиновата киселина. Цистеиновата SH група на един мономер е разположена до 4-фосфопантетеинатната SH група на другия протомер. Така протомерите на ензима са подредени „глава до опашка“. Въпреки че всеки мономер съдържа всички каталитични места, комплекс от 2 протомера е функционално активен. Следователно, 2 LC всъщност се синтезират едновременно.
Този комплекс последователно разширява FA радикала с 2 С атома, чийто донор е малонил-КоА.
Реакции на синтез на палмитинова киселина
1) Прехвърляне на ацетил от CoA към SH групата на цистеин от ацетилтрансацилазния център;
2) Прехвърляне на малонил от CoA към SH групата на ACP от малонил трансацилазния център;
3) В центъра на кетоацил синтазата ацетиловата група кондензира с малонилната група, за да образува кетоацил и да освободи CO 2 .
4) Кетоацилът се редуцира от кетоацил редуктазата до хидроксиацил;
5) Оксиацилът се дехидратира от хидратаза в еноил;
6) Еноил се редуцира от еноил редуктаза до ацил.
В резултат на първия цикъл от реакции се образува ацил с 4 С атома (бутирил). След това бутирилът се прехвърля от позиция 2 в позиция 1 (където ацетилът се намира в началото на първия цикъл от реакции). След това бутирилът претърпява същите трансформации и се удължава с 2 С атома (от малонил-КоА).
Подобни цикли на реакции се повтарят, докато се образува радикал на палмитинова киселина, който под действието на тиоестеразния център се отделя хидролитично от ензимния комплекс, превръщайки се в свободна палмитинова киселина.
Общото уравнение за синтеза на палмитинова киселина от ацетил-КоА и малонил-КоА е както следва:
CH 3 -CO-SKoA + 7 HOOC-CH 2 -CO-SKoA + 14 NADPH 2 → C 15 H 31 COOH + 7 CO 2 + 6
H 2 O + 8 HSKoA + 14 NADP +
Синтез на ФК от палмитинова и други ФК
Удължаване на FAs в елонгазни реакции
Удължаването на мастната киселина се нарича удължаване. FA могат да бъдат синтезирани в резултат на удължаване на палмитинова киселина и други по-дълги FA в ER. Има елонгази за всяка дължина на LC. Последователността на реакциите е подобна на синтеза на палмитинова киселина, но в този случай синтезът се осъществява не с ACP, а с CoA. Основният продукт на удължаване в черния дроб е стеаринова киселина. В нервните тъкани се образуват дълговерижни FA (C = 20-24), които са необходими за синтеза на сфинголипиди.
Синтез на ненаситени мастни киселини в десатуразни реакции
Включването на двойни връзки в FA радикали се нарича десатурация. Десатурацията на FA се случва в ER при монооксигеназни реакции, катализирани от десатурази.
Стеароил-КоА десатураза– интегрален ензим, съдържа нехемово желязо. Катализира образуването на 1 двойна връзка между 9 и 10 въглеродни атома в FA. Стеароил-КоА десатуразата пренася електрони от цитохром b 5 към 1 кислороден атом, с участието на протони този кислород образува вода. Вторият кислороден атом е включен в стеариновата киселина, за да образува нейния хидроксиацил, който се дехидрогенира до олеинова киселина.
FA десатуразите, присъстващи в човешкото тяло, не могат да образуват двойни връзки в FA дистално от деветия въглероден атом, следователно FA от семействата ω-3 и ω-6 не се синтезират в тялото, те са от съществено значение и трябва да се доставят с храната, тъй като те изпълнява важни регулаторни функции. Основните ФК, образувани в човешкия организъм в резултат на десатурация, са палмитолеинова и олеинова.
Синтез на α-хидрокси ФК
Синтезът на други мастни киселини, α-хидрокси киселини, също се случва в нервната тъкан. Оксидазите със смесена функция хидроксилират C22 и C24 киселини, за да образуват церебронова киселина, открита само в мозъчните липиди.
Въглехидратите съставляват основната част от човешката диета и осигуряват значителна част от енергийните нужди на тялото. При балансирана диета дневното количество въглехидрати е средно 4 пъти по-високо от количеството протеини и мазнини.
Ролята на въглехидратите в храненето:
1. Въглехидратите правят енергийна функция.При окисляване на 1 g въглехидрати се освобождават 4,1 kcal енергия. Глюкозата, в която се разгражда по-голямата част от въглехидратите, е основният енергиен субстрат в тялото.
2. Мускулна дейностпридружен от значителна консумация на глюкоза. При физическа работа първо се изразходват въглехидратите и едва при изчерпване на запасите им (гликоген) се включват в обмяната мазнините.
3. Въглехидратите са от съществено значение за нормалната функция Централна нервна система,чиито клетки са много чувствителни към липсата на глюкоза в кръвта.
4. Въглехидратите правят структурна функция.Простите въглехидрати служат като източник на образуване на гликопротеини, които формират основата на съединителната тъкан.
5. Въглехидратите участват в метаболизма на протеини и мазнини.Мазнините могат да се образуват от въглехидрати.
6. Въглехидратите от растителен произход (целулоза, пектинови вещества) стимулират чревната подвижност и насърчават елиминирането на токсичните продукти, които се натрупват в него.
Източницивъглехидратите служат предимно растителни продукти,особено продукти от брашно, зърнени храни, сладкиши. В повечето храни въглехидратите са представени под формата на нишесте и в по-малка степен под формата на дизахариди (мляко, захарно цвекло, плодове и плодове). За по-доброто усвояване на въглехидратите е необходимо повечето от тях да постъпват в организма под формата на нишесте.
Нишестето постепенно се разгражда в стомашно-чревния тракт до глюкоза, която навлиза в кръвта на малки порции, което подобрява нейното използване и поддържа постоянно ниво на кръвната захар. Когато се приемат големи количества захар наведнъж, концентрацията на глюкоза в кръвта рязко се повишава и тя започва да се отделя с урината. Най-благоприятните условия се считат, когато 64% от въглехидратите се консумират под формата на нишесте и 36% под формата на захари.
Разходна нормавъглехидрати зависи от интензивността на работа. При физическа работа въглехидратите са необходими в по-големи количества. Средно на 1 кг телесно тегло се изисква 4-6-8 г въглехидрати на ден, т.е. приблизително 4 пъти повече от протеините и мазнините.
Прекомерен прием на въглехидратиможе да доведе до затлъстяване и прекомерно претоварване на стомашно-чревния тракт, т.к растителните храни, богати на въглехидрати, обикновено са по-обемисти, предизвикват усещане за тежест и влошават общата смилаемост на храната.
Липсата на въглехидратив храната също е нежелателно поради риска от развитие на хипогликемични състояния. Дефицитът на въглехидрати, като правило, е придружен от обща слабост, сънливост, намалена памет, умствена и физическа работоспособност, главоболие, намалена смилаемост на протеини, витамини, ацидоза и др. В тази връзка количеството въглехидрати в дневната диета не трябва да е по-малко от 300 g
Тясно свързани с групата на въглехидратите са веществата, намиращи се в повечето растителни храни, които са трудно усвоими от човешкия организъм – пектинови вещества (несмилаеми въглехидрати) и фибри.
Пектинови вещества сарастителни желиращи вещества с висока сорбционна (абсорбираща) способност. Имат благоприятен ефект при лечението на заболявания на храносмилателната система, изгаряния и язви, а също така имат способността да неутрализират някои токсични вещества (особено активни са при отстраняването на соли на тежки метали, като оловни съединения, от тялото).
Има много пектинови вещества в портокали, ябълки, касис и други плодове и плодове.
Целулоза(други имена - груби растителни, или несмилаеми, или хранителни, или диетични фибри) е полизахарид, който е част от масивните клетъчни стени на растителни храни. Има влакнеста, доста груба структура.
Общи източници на диетични фибри са трици, хляб и зърнени храни (особено елда и овесени ядки). Големи количества се намират в много зеленчуци, плодове, листа и стъбла на растения; има особено много в обвивките на зърната и в корите на плодовете. При консервиране на зеленчуци и плодове диетичните фибри се запазват напълно (с изключение на сокове без пулп).
Без да имат високо калорично съдържание, повечето зеленчуци и плодове обаче, поради високото съдържание на несмилаеми въглехидрати, допринасят за бързо и сравнително устойчиво усещане за ситост: тъй като диетичните фибри имат способността да абсорбират много течности, те набъбват в стомаха, запълват част от обема му - и в резултат насищането настъпва по-бързо. Самите фибри не пренасят нито една калория в тялото.
Стойността на фибрите се крие във факта, че като доста обемен компонент на ежедневното хранене, те не се усвояват от човешкото тяло. Наличието на голямо количество фибри до известна степен намалява общата смилаемост на храната. Пълната му липса обаче има пагубен ефект върху функционирането на стомашно-чревния тракт.
Фибрите предизвикват правилна перисталтика (движение на стените) на червата и по този начин насърчават движението на храната през храносмилателния канал и отстраняването на несмлени хранителни вещества от тялото.
Необходимото количество фибри в храната се осигурява от правилното съчетаване на животински и растителни продукти в ежедневната диета.
След разграждането фибрите, както и другите полизахариди, се превръщат в захари. В човешкия храносмилателен тракт обаче няма ензими, които да извършат такова разграждане. Само малка част от него може да се усвои под въздействието на микроорганизми в червата, но основната част се отстранява от тялото без промени. Благодарение на тази външна безполезност фибрите и пектините се наричат баластни вещества.
Баластните вещества също изпълняват важна функция в процеса на храносмилане: фибрите се ферментират от чревни бактерии и буквално помагат за смилането на храната; като дразнят нервните окончания на чревните стени, те засилват перисталтиката. Ако храната е бедна на баластни вещества, чревната подвижност се нарушава, следователно, за да се избегнат тези нарушения, се препоръчва да се използват груби храни, богати на фибри.
В допълнение, диетичните фибри имат способността да стимулират метаболизма, тъй като фибрите предотвратяват усвояването на токсините, които идват с храната или се образуват по време на нейната обработка, и служат като вид бъркалка: движейки се по храносмилателния тракт, те вземат със себе си всичко, което е залепнал за стените и го отстранете от тялото.
Друго предимство на диетичните фибри е, че имат способността да намаляват нивото на ендогенния холестерол (това е холестерол, който не постъпва в нас с храната, а се произвежда от самия орган в черния дроб от жлъчни киселини, които влизат в черния дроб от червата ).
Хемицелулоза:подобно на фибрите или целулозата, той е част от клетъчните стени на зърнените продукти и малки количества се намират в пулпата на плодовете и зеленчуците. Способен е да задържа вода и да свързва металите.
Окисляване на мастни киселини (бета окисление). Роля Х.С. – Ко в този процес. Енергия на пълното окисление на стеоровата киселина до CO 2 ° С з 2 О . Изчислете броя на ATP молекулите, образувани по време на окислението.
Активирането на FA се случва в цитоплазмата, а бета-окислението се случва в митохондриите.
Acyl-CoA не може да премине през митохондриалната мембрана. Следователно съществува специален механизъм за транспортиране на ФК от цитоплазмата в митохондриите с участието на веществото "карнитин". Във вътрешната мембрана на митохондриите има специален транспортен протеин, който осигурява преноса. Благодарение на това ацилкарнитинът лесно прониква през митохондриалната мембрана.
Цитоплазмените и митохондриалните карнитин ацилтрансферази са различни по структура и също така се различават една от друга по кинетични характеристики. Vmax на цитоплазмената ацилкарнитин трансфераза е по-нисък от Vmax на митохондриалния ензим и също по-нисък от Vmax на β-окислителните ензими. Следователно цитоплазмената ацилкарнитин трансфераза е ключов ензим при разграждането на мастни киселини.
Ако мастна киселина навлезе в митохондриите, тя задължително ще претърпи катаболизъм до ацетил-КоА.
Най-компактното „гориво“, което задоволява енергийните нужди на организма, са мастните киселини, което се определя от характеристиките на тяхната химична структура. На 1 мол пълното окисление на мастните киселини освобождава няколко пъти повече използваема химическа енергия, отколкото окисляването на въглехидратите; например окислението на 1 mol палмитинова киселина произвежда 130 mol ATP, докато окислението на 1 mol глюкоза произвежда 38 mol ATP. На единица тегло енергийният добив също се различава повече от два пъти (9 kcal на 1 g мазнини срещу 4 kcal на 1 g въглехидрати или протеини). Този висок енергиен добив се основава на същата причина, която прави бензина, петрола и другите петролни продукти толкова ефективни горива за генериране на топлинна и механична енергия, а именно високата степен на редукция на въглерода в дългите алкилни вериги. Основната част от молекулата на мастната киселина се състои от повтарящи се единици (CH2)n, т.е. структура, максимално обогатена с водород. Както видяхме от предишната презентация, енергията, съхранявана по време на биологични окислителни процеси, се образува главно във връзка с контролирания трансфер на електрони от водородните атоми на дихателната верига, съчетан с фосфорилирането на ADP до ATP. Тъй като мастните киселини са съставени предимно от въглерод и водород и следователно съдържат значително по-малко кислородни атоми от въглехидратите, окисляването на мастните киселини е придружено от абсорбцията на пропорционално повече кислород и следователно образуването на повече АТФ по време на окислителното фосфорилиране.
Установено е, че окислението на мастните киселини протича най-интензивно в черния дроб, бъбреците, скелетните и сърдечните мускули и в мастната тъкан. В мозъчната тъкан скоростта на окисление на мастните киселини е много ниска, т.к Основният източник на енергия в мозъчната тъкан е глюкозата.
β-окислението е специфичен път на катаболизъм на мастна киселина, при който 2 въглеродни атома се отделят последователно от карбоксилния край на мастна киселина под формата на ацетил-КоА. Метаболитният път - β-окисление - е наречен така, защото реакциите на окисляване на мастни киселини протичат при β-въглеродния атом. Реакциите на β-окисление и последващото окисление на ацетил-КоА в цикъла на ТСА служат като един от основните източници на енергия за синтеза на АТФ чрез механизма на окислително фосфорилиране. β-окислението на мастните киселини се извършва само при аеробни условия.
Активиране на мастни киселини
Преди да влязат в различни реакции, мастните киселини трябва да бъдат активирани, т.е. са свързани чрез макроергична връзка с коензим А:
RCOOH + HSKoA + ATP → RCO ~ CoA + AMP + PPi.
Реакцията се катализира от ензима ацил-КоА синтетаза. Освободеният по време на реакцията пирофосфат се хидролизира от ензима пирофосфатаза: H 4 P 2 O 7 + H 2 O → 2 H 3 PO 4.
Освобождаването на енергия по време на хидролизата на високоенергийната връзка на пирофосфата измества равновесието на реакцията надясно и осигурява пълнотата на реакцията на активиране.
Ацил-КоА синтетазасе намират както в цитозола, така и в митохондриалния матрикс. Тези ензими се различават по своята специфичност за мастни киселини с различна дължина на въглеводородна верига. Мастни киселини с къса и средна дължина на веригата (от 4 до 12 въглеродни атома) могат да проникнат в митохондриалната матрица чрез дифузия. Активирането на тези мастни киселини става в митохондриалната матрица. Дълговерижните мастни киселини, които преобладават в човешкото тяло (12 до 20 въглеродни атома), се активират от ацил-КоА синтетази, разположени върху външната мембрана на митохондриите.
Разграждането на активираните мастни киселини става в съответствие с хипотезата b - окисление F. Knoop, предложен през 1904 г. b - окислението се случва вътре в митохондриите
β- Окисление на мастни киселини- специфичен път на катаболизъм на мастни киселини, протичащ в митохондриалната матрица само при аеробни условия и завършващ с образуването на ацетил-КоА. Водородът от реакциите на β-окисление влиза в CPE, а ацетил-CoA се окислява в цитратния цикъл, който също доставя водород към CPE. Следователно β-окислението на мастни киселини е най-важният метаболитен път, осигуряващ синтеза на АТФ в дихателната верига.
β-Окислението започва с дехидрогениране на ацил-CoA от FAD-зависима ацил-CoA дехидрогеназа, образувайки двойна връзка между α и β въглеродните атоми в реакционния продукт, еноил-CoA. Коензимът FADH 2, възстановен в тази реакция, прехвърля водородни атоми в CPE към коензим Q. В резултат на това се синтезират 2 молекули АТФ (фиг. 8-27). В следващата реакция на р-окисление се добавя водна молекула на мястото на двойната връзка, така че ОН групата да се намира при β-въглеродния атом на ацила, образувайки β-хидроксиацил-CoA. След това β-хидроксиацил-КоА се окислява от NAD+-зависима дехидрогеназа. Редуцираният NADH, окислен в CPE, осигурява енергия за синтеза на 3 ATP молекули. Полученият β-кетоацил-КоА претърпява тиолитично разцепване от ензима тиолаза, тъй като на мястото на разцепване на връзката С-С се добавя молекула коензим А чрез серен атом.В резултат на тази последователност от 4 реакции, a двувъглеродният остатък, ацетил-КоА, се отделя от ацил-КоА. Мастна киселина, съкратена с 2 въглеродни атома, отново претърпява реакциите на дехидрогениране, хидратиране, дехидрогениране и елиминиране на ацетил-КоА. Тази последователност от реакции обикновено се нарича "β-оксидационен цикъл", което означава, че същите реакции се повтарят с радикала на мастната киселина, докато цялата киселина се превърне в ацетилови остатъци.
β - Окисляване на мастни киселини.
Процесът на b-окисление е цикличен.За всеки оборот на цикъла 2 въглеродни атома се отделят от мастната киселина под формата на ацетилов остатък.
След това ацил-КоА, съкратен с 2 въглеродни атома, отново се подлага на окисление (влиза в нов цикъл на b-окислителни реакции). Полученият ацетил-КоА може допълнително да влезе в цикъла на трикарбоксилната киселина.Трябва да можете да изчислите енергийния добив от разграждането на мастните киселини. Представената формула е вярна за всяка наситена мастна киселина, съдържаща n въглеродни атома.Разграждането на ненаситените мастни киселини произвежда по-малко АТФ. Всяка двойна връзка в мастна киселина означава загуба на 2 ATP молекули. b-окислението протича най-интензивно в мускулната тъкан, бъбреците и черния дроб.В резултат на b-окисление на FA се образува ацетил-КоА. Скоростта на окисление се определя от скоростта на процесите на липолиза. Ускоряването на липолизата е характерно за състояние на въглехидратно гладуване и интензивна мускулна работа. Ускоряване на b-окислението се наблюдава в много тъкани, включително черния дроб. Черният дроб произвежда повече ацетил-КоА, отколкото се нуждае. Черният дроб е „алтруистичен орган“ и следователно черният дроб изпраща глюкоза към други тъкани.
Черният дроб се стреми да изпрати собствения си ацетил-КоА към други тъкани, но не може, тъй като клетъчните мембрани са непропускливи за ацетил-КоА. Следователно в черния дроб от ацетил-КоА се синтезират специални вещества, наречени „кетонни тела“. Кетоновите тела са специална транспортна форма на ацетил-КоА.
Молекулата на мастната киселина се разгражда до митохондрии чрез постепенно елиминиране на двувъглеродни фрагменти под формата на ацетил коензим А (ацетил-КоА).
C17H35COOH + 26 O2 = 18 CO2 + 18 H2O.
Когато стеариновата киселина се окислява, клетката ще получи 146 молекули АТФ.