Zsírsav oxidációs termékek. A zsírsavak oxidációjának sajátos útja van. Acetil-CoA és ATP képződése palmitoil-CoA oxidáció példájával
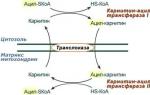
A zsírsavak energiájának ATP-kötések energiájává történő átalakításához a zsírsavak CO 2 -dá és vízzé történő oxidációjának metabolikus útvonala van, amely szorosan összefügg a trikarbonsavciklussal és a légzési lánccal. Ezt az utat hívják β-oxidáció, mert a zsírsav 3. szénatomja (β-helyzet) karboxilcsoporttá oxidálódik, és ezzel egyidejűleg az eredeti zsírsav C 1 és C 2 acetilcsoportja is lehasad a savról.
A β-oxidáció elemi diagramja
β-oxidációs reakciók mennek végbe mitokondriumok a legtöbb sejt a szervezetben (az idegsejtek kivételével). Azokat a zsírsavakat, amelyek a vérből kerülnek a citoszolba, vagy saját intracelluláris TAG-jaik lipolízise során jelennek meg, oxidációra használják fel. A palmitinsav oxidációjának általános egyenlete a következő:
Palmitoil-SCoA + 7FAD + 7NAD + + 7H 2 O + 7HS-KoA → 8 Acetil-SCoA + 7FADH 2 + 7NADH
A zsírsav-oxidáció szakaszai
1. Mielőtt behatol a mitokondriális mátrixba és oxidálódik, a zsírsav must aktiválja a citoszolban. Ezt úgy érik el, hogy koenzim-A-t adnak hozzá, hogy acil-SCoA-t képezzenek. Az acil-SCoA egy nagy energiájú vegyület. A reakció visszafordíthatatlansága a difoszfát két foszforsavmolekulává történő hidrolízisével érhető el.
Az acil-SCoA szintetázok az endoplazmatikus retikulumban, a mitokondriumok külső membránján és azon belül találhatók. A különböző zsírsavakra specifikus szintetázok széles skálája létezik.
Zsírsav aktiválási reakció
2. Az Acyl-SCoA nem képes átjutni a mitokondriális membránon, így egy vitaminszerű anyaggal, karnitinnel kombinálva van mód a szállítására. A mitokondriumok külső membránján egy enzim található karnitin-aciltranszferáz I.

A zsírsavak karnitinfüggő transzportja a mitokondriumba
A karnitint a májban és a vesében szintetizálják, majd más szervekbe szállítják. Ban ben méhen belüli időszakban és in korai évek Az életben a karnitin jelentősége rendkívül nagy a szervezet számára. Az idegrendszer energiaellátása gyerekeknek A test és különösen az agy működését két párhuzamos folyamat végzi: a zsírsavak karnitinfüggő oxidációja és a glükóz aerob oxidációja. A karnitin szükséges az agy és a gerincvelő növekedéséhez, az idegrendszer minden mozgásért és izomkölcsönhatásért felelős részének kölcsönhatásához. Vannak tanulmányok, amelyek összefüggésbe hozzák a karnitinhiányt agyi bénulásés jelenség" halál a bölcsőben".
A kisgyermekek, a koraszülöttek és az alacsony születési súlyú gyermekek különösen érzékenyek a karnitinhiányra. Endogén készleteik gyorsan kimerülnek különféle stresszhelyzetekben (fertőző betegségek, gyomor-bélrendszeri betegségek, táplálkozási zavarok). A karnitin bioszintézise élesen korlátozott az alacsony izomtömeg miatt, és a szokásos élelmiszerekből történő bevitel nem képes megfelelő szintet fenntartani a vérben és a szövetekben.
3. A karnitinhez való kötődés után a zsírsavat a transzlokáz a membránon keresztül szállítja. Itt, a membrán belső oldalán a karnitin-aciltranszferáz II enzim ismét acil-SCoA-t képez, amely belép a β-oxidációs útvonalba.
4. Maga a folyamat β-oxidáció 4 ciklikusan ismétlődő reakcióból áll. Sorban történnek oxidáció(acil-SCoA dehidrogenáz), hidratáció(enoil-SCoA hidratáz) és újra oxidáció 3. szénatom (hidroxiacil-SCoA dehidrogenáz). Az utolsó transzferáz reakcióban az acetil-SCoA lehasad a zsírsavról. A maradék (két szénatommal rövidített) zsírsavhoz HS-CoA-t adnak, és visszatér az első reakcióhoz. Ezt addig ismételjük, amíg az utolsó ciklus két acetil-SCoA-t nem termel.

A zsírsavak β-oxidációjának reakciósorozata
A β-oxidáció energiamérlegének kiszámítása
Korábban az oxidációs hatásfok számításakor a NADH P/O együtthatóját 3,0-nak vettük, a FADH 2 esetében pedig 2,0-nak.
A modern adatok szerint a P/O együttható értéke NADH esetén 2,5, FADH 2 esetén 1,5.
A zsírsavak β-oxidációja során képződött ATP mennyiségének kiszámításakor figyelembe kell venni:
- a képződött acetil-SCoA mennyiségét a zsírsavban lévő szénatomok számának szokásos 2-vel való osztása határozza meg.
- szám β-oxidációs ciklusok. A β-oxidációs ciklusok száma könnyen meghatározható a zsírsav mint két szénatomos egységek láncolata alapján. Az egységek közötti szünetek száma megfelel a β-oxidációs ciklusok számának. Ugyanez az érték kiszámítható az (n/2 -1) képlettel, ahol n a szénatomok száma a savban.
- a kettős kötések száma egy zsírsavban. Az első β-oxidációs reakcióban kettős kötés jön létre a FAD részvételével. Ha egy kettős kötés már jelen van a zsírsavban, akkor nincs szükség erre a reakcióra, és nem képződik FADN 2. Az elveszett FADN 2 száma megfelel a kettős kötések számának. A ciklus többi reakciója változtatás nélkül megy végbe.
- az aktiválásra fordított ATP energia mennyisége (mindig két nagy energiájú kötésnek felel meg).
Példa. A palmitinsav oxidációja
- mivel 16 szénatom van, a β-oxidáció hoz létre 8 acetil-SCoA molekula. Ez utóbbi belép a TCA-ciklusba, a ciklus egy körében oxidálva 3 molekula NADH (7,5 ATP), 1 molekula FADH 2 (1,5 ATP) és 1 molekula GTP képződik, ami 10 molekulának felel meg. az ATP-ből. Tehát 8 molekula acetil-SCoA biztosítja a 8 × 10 = képződést 80 ATP molekulák.
- palmitinsavhoz a β-oxidációs ciklusok száma 7. Minden ciklusban 1 molekula FADH 2 (1,5 ATP) és 1 molekula NADH (2,5 ATP) termelődik. A légzőláncba belépve összesen 4 ATP molekulát „adnak”. Így 7 ciklus alatt 7 × 4 = 28 ATP molekula keletkezik.
- kettős kötések a palmitinsavban Nem.
- 1 molekula ATP-t használnak fel a zsírsav aktiválására, amely azonban AMP-vé hidrolizálódik, azaz elhasználódik. 2 makroerg kapcsolat vagy két ATP.
Így összegezve azt kapjuk 80+28-2 =106 Az ATP-molekulák a palmitinsav oxidációja során keletkeznek.
A zsírsavak biológiai oxidációja összevethető a szénhidrogének elégetésével: mindkét esetben a legnagyobb szabadenergia-hozam figyelhető meg. A zsírsavak szénhidrogén részének biológiai b-oxidációja során két szénatomos aktivált komponensek képződnek, amelyek a TCA körfolyamatban tovább oxidálódnak, és nagyszámú redukáló ekvivalens, amelyek ATP szintéziséhez vezetnek a légzési láncban. . A legtöbb aerob sejt képes a zsírsavak szén-dioxiddá és vízzé történő teljes oxidációjára.
A zsírsavak forrása exogén vagy endogén lipidek. Ez utóbbiakat leggyakrabban triacilgliceridek képviselik, amelyek tartalék energia- és szénforrásként rakódnak le a sejtekben. Emellett a sejtek poláris membránlipideket is használnak, amelyek metabolikus megújulása folyamatosan történik. A lipideket specifikus enzimek (lipázok) glicerinné és szabad zsírsavakra bontják.
a zsírsavak b-oxidációja. A zsírsav-oxidációnak ez az alapvető folyamata a mitokondriumokban lévő eukariótákban megy végbe. A zsírsavak mitokondriális membránokon keresztül történő szállítását elősegíti karnitin(g-trimetilamino-b-hidroxi-butirát), amely speciális módon köt meg egy zsírsav molekulát, melynek eredményeként a pozitív (a nitrogénatomon) és a negatív (a karboxilcsoport oxigénatomján) töltések közelebb kerülnek egymáshoz. együtt és semlegesítik egymást.
A mitokondriális mátrixba történő transzport után a zsírsavakat CoA aktiválja egy ATP-függő reakcióban, amelyet acetát-tiokináz katalizál (9.1. ábra). Az acil-CoA származékot ezután acil-dehidrogenáz részvételével oxidálják. A sejtben számos különböző acil-dehidrogenáz található, amelyek specifikusak a különböző szénhidrogénlánchosszúságú zsírsavak CoA-származékaira. Mindezek az enzimek a FAD-ot használják protetikus csoportként. A reakció során az acil-dehidrogenáz részeként képződő FADH 2-t egy másik flavoprotein oxidálja, amely a mitokondriális membrán részeként elektronokat ad át a légzőláncba.
Az oxidációs terméket, az enoil-CoA-t enoil-hidratázzal hidratálják b-hidroxi-acil-CoA-vá (9.1. ábra). Vannak enoil-CoA hidratázok, amelyek specifikusak a zsírsavak enoil-CoA származékainak cisz- és transz-formáira. Ebben az esetben a transz-enoil-CoA sztereospecifikusan L-b-hidroxi-acil-CoA-vá, a cisz-izomerek pedig a -b-hidroxi-acil-CoA-észterek D-sztereoizomerjévé hidratálódnak.
A zsírsavak b-oxidációjának reakcióinak utolsó lépése az L-b-hidroxiacil-CoA dehidrogénezése (9.1. ábra). A molekula b-szénatomja oxidáción megy keresztül, ezért az egész folyamatot b-oxidációnak nevezik. A reakciót a b-hidroxiacil-CoA dehidrogenáz katalizálja, amely csak a b-hidroxi-acil-CoA L-formáira specifikus. Ez az enzim a NAD-ot használja koenzimként. A b-hidroxi-acil-CoA D-izomereinek dehidrogénezését egy további L-b-hidroxi-acil-CoA-vá (enzim-b-hidroxi-acil-CoA epimeráz) végzett izomerizáció után hajtjuk végre. A reakció ezen szakaszának terméke a b-ketoacil-CoA, amelyet a tioláz könnyen 2 származékra hasít: acil-CoA, amely 2 szénatommal rövidebb, mint az eredeti aktivált szubsztrát, és egy acetil-CoA kétszén komponens. , a zsírsavláncról lehasadva (9.1. ábra) . Az acil-CoA származék egy további b-oxidációs reakciócikluson megy keresztül, és az acetil-CoA beléphet a trikarbonsav ciklusba további oxidáció céljából.
Így a zsírsavak b-oxidációjának minden ciklusát egy kétszénből álló fragmentum (acetil-CoA) és két pár hidrogénatom leválása kíséri a szubsztrátról, ami 1 molekula NAD + és egy FAD molekula redukálásával jár. A folyamat addig tart, amíg a zsírsavlánc teljesen le nem bomlik. Ha a zsírsav páratlan számú szénatomból állt, akkor a b-oxidáció propionil-CoA képződésével végződik, amely több reakció során szukcinil-CoA-vá alakul, és ebben a formában kerülhet be a TCA ciklusba.
Az állatok, növények és mikroorganizmusok sejtjeit alkotó zsírsavak többsége el nem ágazó szénhidrogénláncokat tartalmaz. Ugyanakkor egyes mikroorganizmusok és növényi viaszok lipidjei olyan zsírsavakat tartalmaznak, amelyek szénhidrogén gyökeinek elágazási pontjai vannak (általában metilcsoportok formájában). Ha kevés az elágazás, és mindegyik páros pozícióban fordul elő (2-es, 4-es szénatomon stb.), akkor a b-oxidációs folyamat a szokásos séma szerint megy végbe, acetil- és propionil-CoA képződésével. Ha a metilcsoportok páratlan szénatomokon helyezkednek el, a b-oxidációs folyamat blokkolva van a hidratációs szakaszban. Ezt figyelembe kell venni a szintetikus mosószerek előállítása során: a környezetben történő gyors és teljes biológiai lebomlásuk érdekében csak az egyenes szénhidrogénláncú változatokat szabad tömegfogyasztásra engedélyezni.
Telítetlen zsírsavak oxidációja. Ezt a folyamatot a b-oxidáció összes törvényének megfelelően hajtják végre. Azonban a legtöbb természetben előforduló telítetlen zsírsav kettős kötést tartalmaz a szénhidrogénlánc egyes helyein úgy, hogy a két szénatomos csoportok egymást követő eltávolítása a karboxilvégről egy acil-CoA származékot eredményez, amelyben a kettős kötés a 3-4. Ezenkívül a természetes zsírsavak kettős kötései cisz konfigurációjúak. A b-hidroxiacil-CoA dehidrogenáz részvételével, a b-hidroxi-acil-CoA L-formáira jellemző dehidrogénezési szakasz végrehajtásához egy további enzimatikus izomerizációs lépésre van szükség, amelynek során a kettős kötés a a CoA-eredetű zsírsavmolekula a 3-4-es pozícióból a 2-3-as pozícióba kerül, és a kettős kötés konfigurációja cisz-ről transz-re változik. Ez a metabolit az enoil-hidratáz szubsztrátjaként szolgál, amely a transz-enoil-CoA-t L-b-hidroxi-acil-CoA-vá alakítja.
Azokban az esetekben, amikor a kettős kötés átvitele és izomerizálása lehetetlen, az ilyen kötést a NADPH részvételével helyreállítják. A zsírsav későbbi lebomlása a szokásos b-oxidációs mechanizmuson keresztül megy végbe.
A zsírsav-oxidáció kisebb útjai. b-oxidáció a fő, de nem az egyetlen útja a zsírsavak lebontásának. Így a növényi sejtekben a 15-18 szénatomos zsírsavak a-oxidációjának folyamatát fedezték fel. Ez az út magában foglalja a zsírsav kezdeti peroxidáz általi támadását hidrogén-peroxid jelenlétében, ami a karboxil-szén eltávolítását eredményezi CO 2 formájában, és az a-helyzetű szén oxidációját aldehidcsoporttá. Ezután az aldehidet dehidrogenáz részvételével magasabb zsírsavvá oxidálják, és a folyamatot megismételjük (9.2. ábra). Ez az út azonban nem tudja biztosítani a teljes oxidációt. Kizárólag zsírsavláncok lerövidítésére használják, és kitérőként is használják, amikor a β-oxidáció blokkolva van a metil oldalcsoportok jelenléte miatt. A folyamat nem igényli a CoA részvételét, és nem kíséri ATP képződése.
Egyes zsírsavak a w-szénatomon is oxidálódhatnak (w-oxidáció). Ebben az esetben a CH 3 csoport monooxigenáz hatására hidroxilezésen megy keresztül, melynek során w-hidroxisav keletkezik, amely azután dikarbonsavvá oxidálódik. A dikarbonsav mindkét végén lerövidíthető b-oxidációs reakciókkal.

Hasonlóképpen a mikroorganizmusok sejtjeiben és egyes állati szövetekben a telített szénhidrogének lebomlása következik be. Az első szakaszban, molekuláris oxigén részvételével, a molekula hidroxilezése alkoholt képez, amely egymás után aldehiddé és karbonsavvá oxidálódik, CoA hozzáadásával aktiválódik, és belép a b-oxidációs útvonalba.
Mint már jeleztük, az állati szervezet az oxidációs folyamat során kinyert energia jelentős részét zsírsavakból nyeri, amelyek a β-szénatomnál oxidációval bomlanak le.
A zsírsavak β-oxidációját először 19004-ben F. Knoop tanulmányozta. Később kiderült, hogy a β-oxidáció csak a mitokondriumokban fordul elő. F. Linen és munkatársai (1954-1958) munkájának köszönhetően sikerült tisztázni a zsírsav-oxidáció főbb enzimatikus folyamatait. A zsírsav-oxidáció ezen útját felfedező tudósok tiszteletére a β-oxidáció folyamatát ún. Knoop-Linen ciklus.
β-oxidáció- a zsírsavkatabolizmus specifikus útja, amelyben 2 szénatom szekvenciálisan elválik a zsírsav karboxilvégétől acetil-CoA formájában. A metabolikus útvonalat - β-oxidációt - azért nevezték így, mert a zsírsav-oxidációs reakciók a β-szénatomon mennek végbe. A β-oxidáció és az acetil-CoA ezt követő oxidációja a TCA-ciklusban (trikarbonsav-ciklus) az oxidatív foszforiláció mechanizmusán keresztül az ATP-szintézis egyik fő energiaforrásaként szolgál. A zsírsavak β-oxidációja csak aerob körülmények között megy végbe.
Minden többlépcsős oxidációs reakciót specifikus enzimek gyorsítanak. A magasabb zsírsavak β-oxidációja egy univerzális biokémiai folyamat, amely minden élő szervezetben előfordul. Emlősöknél ez a folyamat számos szövetben, leginkább a májban, a vesében és a szívben játszódik le. A zsírsavak oxidációja a mitokondriumokban megy végbe. A telítetlen magasabb zsírsavak (olajsav, linolsav, linolén stb.) előzetesen telített savakká redukálódnak.
A zsírsavak behatolását a mitokondriális mátrixba megelőzik azok aktiválás kapcsolat kialakításával koenzim A(HS~CoA), amely nagy energiájú kötést tartalmaz. Ez utóbbi nyilvánvalóan hozzájárul a keletkező vegyület oxidációs reakcióinak simább lefolyásához, amelyet ún acil koenzim A(acil-CoA).
A magasabb zsírsavak CoA-val való kölcsönhatását specifikus ligázok gyorsítják - acil-CoA szintetázok három típus, amelyek a rövid, közepes és hosszú szénhidrogéngyököket tartalmazó savakra specifikusak. Az endoplazmatikus retikulum membránjában és a mitokondriumok külső membránjában lokalizálódnak. Az összes acil-CoA szintetáz multimernek tűnik; Így a máj mikroszómáiból származó enzim molekulatömege 168 kDa, és 6 azonos alegységből áll. A zsírsavak aktiválási reakciója 2 szakaszban megy végbe:
a) először a zsírsav reakcióba lép az ATP-vel, és aciladenilátot képez:
RCOOH + ATP → RCO~AMP + FF
b) ekkor az acil-CoA aktivált formája képződik:
RCO~AMФ + NS~KoA → RCO~SKoA + AMF
A pirofoszfátot (PP) a pirofoszfatáz gyorsan hidrolizálja, aminek következtében az egész reakció visszafordíthatatlan: PP + H 2 O → 2P
Összefoglaló egyenlet:
RCOOH + ATP+ HS~CoA→ RCO~SKoA + AMF + 2P
A rövid és közepes lánchosszúságú (4-12 szénatomos) zsírsavak diffúzió útján behatolhatnak a mitokondriális mátrixba, ahol aktiválódásuk megtörténik. Az emberi szervezetben túlsúlyban lévő (12-20 szénatomos) hosszú szénláncú zsírsavakat a mitokondriumok külső membránján található acil-CoA szintetázok aktiválják.
A belső mitokondriális membrán áthatolhatatlan a citoplazmában képződő hosszú láncú acil-CoA-k számára. Aktivált zsírsavak hordozójaként szolgál karnitin (Bt-vitamin), amely élelmiszerből származik, vagy a lizin és a metionin esszenciális aminosavakból szintetizálódik.
A mitokondriumok külső membránja tartalmaz karnitin-aciltranszferáz I enzim(karnitin palmitoiltranszferáz I), katalizálja az acilkarnitin képződésével járó reakciót:
RCO~SKoA + H 3 C- N + -CH 2 -CH-CH 2 -COOH ↔ H 3 C- N + -CH 2 -CH-CH 2 -COOH + HS~KoA
Acil-CoA karnitin (B t) Acilkarnitin koenzim A
Ez az enzim szabályozó, szabályozza az acilcsoportok bejutását a mitokondriumokba, és ennek következtében a zsírsav-oxidáció sebességét.
A keletkező acilkarnitin a membránközi téren keresztül a belső membrán külső oldalára jut, és a karnitin-acilkarnitin transzlokáz a belső mitokondriális membrán belső felületére szállítja, ahol az enzim karnitin-aciltranszferáz II katalizálja az acil átvitelét az intramitokondriális CoA-ba, vagyis a fordított reakciót (9. ábra).

9. ábra. Zsírsavak átvitele hosszú szénhidrogén gyökökkel a mitokondriális membránokon keresztül
Így az acil-CoA elérhetővé válik a β-oxidációs enzimek számára. A szabad karnitint ugyanaz a transzlokáz juttatja vissza a belső mitokondriális membrán citoszolos oldalára. Ezt követően az acil-CoA bekerül a β-oxidációs reakciókba.
A mitokondriális mátrixban az acil-CoA katabolizmusa (lebomlása) egy ismétlődő szekvencia eredményeként megy végbe. négy reakció.
1) Minden ciklus első reakciója az enzim általi oxidáció acil-CoA dehidrogenáz, melynek koenzimje a FAD. A β és α szénatomok között dehidrogénezés megy végbe, melynek eredményeként kettős kötés képződik a szénláncban, és ennek a reakciónak a terméke az enoil-CoA:
R-CH2-CH2CO~SKoA + FAD → R-CH=CHCO~SKoA + FADN2
Acil-CoA Enoil-CoA
2) A zsírsav-oxidációs ciklus második lépésében az enoil-CoA kettős kötés hidratálódik, ami β-hidroxi-acil-CoA képződését eredményezi. A reakciót egy enzim katalizálja enoil-CoA hidratáz:
R-CH=CHCO-SKoA +H20 → R-CH-CH2CO-SKoA
Enoil-CoA β-hidroxi-acil-CoA
3) A ciklus harmadik szakaszában a β-hidroxi-acil-CoA dehidrogénezésen (második oxidáción) megy keresztül az enzim részvételével β-hidroxiacil-CoA dehidrogenáz, melynek koenzimje a NAD +. Ennek a reakciónak a terméke a β-ketoacil-CoA:
R-CH-CH2CO~SKoA + NAD + → R-CОCH2CO~SKoA + NADH + H +
β-hidroxi-acil-CoA β-ketoacil-CoA
4) A zsírsav-oxidációs ciklus végső reakcióját katalizálja acetil-CoA aciltranszferáz (tioláz). Ebben a szakaszban a β-ketoacil-CoA reagál a szabad CoA-val, és felhasad, és először egy kétszénből álló fragmenst képez, amely a kiindulási zsírsav két terminális szénatomját tartalmazza acetil-CoA formájában, másodszor pedig egy CoA-t. zsírsav-észter, most két szénatommal lerövidült. A hidrolízissel analóg módon ezt a reakciót nevezzük tiolízis:
R-COCH 2 CO~SKoA + HS~KoA → CH 3 CO~SKoA + R 1 CO~SKoA
β-ketoacil-CoA Acetil-CoA Acil-CoA,
által lerövidítve
2 szénatom
A lerövidített acil-CoA ezután a következő oxidációs cikluson megy keresztül, amely egy acil-CoA dehidrogenázzal katalizált reakcióval kezdődik (oxidáció), majd egy hidratációs reakció, egy második oxidációs reakció, egy tioláz reakció, vagyis ez a folyamat sokszor megismétlődik. (10. ábra).
β- A magasabb zsírsavak oxidációja a mitokondriumokban megy végbe. A légzési ciklus enzimei is lokalizálódnak bennük, ami az ADP oxidatív foszforilációjának körülményei között a hidrogénatomok és elektronok oxigénbe történő átviteléhez vezet, ezért a magasabb zsírsavak β-oxidációja energiaforrás az ATP szintéziséhez.

10. ábra. Zsírsav oxidáció
A magasabb zsírsavak β-oxidációjának végterméke a páros számú szénatom van acetil-CoA, A páratlannal- propionil-CoA.
Ha acetil-CoA felhalmozódik a szervezetben, akkor a HS~KoA tartalékai hamar kimerülnének, a magasabb zsírsavak oxidációja pedig leállna. De ez nem történik meg, mivel a CoA gyorsan felszabadul az acetil-CoA-ból. Számos folyamat vezet ehhez: az acetil-CoA a trikarbonsavak és a dikarbonsavak körforgásában vagy az ahhoz nagyon közel álló glioxil ciklusban szerepel, vagy az acetil-CoA-t szterolok és izoprenoid csoportokat tartalmazó vegyületek szintézisére használják fel, stb.
propionil-CoA, amely a páratlan szénatomszámú magasabb zsírsavak β-oxidációjának végterméke, szukcinil-CoA-vá alakul, amely a trikarbonsavak és a dikarbonsavak körforgása során hasznosul.
Az emberi szervezetben található zsírsavak körülbelül fele telítetlen .
Ezeknek a savaknak a β-oxidációja a szokásos módon megy végbe, amíg a kettős kötés a harmadik és negyedik szénatom közé nem kerül. Aztán az enzim enoil-CoA izomeráz a kettős kötést a 3-4 pozícióból a 2-3 pozícióba mozgatja, és a kettős kötés cisz-ét transz konformációvá változtatja, ami a β-oxidációhoz szükséges. Ebben a β-oxidációs ciklusban az első dehidrogénezési reakció nem megy végbe, mivel a zsírsavgyökben már jelen van a kettős kötés. Továbbá a β-oxidációs ciklusok folytatódnak, nem különbözve a szokásostól. A zsírsav-anyagcsere fő útjait a 11. ábra mutatja be.

11. ábra A zsírsav-anyagcsere főbb útvonalai
Nemrég fedezték fel, hogy a β-oxidáció mellett a zsírsav-katabolizmus fő útja, az agyszövet zsírsavak α-oxidációja a szénatomok számával (C 13 -C 18), vagyis a molekula karboxilvégéről az egyszénből álló fragmensek szekvenciális eliminációja.
Ez a fajta oxidáció leggyakrabban növényi szövetekben fordul elő, de előfordulhat egyes állati szövetekben is. Az α-oxidáció ciklikus jellegű, és a ciklus két reakcióból áll.
Az első reakció abból áll, hogy egy zsírsavat hidrogén-peroxiddal a megfelelő aldehiddé és CO 2 -dá oxidálnak egy specifikus vegyület részvételével. peroxidázok:

A reakció eredményeként a szénhidrogénlánc egy szénatommal lerövidül.
A második reakció lényege a keletkező aldehid hidratálása és oxidációja a megfelelő karbonsavvá az ún. aldehid-dehidrogenáz a NAD koenzim oxidált formáját tartalmazza:
Az α-oxidációs ciklus ezután ismét megismétlődik. A β-oxidációhoz képest ez a fajta oxidáció energetikailag kevésbé kedvező.
ω-Zsírsavak oxidációja. Az állatok és egyes mikroorganizmusok májában van egy enzimrendszer, amely biztosítja a zsírsavak ω-oxidációját, vagyis az ω betűvel jelölt terminális CH 3 csoport oxidációját. Először befolyás alatt monooxigenázok A hidroxilezés során ω-hidroxisav keletkezik:

Az ω-hidroxisavat ezután ω-dikarbonsavvá oxidálják a megfelelő vegyület hatására. dehidrogenázok:
Az így kapott ω-dikarbonsav mindkét végén β-oxidációs reakciókkal lerövidül.
Hidrolízis trigliceridek hasnyálmirigy-lipáz hajtja végre. Optimális pH = 8, túlnyomórészt 1-es és 3-as pozícióban hidrolizálja a TG-t, 2 szabad zsírsav és 2-monoacilglicerin (2-MG) képződésével. A 2-MG jó emulgeálószer. A 2-MG 28%-a izomeráz hatására 1-MG-vé alakul. Az 1-MG nagy részét a hasnyálmirigy-lipáz hidrolizálja glicerinné és zsírsavvá, a hasnyálmirigyben a hasnyálmirigy-lipáz a kolipáz proteinnel együtt szintetizálódik. A kolipáz inaktív formában képződik, és a bélben a tripszin hatására részleges proteolízissel aktiválódik. A kolipáz hidrofób doménjével a lipidcsepp felszínéhez kötődik, hidrofil doménje pedig segít a hasnyálmirigy-lipáz aktív központját a lehető legközelebb hozni a TG-hez, ami felgyorsítja a hidrolízisüket.
|
Barna zsírszövet |
|
|
Mennyiség |
Felnőttben kicsi, újszülöttben magas |
|
Lokalizáció |
Tiszta formájában: a vesék és a pajzsmirigy közelében. Vegyes zsírszövet: a lapockák között, a mellkason és a vállakon. |
|
Vérellátás |
Nagyon jó |
|
A zsírsejtek szerkezete |
A citoplazmában sok apró zsírcsepp található, a sejtmag és a sejtszervecskék a sejt közepén helyezkednek el, sok a mitokondrium és a citokróm. |
|
termogenezis |
|
Az oxidáció a mitokondriális mátrixban történik. Először a zsírsav aktiválódik: 1 .A citoplazmában minden sav CoA-8H és ATP energiával aktiválódik. 2. Az aktív zsírsav, az acil-CoA a citoszolból a mitokondriális mátrixba (MC) transzportálódik. A CoA-8H a citoszolban marad, és a zsírsavmaradék - acil - karnitinnel egyesül (a latin - karnitin - húsból - a karnitint az izomszövetből izolálják) acil-karnitint képezve, amely bejut a mitokondriumok membránközi terébe. A mitokondriumok membránközi teréből az acil-karnitin komplex átkerül a mitokondriális mátrixba. Ebben az esetben a karnitin az intermembrán térben marad. A mátrixban az acil egyesül CoA-8H-val. 3. Oxidáció. Az MC mátrixban aktív zsírsav képződik, amely ezt követően oxidációs reakciókon megy keresztül a végtermékekké. A béta-oxidáció során a zsírsav béta-helyzetében lévő CH2- csoport C-csoporttá oxidálódik. Ebben az esetben a dehidrogénezés két szakaszban történik: az acil-dehidrogenáz (flavin enzim, a hidrogén ubikinonba kerül) és a béta-hidroxi-acil-dehidrogenáz (hidrogén-akceptor NAD+) részvételével. Ezután a béta-ketoacil-CoA a tioláz enzim hatására acetil-CoA-ra és acil-CoA-ra bomlik, az eredetihez képest 2 szénatommal rövidülve. Ez az acil-CoA ismét béta-oxidáción megy keresztül. Ennek a folyamatnak az ismételt megismétlése a zsírsav teljes lebomlásához vezet acil-CoA-vá. Zsírsavak oxidációja. 2 szakaszból áll: 1. egy kétszénből álló fragmens szekvenciális lehasítása acetil-CoA formájában a sav C-terminálisáról; 2. acetil-CoA oxidációja a Krebs-ciklusban CO2-vé és H2O-vá. A zsírsav-oxidáció energiaértéke. A sztearinsav (C 18) 8 oxidációs cikluson megy keresztül, 9 acetil-CoA képződésével, minden oxidációs ciklusban 8 * 5 ATP = 40 ATP keletkezik, az acetil-CoA 9 * 12 ATP = 108 ATP-t termel. Összesen: 148 ATP, de 1 ATP fordítódik a citoszolban lévő zsírsav aktiválására, így összesen 147 ATP
β - magasabb zsírsavak (HFA-k) oxidációja. Az eljárás energiahatékonysága (telített és telítetlen zsírsavak esetében). Az IVFA szöveti oxidációjának hatása a szövetek glükózfelhasználására.
β-oxidáció - az el nem ágazó közepes és rövid szénhidrogénláncú zsírsavak sajátos katabolizmusa. A β-oxidáció a mitokondriális mátrixban megy végbe, melynek során 2 C atom egymás után elválik az FA C végétől acetil-CoA formájában. A FA β-oxidációja csak aerob körülmények között megy végbe, és nagy mennyiségű energiaforrás, A FA β-oxidációja aktívan előfordul a vörös vázizmokban, a szívizomban, a vesékben és a májban. A FA-k nem szolgálnak energiaforrásként az idegszövetek számára, mivel a FA-k más hidrofób anyagokhoz hasonlóan nem jutnak át a vér-agy gáton A FA-k β-oxidációja fokozódik a felszívódás utáni időszakban, éhezés és fizikai munka során. Ugyanakkor a FA-k koncentrációja a vérben megemelkedik a zsírszövetből származó FA-k mobilizálása következtében.
LCD aktiválás
Az FA aktiválása az FA és a HSCoA közötti nagy energiájú kötés kialakulásának eredményeként következik be, az Acil-CoA képződésével. A reakciót az Acil-CoA szintetáz enzim katalizálja:
RCOOH + HSKoA + ATP → RCO~SCoA + AMP+ PPn
A pirofoszfátot a pirofoszfatáz enzim hidrolizálja: H 4 P 2 O 7 + H 2 O → 2H 3 PO 4
Az acil-CoA szintetázok mind a citoszolban (a mitokondriumok külső membránján), mind a mitokondriális mátrixban megtalálhatók. Ezek az enzimek különböznek a különböző szénhidrogénlánchosszúságú FA-kra vonatkozó specifitásukban.
Szállítási LCD. A FA-k szállítása a mitokondriális mátrixba a szénlánc hosszától függ.
A rövid és közepes lánchosszúságú (4-12 szénatomos) FA-k diffúzióval behatolhatnak a mitokondriális mátrixba. Ezen FA-k aktiválása a mitokondriális mátrixban található acil-CoA szintetázok révén történik, a hosszú láncú FA-k először a citoszolban aktiválódnak (a külső mitokondriális membránon lévő acil-CoA szintetázok), majd egy speciális transzportrendszer segítségével a mitokondriális mátrixba kerülnek. karnitin használatával. karnitin élelmiszerből származik, vagy lizinből és metioninból szintetizálódik C-vitamin részvételével.
A mitokondriumok külső membránjában a karnitin-aciltranszferáz I (karnitin-palmitoiltranszferáz I) enzim katalizálja az acil átvitelét a CoA-ból a karnitinbe, így acilkarnitin keletkezik;
Az acilkarnitin a membránközi téren keresztül a belső membrán külső oldalára jut, és a karnitin-acilkarnitin transzlokáz a belső mitokondriális membrán belső felületére szállítja;
A karnitin-aciltranszferáz II enzim katalizálja az acil átvitelét a karnitinből az intramitokondriális HSCoA-ba, hogy Acil-CoA-t képezzen;
A szabad karnitint ugyanaz a transzlokáz juttatja vissza a belső mitokondriális membrán citoszolikus oldalára.
Reakciók FA β-oxidációja
1. A β-oxidáció az acil-CoA dehidrogénezésével kezdődik FAD-függő acil-CoA dehidrogenázzal, kettős kötést (transz) hozva létre az Enoil-CoA α- és β-C atomjai között. A CPE-ben oxidáló redukált FADN 2 2 ATP molekula szintézisét biztosítja;
2. Az Enoil-CoA hidratáz vizet ad az Enoil-CoA kettős kötéséhez, hogy β-hidroxiacil-CoA-t képezzen;
3. A β-hidroxi-acil-CoA-t a NAD-függő dehidrogenáz β-ketoacil-CoA-vá oxidálja. A CPE-vé oxidáló redukált NADH 2 biztosítja 3 ATP molekula szintézisét;
4. A tioláz a HCoA részvételével lehasítja az acetil-CoA-t a β-ketoacil-CoA-ból. 4 reakció eredményeként Acil-CoA képződik, amely 2 szénatommal rövidebb, mint az előző Acil-CoA. A képződött acetil-CoA, amely a TCA ciklusban oxidálódik, 12 ATP molekula szintézisét biztosítja a CPE-ben.
Az acil-CoA ezután ismét β-oxidációs reakciókba lép. A ciklusok addig folytatódnak, amíg az Acil-CoA 2 szénatomos acetil-CoA-vá nem alakul (ha az FA páros számú szénatomot tartalmaz) vagy 3 szénatomos butiril-CoA-vá (ha az FA páratlan számú szénatomot tartalmaz).
A páros szénatomszámú telített zsírsavak oxidációjának energiamérlege
Amikor az FA aktiválódik, az ATP 2 makroerg kötése elhasználódik.
A páros számú szénatomot tartalmazó telített FA oxidációja során csak FADH 2, NADH 2 és Acetil-CoA képződik.
A β-oxidáció 1 ciklusa során 1 FADH 2, 1 NADH 2 és 1 Acetil-CoA képződik, amelyek oxidáció során 2 + 3 + 12 = 17 ATP-t termelnek.
A ciklusok száma az FA β-oxidációja során = a szénatomok száma az (FA/2)-1-ben. A β-oxidáció során a palmitinsav (16/2)-1 = 7 cikluson megy keresztül. 7 ciklus alatt 17*7=119 ATP keletkezik.
A β-oxidáció utolsó ciklusát további acetil-CoA képződése kíséri, amely oxidáció során 12 ATP-t termel.
Így a palmitinsav oxidációja során: -2+119+12=129 ATP keletkezik.
Összefoglaló egyenlet a β-oxidációra, palmitoil-CoA:
C15H31CO-CoA + 7 FAD + 7 NAD + + 7 HSKoA → 8 CH 3 -CO-KoA + 7 FADH 2 + 7 NADH 2
A páratlan szénatomszámú telített zsírsavak oxidációjának energiamérlege
A páratlan számú szénatomot tartalmazó telített FA β-oxidációja az elején ugyanúgy megy végbe, mint a páros számú atommal. Az ATP 2 makroerg kötése aktiválódik.
A 17 szénatomos FA β-oxidáción megy keresztül 17/2-1 = 7 ciklus. 1 ciklus alatt 2+3+12=17 ATP képződik 1 FADN 2-ből, 1 NADH 2-ből és 1 Acetil-CoA-ból. 7 ciklus alatt 17*7=119 ATP képződik.
A β-oxidáció utolsó ciklusát nem acetil-CoA, hanem 3 szénatomos propionil-CoA képződése kíséri.
A propionil-CoA-t 1 ATP árán propionil-CoA karboxiláz karboxilezi, D-metil-malonil-CoA-t képezve, amely izomerizáció után először L-metil-malonil-CoA-vá, majd szukcinil-CoA-vá alakul. A szukcinil-CoA részt vesz a TCA-ciklusban, és oxidáció után PCA-t és 6 ATP-t termel. A PIKE beléphet a glükoneogenezisbe a glükóz szintézis érdekében. A B12-vitamin hiánya a metil-malonil felhalmozódásához vezet a vérben és a vizelettel való kiválasztódásához. A FA oxidációja során a következők keletkeznek: -2+119-1+6=122 ATP.
A 17 szénatomos FA-k β-oxidációjának általános egyenlete:
C16H33CO-CoA + 7 FAD + 7 NAD + + 7 HSKoA → 7 CH 3 -CO-KoA + 1 C 2 H 5 -CO-KoA + 7 FADH 2 + 7 NADH 2
A páros szénatomszámú telítetlen zsírsavak oxidációjának energiamérlege
Az emberi szervezetben található zsírsavak körülbelül fele telítetlen. Ezeknek a savaknak a β-oxidációja a szokásos módon megy végbe, amíg a kettős kötés a 3. és 4. szénatom közé nem kerül. Az enoil-CoA izomeráz enzim ezután a kettős kötést a 3-4. pozícióból a 2-3. pozícióba mozgatja, és megváltoztatja a cisz-konformációt. a kettős kötés a transzhoz, ami a β-oxidációhoz szükséges. Ebben a β-oxidációs ciklusban, mivel a kettős kötés már jelen van az FA-ban, nem megy végbe az első dehidrogénezési reakció és nem képződik FADH 2. Továbbá a β-oxidációs ciklusok folytatódnak, nem különbözve a szokásostól.
Az energiamérleget ugyanúgy számítjuk ki, mint a páros számú szénatomot tartalmazó telített FA-k esetében, csak minden kettős kötéshez 1 FADN 2 és ennek megfelelően 2 ATP hiányzik.
A palmitoleil-CoA β-oxidációjának általános egyenlete:
C15H29CO-CoA + 6 FAD + 7 NAD + + 7 HSKoA → 8 CH 3 -CO-KoA + 6 FADH 2 + 7 NADH 2
A palmitoleinsav β-oxidációjának energiamérlege: -2+8*12+6*2+7*3=127 ATP.
Éhség, fizikai aktivitás → glukagon, adrenalin → TG lipolízis zsírsejtekben → FA a vérben → β-oxidáció aerob körülmények között izmokban, májban → 1) ATP; 2) ATP, NADH 2, Acetil-CoA, (FA) → ↓ glikolízis → glükóz megtakarítás szükséges idegszövethez, vörösvértestekhez stb.
Élelmiszer → inzulin → glikolízis → acetil-CoA → malonil-CoA és FA szintézise
Malonil-CoA → malonil-CoA → ↓ karnitin-aciltranszferáz I szintézise a májban → ↓ FA-k transzportja a mitokondriális mátrixba → ↓ FA-k a mátrixban → ↓ FA-k β-oxidációja
IVFA bioszintézise. A palmitát szintáz komplex szerkezete. A folyamat kémiája és szabályozása.
Palmitinsav szintézis
Malonil-CoA képződése
Az FA-szintézis első reakciója az acetil-CoA átalakulása malonil-CoA-vá. Ezt a szabályozó reakciót az FA szintézisben az acetil-CoA karboxiláz katalizálja.
Az acetil-CoA karboxiláz több biotint tartalmazó alegységből áll.
A reakció 2 szakaszban megy végbe:
1) CO 2 + biotin + ATP → biotin-COOH + ADP + Fn
2) acetil-CoA + biotin-COOH → malonil-CoA + biotin
Az acetil-CoA karboxiláz szabályozása többféle módon történik:
3) Enzim alegység komplexek asszociációja/disszociációja. Inaktív formájában az acetil-CoA karboxiláz 4 alegységből álló komplex. A citrát stimulálja a komplexek egyesülését, aminek következtében az enzimaktivitás megnő. A palmitoil-CoA a komplexek disszociációját és az enzimaktivitás csökkenését okozza;
2) Az acetil-CoA karboxiláz foszforilációja/defoszforilációja. A glukagon vagy az adrenalin az adenilát-cikláz rendszeren keresztül serkenti az acetil-CoA karboxiláz alegységeinek foszforilációját, ami inaktiválásához vezet. Az inzulin aktiválja a foszfoprotein foszfatázt, az acetil-CoA karboxiláz defoszforilálódik. Ezután citrát hatására az enzim protomereinek polimerizációja megtörténik, és ez aktívvá válik;
3) A szénhidrátban gazdag és lipidekben szegény élelmiszerek hosszú távú fogyasztása fokozza az inzulin szekréciót, ami indukálja az acetil-CoA karboxiláz, palmitát szintáz, citrát liáz, izocitrát dehidrogenáz szintézisét és felgyorsítja a FA szintézisét és TG. A böjt vagy a zsírban gazdag étrend az enzimek és ennek megfelelően az FA és a TG szintézisének csökkenéséhez vezet.
Palmitinsav képződése
A malonil-CoA képződése után a palmitinsav szintézise a multienzim komplexben folytatódik - zsírsav-szintetáz (palmitoil-szintetáz) .
A palmitoil-szintáz egy dimer, amely két azonos polipeptidláncból áll. Minden láncban 7 aktív hely és egy aciltranszfer fehérje (ACP) található. Mindegyik láncban 2 SH csoport található: az egyik SH csoport a ciszteinhez, a másik a foszfopanteinsavhoz tartozik. Az egyik monomer cisztein SH csoportja a másik protomer 4-foszfopanteteinát SH csoportja mellett helyezkedik el. Így az enzim protomerei „fejtől farokig” helyezkednek el. Bár mindegyik monomer tartalmazza az összes katalitikus helyet, egy 2 protomerből álló komplex funkcionálisan aktív. Ezért 2 LC-t szintetizálnak egyszerre.
Ez a komplex szekvenciálisan kiterjeszti az FA-gyököt 2 szénatommal, amelynek donora malonil-CoA.
Palmitinsav szintézis reakciói
1) Az acetil átvitele a CoA-ból a cisztein SH csoportjába az acetil-transaciláz központ által;
2) malonil átvitele a CoA-ból az ACP SH csoportjába a malonil-transaciláz centrummal;
3) A ketoacil-szintáz centrumban az acetilcsoport a malonilcsoporttal kondenzálódik, így ketoacil keletkezik, és CO 2 szabadul fel.
4) A ketoacilt a ketoacil-reduktáz hidroxiacillá redukálja;
5) Az oxiacilt hidratáz dehidratálja enoillé;
6) Az enoilt az enoil-reduktáz acillá redukálja.
Az első reakcióciklus eredményeként 4 szénatomos acil (butiril) keletkezik. Ezután a butiril a 2. pozícióból az 1. pozícióba kerül (ahol az acetil az első reakcióciklus elején volt). A butiril ezután ugyanazon átalakuláson megy keresztül, és 2 szénatommal meghosszabbodik (malonil-CoA-ból).
Hasonló reakcióciklusok ismétlődnek, amíg egy palmitinsav gyök keletkezik, amely a tioészteráz centrum hatására hidrolitikusan elválik az enzimkomplextől, és szabad palmitinsavvá alakul.
A palmitinsav acetil-CoA-ból és malonil-CoA-ból történő szintézisének általános egyenlete a következő:
CH 3 -CO-SKoA + 7 HOOC-CH 2 -CO-SKoA + 14 NADPH 2 → C 15 H 31 COOH + 7 CO 2 + 6
H 2 O + 8 HSKoA + 14 NADP +
FA-k szintézise palmitinsavból és más FA-kból
A FA-k megnyúlása elongáz reakciókban
A zsírsav meghosszabbodását elongációnak nevezzük. A FA-k szintetizálhatók a palmitinsav és más hosszabb FA-k megnyúlása eredményeként az ER-ben. Minden LC hosszhoz vannak elongázok. A reakciók sorrendje hasonló a palmitinsav szintéziséhez, de ebben az esetben a szintézis nem ACP-vel, hanem CoA-val történik. A májban a fő megnyúlási termék a sztearinsav. Az idegszövetekben hosszú láncú FA-k (C = 20-24) képződnek, amelyek a szfingolipidek szintéziséhez szükségesek.
Telítetlen FA-k szintézise deszaturáz reakciókban
A kettős kötések beépülését az FA gyökökbe deszaturációnak nevezzük. A FA-k deszaturációja az ER-ben megy végbe a deszaturázok által katalizált monooxigenáz reakciókban.
Sztearoil-CoA deszaturáz– integrál enzim, nem hem vasat tartalmaz. Katalizálja 1 kettős kötés kialakulását 9 és 10 szénatom között FA-ban. A sztearoil-CoA deszaturáz elektronokat ad át a citokróm b 5-ről 1 oxigénatomra, a protonok részvételével ez az oxigén vizet képez. A második oxigénatom beépül a sztearinsavba, így hidroxiacil keletkezik, amely olajsavvá dehidrogenizálódik.
Az emberi szervezetben jelenlévő FA-deszaturázok nem tudnak kettős kötést létrehozni a kilencedik szénatomtól távolabbi FA-kban, ezért az ω-3 és ω-6 családba tartozó FA-k nem szintetizálódnak a szervezetben, nélkülözhetetlenek és táplálékkal kell ellátni őket, mivel fontos szabályozó funkciókat lát el. Az emberi szervezetben a deszaturáció következtében képződő fő zsírsavak a palmitolein és az olajsav.
α-hidroxi-FA-k szintézise
Az idegszövetben más FA-k, α-hidroxisavak szintézise is előfordul. A vegyes funkciójú oxidázok a C22 és C24 savakat hidroxilálják cerebronsavvá, amely csak az agyi lipidekben található.
A szénhidrátok teszik ki az emberi táplálkozás nagy részét, és biztosítják a szervezet energiaszükségletének jelentős részét. Kiegyensúlyozott étrend mellett a szénhidrát napi mennyisége átlagosan 4-szerese a fehérjék és zsírok mennyiségének.
A szénhidrátok szerepe a táplálkozásban:
1. A szénhidrátok igen energia funkció. Ha 1 g szénhidrátot oxidálunk, 4,1 kcal energia szabadul fel. A glükóz, amelyre a szénhidrátok nagy része lebomlik, a szervezet fő energiahordozója.
2. Izomtevékenység jelentős glükózfogyasztás kíséri. A fizikai munka során először a szénhidrátokat fogyasztják el, és csak akkor, amikor azok tartalékai (glikogén) kimerülnek, akkor kerül sor a zsírok cseréjére.
3. A szénhidrátok elengedhetetlenek a normál működéshez központi idegrendszer, amelynek sejtjei nagyon érzékenyek a vér glükóz hiányára.
4. A szénhidrátok igen szerkezeti funkciója. Az egyszerű szénhidrátok a glikoproteinek képződésének forrásaként szolgálnak, amelyek a kötőszövet alapját képezik.
5. A szénhidrátok részt vesznek a fehérjék és zsírok anyagcseréjében. A zsírok szénhidrátokból képződhetnek.
6. A növényi eredetű szénhidrátok (cellulóz, pektin anyagok) serkentik a bélmozgást, elősegítik a benne felhalmozódó mérgező termékek kiürülését.
Források a szénhidrátok szolgálnak túlnyomórészt növényi termékek, különösen a lisztből készült termékek, gabonafélék, édességek. A legtöbb élelmiszerben a szénhidrátok keményítő, és kisebb mértékben diszacharidok (tej, cukorrépa, gyümölcsök és bogyók) formájában jelennek meg. A szénhidrátok jobb felszívódásához szükséges, hogy a legtöbbjük keményítő formájában kerüljön a szervezetbe.
A keményítő a gyomor-bélrendszerben fokozatosan glükózzá bomlik, amely kis adagokban kerül a vérbe, ami javítja annak hasznosulását és állandó vércukorszintet tart. Ha egyszerre nagy mennyiségű cukrot adnak be, a glükóz koncentrációja a vérben meredeken megemelkedik, és elkezd ürülni a vizelettel. A legkedvezőbb feltételeknek akkor tekinthetők, ha a szénhidrátok 64%-a keményítő, 36%-a cukor formájában kerül fogyasztásra.
Fogyasztási arány szénhidrát a munka intenzitásától függ. A fizikai munka során a szénhidrátok nagyobb mennyiségben szükségesek. Átlagosan 1 kg testtömegre van szükség 4-6-8 g szénhidrát naponta, azaz. körülbelül 4-szer több, mint a fehérjékben és zsírokban.
Túlzott szénhidrátbevitel elhízáshoz és a gyomor-bélrendszer túlzott túlterheléséhez vezethet, mert a szénhidrátban gazdag növényi élelmiszerek általában terjedelmesebbek, elnehezültek, és rontják a táplálék általános emészthetőségét.
A szénhidrátok hiányaélelmiszerekben szintén nem kívánatos a hipoglikémiás állapotok kialakulásának kockázata miatt. A szénhidráthiányt általában általános gyengeség, álmosság, csökkent memória, szellemi és fizikai teljesítőképesség, fejfájás, fehérjék, vitaminok csökkent emészthetősége, acidózis stb. kíséri. Ebben a tekintetben a napi étrendben a szénhidrát mennyiségét nem szabad 300 g-nál kisebb legyen
A szénhidrátok csoportjával szorosan összefüggenek a legtöbb növényi élelmiszerben megtalálható olyan anyagok, amelyek az emberi szervezet által rosszul emészthetők - a pektin anyagok (emészthetetlen szénhidrátok) és a rostok.
A pektin anyagok azok nagy szorpciós (abszorpciós) képességű növényi zselésítő anyagok. Jótékony hatást fejtenek ki az emésztőrendszeri betegségek, égési sérülések, fekélyek kezelésében, emellett képesek egyes mérgező anyagok semlegesítésére is (különösen aktívak a nehézfémsók, például az ólomvegyületek szervezetből történő eltávolításában).
A narancsban, almában, fekete ribizliben és más gyümölcsökben, bogyókban sok pektin található.
Cellulóz(más nevek - durva növényi, vagy emészthetetlen, vagy élelmiszer, vagy élelmi rost) egy poliszacharid, amely a növényi élelmiszerek hatalmas sejtfalának része. Rostos, meglehetősen durva szerkezetű.
Az élelmi rost általános forrásai a korpa, a kenyér és a gabonafélék (különösen a hajdina és a zabpehely). Nagy mennyiségben megtalálható sok zöldségben, gyümölcsben, növény levelében és szárában; különösen sok van belőle a szemek héjában és a gyümölcsök héjában. Zöldségek és gyümölcsök befőzésekor az élelmi rostok teljesen megőrződnek (kivéve a pép nélküli gyümölcsleveket).
A legtöbb zöldség és gyümölcs magas kalóriatartalma nélkül azonban magas emészthetetlen szénhidráttartalma miatt hozzájárul a gyors és meglehetősen tartós jóllakottság érzéséhez: mivel az élelmi rostok sok folyadékot képesek felszívni, megduzzadnak a gyomrot, töltse meg térfogatának egy részét - és ennek eredményeként a telítettség gyorsabban következik be. Maguk a rostok egyetlen kalóriát sem visznek be a szervezetbe.
A rostok értéke abban rejlik, hogy mivel a napi táplálkozás meglehetősen terjedelmes összetevője, az emberi szervezet nem emészti meg őket. A nagy mennyiségű rost jelenléte némileg csökkenti az élelmiszer általános emészthetőségét. Teljes hiánya azonban káros hatással van a gyomor-bél traktus működésére.
A rostok előidézik a belek megfelelő perisztaltikáját (a falak mozgását), ezáltal elősegítik a táplálék emésztőcsatornán keresztüli mozgását és az emésztetlen tápanyagok eltávolítását a szervezetből.
Az élelmiszerekben található rost szükséges mennyiségét az állati és növényi termékek megfelelő kombinációja biztosítja a napi étrendben.
Lebomlás után a rostok, mint más poliszacharidok, cukrokká alakulnak. Az emberi emésztőrendszerben azonban nincsenek olyan enzimek, amelyek ilyen lebontást végezhetnének. Csak egy kis része emészthető meg a bélben lévő mikroorganizmusok hatására, de nagy része változás nélkül távozik a szervezetből. Ennek a külső haszontalanságnak köszönhetően a rostokat és a pektineket ballasztanyagnak nevezik.
A ballasztanyagok az emésztési folyamatban is fontos szerepet töltenek be: a rostokat a bélbaktériumok erjesztik, és szó szerint segítik az élelmiszer őrlését; a bélfalak idegvégződéseinek irritálásával fokozzák a perisztaltikát. Ha a táplálék ballasztanyagban szegény, a bélmotilitás megzavarodik, ezért e zavarok elkerülése érdekében rostban gazdag durva élelmiszerek fogyasztása javasolt.
Ezen túlmenően az élelmi rostok képesek az anyagcserét serkenteni, mivel a rostok megakadályozzák az élelmiszerrel érkező vagy a feldolgozás során keletkező méreganyagok felszívódását, és egyfajta habverőként szolgálnak: az emésztőrendszeren haladva magukkal visznek mindent, ami a falakhoz ragadt és eltávolítható a testből.
Az élelmi rost másik előnye, hogy képes csökkenteni az endogén koleszterin szintjét (ez az a koleszterin, amely nem a táplálékkal kerül be hozzánk, hanem a szervezet maga állítja elő a májban a bélből a májba jutó epesavakból ).
Hemicellulóz: a rostokhoz vagy a cellulózhoz hasonlóan a gabonatermékek sejtfalának része, és kis mennyiségben megtalálható a gyümölcsök és zöldségek pépében. Képes megtartani a vizet és megkötni a fémeket.
Zsírsavak oxidációja (béta-oxidáció). Szerep H.S. – Ko ebben a folyamatban. A szteorinsav teljes oxidációjának energiája CO 2 c H 2 O . Számítsa ki az oxidáció során keletkező ATP-molekulák számát!
Az FA aktiválása a citoplazmában, a béta-oxidáció pedig a mitokondriumokban megy végbe.
Az acil-CoA nem tud átjutni a mitokondriális membránon. Ezért van egy speciális mechanizmus az FA-knak a citoplazmából a mitokondriumba történő szállítására a „karnitin” anyag részvételével. A mitokondriumok belső membránjában egy speciális transzportfehérje található, amely biztosítja az átvitelt. Ennek köszönhetően az acilkarnitin könnyen áthatol a mitokondriális membránon.
A citoplazmatikus és a mitokondriális karnitin-aciltranszferázok szerkezetükben eltérőek, és kinetikai jellemzőikben is különböznek egymástól. A citoplazmatikus acilkarnitin transzferáz Vmax értéke alacsonyabb, mint a mitokondriális enzim Vmax értéke, és alacsonyabb, mint a β-oxidációs enzimek Vmax értéke. Ezért a citoplazmatikus acilkarnitin-transzferáz kulcsenzim a zsírsavak lebontásában.
Ha egy zsírsav bejut a mitokondriumokba, szükségszerűen acetil-CoA-vá katabolizálódik.
A szervezet energiaszükségletét kielégítő legkompaktabb „üzemanyag” a zsírsav, amelyet kémiai szerkezetük sajátosságai határoznak meg. 1 mólra vetítve a zsírsavak teljes oxidációja többszörösen több felhasználható kémiai energiát szabadít fel, mint a szénhidrátok oxidációja; például 1 mol palmitinsav oxidációja 130 mol ATP-t, míg 1 mol glükóz oxidációja 38 mol ATP-t eredményez. Súlyegységenként az energiakibocsátás is több mint kétszeres eltérést mutat (9 kcal/1 g zsír szemben 4 kcal/1 g szénhidrát vagy fehérje). Ez a magas energiahozam ugyanazon az okon alapul, amely a benzint, a kőolajat és más kőolajtermékeket olyan hatékony tüzelőanyaggá teszi a hő- és mechanikai energia előállítására, nevezetesen a szén nagyfokú redukciója a hosszú alkilláncokban. A zsírsavmolekula fő része ismétlődő egységekből (CH2)n, azaz egy hidrogénben maximálisan dúsított szerkezetből áll. Ahogy az előző előadásból is láthattuk, a biológiai oxidációs folyamatok során elraktározott energia főként a légzőlánc hidrogénatomjaiból irányított elektrontranszferrel, az ADP ATP-vé való foszforilálásával párosulva jön létre. Mivel a zsírsavak elsősorban szénből és hidrogénből állnak, és így lényegesen kevesebb oxigénatomot tartalmaznak, mint a szénhidrátok, a zsírsavak oxidációja arányosan több oxigén felszívódásával jár együtt, és így az oxidatív foszforiláció során több ATP képződésével jár.
Megállapítást nyert, hogy a zsírsavak oxidációja legintenzívebben a májban, a vesében, a váz- és szívizmokban, valamint a zsírszövetben megy végbe. Az agyszövetben a zsírsav oxidáció sebessége nagyon alacsony, mert Az agyszövetben a fő energiaforrás a glükóz.
A β-oxidáció a zsírsav-katabolizmus egy specifikus útja, amelyben 2 szénatom szekvenciálisan elválik a zsírsav karboxilvégétől acetil-CoA formájában. A metabolikus útvonalat - β-oxidációt - azért nevezték így, mert a zsírsav-oxidációs reakciók a β-szénatomon mennek végbe. A β-oxidáció és az acetil-CoA ezt követő oxidációja a TCA ciklusban az oxidatív foszforilációs mechanizmuson keresztül az ATP szintézis egyik fő energiaforrásaként szolgál. A zsírsavak β-oxidációja csak aerob körülmények között megy végbe.
A zsírsavak aktiválása
A különböző reakciókba való belépés előtt a zsírsavakat aktiválni kell, pl. makroerg kötéssel kapcsolódnak a koenzim A-hoz:
RCOOH + HSKoA + ATP → RCO ~ CoA + AMP + PPi.
A reakciót az acil-CoA szintetáz enzim katalizálja. A reakció során felszabaduló pirofoszfátot a pirofoszfatáz enzim hidrolizálja: H 4 P 2 O 7 + H 2 O → 2 H 3 PO 4.
A pirofoszfát nagyenergiájú kötésének hidrolízise során felszabaduló energia a reakció egyensúlyát jobbra tolja el és biztosítja az aktiválási reakció teljességét.
Acil-CoA szintetáz a citoszolban és a mitokondriális mátrixban egyaránt megtalálhatók. Ezek az enzimek különböznek a különböző szénhidrogénlánchosszúságú zsírsavak specifikusságában. A rövid és közepes lánchosszúságú (4-12 szénatomos) zsírsavak diffúzióval behatolhatnak a mitokondriális mátrixba. Ezek a zsírsavak a mitokondriális mátrixban aktiválódnak. Az emberi szervezetben túlsúlyban lévő (12-20 szénatomos) hosszú szénláncú zsírsavakat a mitokondriumok külső membránján található acil-CoA szintetázok aktiválják.
Az aktivált zsírsavak lebontása a hipotézisnek megfelelően történik b - oxidáció F. Knoop, javasolta 1904-ben b - oxidáció történik a mitokondriumokon belül
β- Zsírsav oxidáció- a zsírsav-katabolizmus sajátos útja, amely a mitokondriális mátrixban csak aerob körülmények között fordul elő, és acetil-CoA képződésével végződik. A β-oxidációs reakciókból származó hidrogén belép a CPE-be, az acetil-CoA pedig oxidálódik a citrát körfolyamatban, ami egyben hidrogént is szállít a CPE-be. Ezért a zsírsavak β-oxidációja a legfontosabb anyagcsereút, amely biztosítja az ATP szintézist a légzési láncban.
A β-oxidáció az acil-CoA FAD-függő acil-CoA dehidrogenáz általi dehidrogénezésével kezdődik, és kettős kötés jön létre a reakciótermékben, az enoil-CoA-ban az α és β szénatomok között. Az ebben a reakcióban helyreállított FADH 2 koenzim a CPE-ben lévő hidrogénatomokat Q koenzimmé viszi át. Ennek eredményeként 2 ATP molekula szintetizálódik (8-27. ábra). A következő p-oxidációs reakcióban egy vízmolekulát adnak a kettős kötés helyére, így az OH-csoport az acil β-szénatomján helyezkedik el, és β-hidroxiacil-CoA-t képez. A β-hidroxi-acil-CoA-t ezután NAD+-függő dehidrogenáz oxidálja. A CPE-ben oxidált redukált NADH 3 ATP molekula szintéziséhez biztosít energiát. A keletkező β-ketoacil-CoA a tioláz enzim hatására tiolitikus hasításon megy keresztül, mivel a C-C kötés hasítási helyén egy kénatomon keresztül koenzim-A molekula adódik hozzá.E 4 reakciósor eredményeként a két szénatomos maradék, az acetil-CoA, elválik az acil-CoA-tól. A 2 szénatommal lerövidült zsírsav ismét dehidrogénezési, hidratálási, dehidrogénezési és acetil-CoA eltávolítási reakciókon megy keresztül. Ezt a reakciósorozatot általában "β-oxidációs ciklusnak" nevezik, ami azt jelenti, hogy ugyanazok a reakciók ismétlődnek a zsírsavgyökkel, amíg az összes sav acetilmaradékká nem alakul.
β - Zsírsavak oxidációja.
A b-oxidációs folyamat ciklikus. A ciklus minden egyes fordulatánál 2 szénatom válik le a zsírsavról acetil-maradék formájában.
Ezt követően a 2 szénatommal lerövidült acil-CoA ismét oxidáción megy keresztül (a b-oxidációs reakciók új ciklusába lép). A keletkező acetil-CoA tovább tud belépni a trikarbonsav körforgásba.A zsírsavak lebontásából ki kell tudni számolni az energiahozamot. A bemutatott képlet minden n szénatomot tartalmazó telített zsírsavra igaz A telítetlen zsírsavak lebontása kevesebb ATP-t termel. Minden kettős kötés egy zsírsavban 2 ATP molekula elvesztését jelenti. A b-oxidáció legintenzívebben az izomszövetekben, a vesékben és a májban fordul elő. A FA b-oxidációja következtében acetil-CoA képződik. Az oxidáció sebességét a lipolízis folyamatok sebessége határozza meg. A lipolízis felgyorsulása a szénhidrát-éhezés és az intenzív izommunka állapotára jellemző. A b-oxidáció felgyorsulása számos szövetben megfigyelhető, beleértve a májat is. A máj több acetil-CoA-t termel, mint amennyire szüksége van. A máj „altruista szerv”, ezért a máj glükózt küld más szöveteknek.
A máj arra törekszik, hogy saját acetil-CoA-ját küldje el más szövetekhez, de nem tudja, mivel a sejtmembránok áthatolhatatlanok az acetil-CoA számára. Ezért az acetil-CoA-ból a májban speciális anyagok, úgynevezett „ketontestek” szintetizálódnak. A ketontestek az acetil-CoA speciális szállítási formája.
A zsírsavmolekula mitokondriumokká bomlik a két szénből álló fragmensek fokozatos eliminálásával acetil-koenzim A (acetil-CoA) formájában.
C17H35COOH + 26 O2 = 18 CO2 + 18 H2O.
Amikor a sztearinsav oxidálódik, a sejt 146 ATP-molekulát kap.