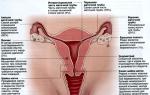
Tehneetsium sestamibi. Tehneetsium Radionukliididega märgistatud vererakud
See on Uljanovski oblastis Dimitrovgradi linnas asuva aatomireaktorite uurimisinstituudi artiklite seeria viimane osa. Oleme juba tutvunud planeedi kõige kallima metalli tootmise tehnoloogiaga – oleme õppinud, kuidas valmistatakse tuumareaktorite kütuseagregaate, ja oleme näinud ainulaadset SM-3 reaktorit, mis on võimeline tekitama väga tihedat neutronivoogu. . Kuid ikkagi pole see peamine toode, mida uurimisinstituut toodab. On üks aine, ilma milleta kõik maailma onkoloogiakliinikud ei ela päevagi. Selle radioisotoobi hind ulatub 46 miljoni dollarini grammi kohta. Mis ainega on tegu ja miks põhjustab selle tarnete väikseimgi häire globaalses nukleaarmeditsiinis suurt kära – loe edasi...

Tehneetsium ja molübdeen
See aine on molübdeen-99, mille abil tehakse täna onkoloogia valdkonnas umbes 70%, kardioloogias 50% ja radionukliiddiagnostikas umbes 90% diagnostilistest protseduuridest. Kuna seda on raske ja kallis hankida, on see laialdaselt saadaval vaid vähestes arenenud riikides. Kuidas aga aitab molübdeen-99 diagnostikas?

Tegelikult pole see nii lihtne. Molübdeen-99 ei ole tuumameditsiinis kasutatav lõpptoode. Selle tööhobune on teine radioaktiivne metall - tehneetsium-99.
Segaduses? Püüan selgitada.
Enamik kunstlikult toodetud isotoope (sama keemilise elemendi sordid) on väga ebastabiilsed ja lagunevad kiiresti radioaktiivse kiirguse toimel. Aega, mille möödudes jääb järele täpselt pool aine esialgsest kogusest (tegelikult tehakse mõõtmised Curie aktiivsuse väärtuse põhjal, kuid lihtsuse huvides loeme massi), nimetatakse poolestusajaks. Näiteks üks gramm tollest väga kallist California-252-st muutub 2,5 aasta pärast pooleks grammiks ning perioodilisuse tabeli uusim ja viimati saadud 118. element Ununoctium-294 väheneb pooleks vaid 1 ms-ga. Meie megakasuliku isotoobi tehneetsium-99 poolestusaeg on vaid 6 tundi. See on nii selle eelis kui ka puudus.

RIARi reaktorihoone
Selle isotoobi kiirgus on üsna pehme, ei mõjuta naaberorganeid ja sobib ideaalselt spetsiaalse seadmega salvestamiseks. Tehneetsium võib akumuleeruda kasvajaga mõjutatud organitesse või südamelihase surnud piirkondadesse, mistõttu on seda meetodit kasutades võimalik näiteks müokardiinfarkti kolde tuvastada 24 tunni jooksul pärast selle algust – probleemsed piirkonnad kehas lihtsalt hävivad. pildil või ekraanil esile tõstetud. Mõni tund pärast manustamist muutub tehneetsium-99 stabiilsemaks isotoobiks ja eritub organismist täielikult ilma tervisemõjudeta. Need 6 tundi valmistavad aga peavalu ka arstidele, kuna nii lühikese ajaga on seda lihtsalt võimatu tootmiskohast kliinikusse toimetada.

RIAR Dimitrovgradis
Ainus väljapääs sellest olukorrast on tehneetsium-99 tootmine kohapeal, otse diagnostikakliinikus. Aga kuidas seda teha? Kas tõesti on vaja varustada iga kliiniku tuumareaktoriga? Õnneks polnud seda vaja. Asi on selles, et tehneetsium-99 saab suhteliselt lihtsalt ja ilma reaktorita saada teisest isotoobist - molübdeen-99, mille poolestusaeg on juba 66 tundi! Ja see on enam-vähem adekvaatne aeg, mille jooksul saab isotoobi kõikjalt maailmast kliinikusse toimetada. Kliiniku spetsialistid saavad Molübdeen-99 tehneetsium-99-ks muuta ainult spetsiaalse tehneetsiumigeneraatori abil

Generaatoris toimub molübdeen-99 loomulik lagunemine, mille üheks produktiks on tehneetsium-99, mis eraldatakse keemiliselt - soolalahus uhub tehneetsiumi välja, kuid jätab molübdeeni oma kohale. Sarnast protseduuri saab teha mitu korda päevas nädala jooksul, pärast mida tuleb generaator värske vastu välja vahetada. See vajadus on seotud molübdeen-99 aktiivsuse vähenemisega selle lagunemise tõttu, samuti tehneetsiumi saastumise algusega molübdeeniga. "Vana" generaator muutub meditsiiniliste vajaduste jaoks sobimatuks. Molübdeen-99 lühikese poolestusaja tõttu on tehneetsiumigeneraatorite varumine võimatu. Nende regulaarsed tarned on nõutavad iganädalaselt või isegi lühemate perioodide kaupa.
Seega on molübdeen-99 omamoodi lähteisotoop, mida on mugav lõppkasutajale transportida. Nüüd jõuame kõige olulisema asjani - molübdeen-99 saamise protsessi.
Kuidas valmistatakse molübdeen-99
Molübdeen-99 on võimalik saada ainult kahel viisil ja ainult tuumareaktoris. Esimene võimalus on võtta stabiilne isotoop Molübdeen-98 ja kasutada tuumaneutronite püüdmise reaktsiooni, et muuta see molübdeen-99-ks. See on "puhtaim" meetod, mis aga ei võimalda saada isotoobi kaubanduslikku mahtu. Tuleb märkida, et see meetod on paljulubav ja seda praegu täiustatakse. Täna kasutab Jaapan seda meetodit oma vajaduste jaoks molübdeeni tootmiseks.

Teine meetod on tugevalt rikastatud uraan-235 tuumade lõhustamine tiheda neutronite vooga. Kui uraani sihtmärki "tulistada" neutronitega, laguneb see paljudeks kergemateks elementideks, millest üks on molübdeen-99. Kui olete selle artiklisarja esimest osa juba lugenud, peaksite ilmselt meeles pidama ainulaadset omataolist, mis genereerib sama tiheda neutronite voo - mürsud, mis purustavad uraani vaarikad mitmeks väikeseks "marjaks". .

Sihtmärgid võivad olla erineva kujuga – plaadid, vardad jne. Need võivad olla valmistatud uraani metallist, selle oksiidist või sulamist mõne muu metalliga (näiteks alumiiniumiga). Alumiiniumist või roostevabast terasest kestades sihtmärgid asetatakse reaktori aktiivkanalisse ja hoitakse seal teatud aja.

RIARi reaktor SM-3
Pärast sihtmärgi eemaldamist reaktorist jahutatakse seda pool päeva veega ja viiakse spetsiaalsesse "kuuma" laborisse, kus soovitud molübdeen-99 isoleeritakse keemiliselt uraani lõhustumisproduktide segust, millest ainult 6%. ole seal. Sellest hetkest algab meie molübdeeni eluea loendus, mille eest klient on nõus maksma. See protseduur tuleb läbi viia nii kiiresti kui võimalik, kuna pärast sihtmärgi kiiritamist kaob selle lagunemise tõttu igas tunnis kuni 1% molübdeenist.

“Kuumas” kambris muudetakse elektromehaaniliste manipulaatorite abil sihtmaterjal leelise või happe abil vedelaks lahuseks, millest erinevate keemiliste reaktiivide abil eraldub molübdeen. RIAR kasutab leeliselist meetodit, mis on ohutum kui happemeetod, kuna jätab maha vähem ohtlikke vedelaid jäätmeid.

Lõpptoode näeb välja nagu värvitu vedelik – naatriummolübdaatsoola lahus.

foto ngs.ru
Vedelikupudel asetatakse spetsiaalsesse pliimahutisse ja saadetakse tarbijale erilennuga lähimast Uljanovski lennujaamast.

Kogu protsessi juhib arvutisüsteem. välja arvatud operaatori viga ja inimfaktor, mis on molübdeen-99 tootmisel väga oluline. Samuti on vaja järgida kõiki ohutusnõudeid.

Kahjuks on ülalkirjeldatud meetod suure hulga radioaktiivsete jäätmete tekitamise seisukohalt äärmiselt “räpane”, mida edaspidi praktiliselt ei kasutata ja mis tuleb maha matta. Olukorda raskendab veelgi asjaolu, et need jäätmed on vedelad – neid on kõige keerulisem ladustada ja kõrvaldada. Muide, 97% algsest sihtmärgi uraani laadimisest jõuab jäätmete hulka! Puhtalt teoreetiliselt saab jäätmetest kõrgelt rikastatud uraani kaevandada edasiseks kasutamiseks, kuid praktikas ei tee seda keegi.

Probleemid
Kuni viimase ajani oli maailmas vaid 3 peamist molübdeen-99 tootjat ja nende arvele langes 95% kõigist tarnetest. Dimitrovgradi RIAR kattis selle isotoobi vajadusest vaid kuni 5%. Kõige võimsamad tegijad selles valdkonnas olid Kanada (40%), Holland + Belgia (45%) ja Lõuna-Aafrika Vabariik (10%). Kanada suurimal tarnijal tekkis aga probleeme oma peamise tootmisreaktoriga ja ootamatult tekkis nišš. Rosatom nägi selles võimalust seda lühikeseks ajaks hõivata.
Molübdeen-99 puudus maailmaturul ületab praegu 30%, keskmise vajadusega kuni 12 000 curied nädalas (seda toodangut mõõdetakse mitte grammides, vaid materiaalse aktiivsuse ühikutes). Ja selle aine hinnad ulatuvad 1500 dollarini curie kohta.
Selliste molübdeen-99 tootmismahtude juures tekib aga küsimus radioaktiivsete jäätmete koguse proportsionaalsest suurenemisest, mis tuleb kuhugi ladustada. Kahjuks on ainus viis vedelate jäätmete matmiseks RIAR-i endiselt rõhu all pumbata 1300 meetri sügavusele. See on väga ohtlik, arvestades ladustamiskoha asukohta tektooniliste rikete ristumiskohas (vastavalt TsNIIgeolneruda uuringutele). Täna on see kõige valusam probleem, millele lahendust veel pole: Dimitrovgradi lähedale on maa alla juba tekkinud väike radioaktiivsete jäätmete meri, mis teoreetiliselt võib sattuda Volgasse.

RIARi uue mitmeotstarbelise kiirneutronreaktori ehitamine
Üldjuhul tuleb vedelad jäätmed tsementeerimise teel muuta tahketeks jäätmeteks ja ladustada spetsiaalsetes konteinerites. RIAR ehitas 2015. aastal uue tahkejäätmete hoidla mahuga 8000 kuupmeetrit, kus on sorteerimise, töötlemise ja konditsioneerimise tehnoloogilised alad.

foto niiar.ru
IAEA on enam kui kahe aastakümne jooksul väljendanud äärmist rahulolematust kõrgelt rikastatud uraani kasutamise tehnoloogiaga molübdeen-99 tootmisel. Kuid RIAR-is kasutatav tehnoloogia on loodud spetsiaalselt selle meetodi jaoks. Aja jooksul kavatseb Dimitrovgradi uurimisinstituut minna üle madala rikastatud uraaniga töötamisele. Kuid see on tuleviku küsimus ja praegu on molübdeeni tootmise kõige keerulisem küsimus radioaktiivsete jäätmete kõrvaldamine.

Ja neid on palju ja nad kõik on keskkonnale ja elanikkonnale äärmiselt ohtlikud. Võtame näiteks strontsiumi ja joodi isotoobid, mis võivad kergesti atmosfääri sattuda ja levida sadu kilomeetreid. Piirkonnas, kus elanikel on loomulik joodipuudus, on see eriti ohtlik. Organism võtab vajaliku joodi keskkonnast, sealhulgas radioaktiivsest, mis toob kaasa kurbad tagajärjed tervisele. Kuid RIARi sõnul on nende tehnoloogiline protsess väga kaitstud joodiheitmete eest atmosfääri.

Kingsepp ilma kingadeta
Igal aastal tehakse maailmas radionukliide kasutades üle 30 miljoni meditsiinilise protseduuri. Venemaal endas, mis väidab end olevat molübdeen-99 peamine tarnija, on aga vajadus selle isotoobi järele minimaalne. Üle 70% kõigist Venemaal toodetud radioaktiivsetest isotoopidest eksporditakse. Venemaal on vähihaigetel võimalus saada kaasaegset ja õigeaegset ravi, mis ei ületa 10%, kuna spetsialiseerunud diagnostikakeskuste banaalne puudumine. Selliseid keskusi on riigis vaid seitse. Aga neid peab olema vähemalt 140. Selgub, et uusimatel isotoope kasutavatel tehnoloogiatel pole Venemaal sageli lihtsalt kuhugi rakendada.

Võrdluseks, Ameerika Ühendriikides on üle 2000 nukleaarmeditsiini keskuse. Teistes arenenud riikides on üks selline keskus iga 500 tuhande inimese kohta. Pole üllatav, et WHO andmetel on vähihaigete viieaastane elulemus USA-s 62%, Prantsusmaal - 58%, Venemaal ei ulatu see näitaja isegi 43% -ni.
See loob mitte eriti õnneliku pildi: mõne jaoks topsid, aga meile juured.
Vene nimi
Tehneetsium sestamibiAine ladinakeelne nimetus on Technetium sestamibi
Tehnetii sestamibi ( perekond. Tehniline sestamibi)Aine tehneetsium sestamibi farmakoloogiline rühm
Tüüpiline kliiniline ja farmakoloogiline artikkel 1
Farmatseutiline toime. Diagnostiline aine (radiofarmatseutiline ravim), mis on ette nähtud müokardi perfusiooni hindamiseks mitmesuguste patoloogiliste seisundite korral.
Farmakokineetika. Pärast IV manustamist lahkub see kiiresti veresoonte voodist ja 3-5 minuti pärast ei ületa selle kontsentratsioon veres 2%. Ravimi maksimaalne akumulatsioon terves müokardis täheldatakse 5 minutit pärast manustamist ja see on keskmiselt 2,2% manustatud annusest. See müokardi omastamise tase püsib muutumatuna 3 tundi, mis määrab tasapinnalise või ühefotoni emissioontomograafia optimaalse aja (1-2 tunni jooksul pärast ravimi manustamist).Ravimi kontsentratsioon kopsudes on ebaoluline (5 minuti pärast - mitte rohkem kui 3-5%) ja selle eemaldamine määrab oluliselt ravimi kliirensi müokardist. See eritub maksa- ja sapiteede ning peensoole kaudu (umbes 40% 2 päeva jooksul). Väiksem kogus (umbes 22%) eritub uriiniga.
Näidustused. Planaar- või ühefotoni emissioontomograafia müokardi verevarustuse hindamiseks mitmesugustes patoloogilistes protsessides, mis põhjustavad müokardi perfusiooni häireid (koronaarateroskleroos, äge müokardiinfarkt, infarkti- ja müokardijärgne kardioskleroos jne), samuti koronaararterite haiguse korral.
Vastunäidustused.Ülitundlikkus, rasedus.
Doseerimine. IV tühja kõhuga või vähemalt 4 tundi pärast sööki. Patsientide uurimisel puhkeolekus ja stressitesti tingimustes umbes 24-tunnise intervalliga uuringutes - 259-370 MBq (7-10 mKu) iga uuringu kohta.
Kõrvalmõju. Allergilised reaktsioonid.
Erijuhised. Ettevalmistusprotseduur: lisage aseptilistes tingimustes reaktiivipudelisse 3 ml eluaati 99mTc generaatorist. Vajadusel lahjendatakse eluaat esmalt 0,9% NaCl lahusega vajaliku mahulise aktiivsuseni. Pudel ravimiga asetatakse pliimahutisse ja kuumutatakse keeva veevannis 15 minutit alates vee keemisest. Veetase veevannis peaks olema kõrgem kui viaalis oleva ravimi lahuse tase. Ravim on kasutamiseks valmis pärast pudeli sisu jahutamist toatemperatuurini. Ärge kasutage õhunõela.
Valmis ravimit, mis on valmistatud 1 pudelis sisalduva reagendi alusel, saab kasutada 5 patsiendi uurimiseks.
Imetavad emad peaksid hoiduma oma lapse toitmisest 24 tunni jooksul pärast ravimi manustamist.
Riiklik ravimite register. Ametlik väljaanne: 2 köites - M.: Arstinõukogu, 2009. - 2. köide, 1. osa - 568 lk; 2. osa - 560 s.
Artikli sisu
TEHNETIUM– tehneetsium (lat. tehneetsium, tähis Tc) – perioodilisustabeli rühma element 7 (VIIb), aatomnumber 43. Tehneetsium on perioodilisuse tabeli kõige kergem element, millel puuduvad stabiilsed isotoobid ja esimene kunstlikult saadud element . Tänaseks on sünteesitud 33 tehneetsiumi isotoopi massinumbritega 86–118, neist stabiilseimad on 97 Tc (poolestusaeg 2,6 10 6 aastat), 98 Tc (1,5 10 6) ja 99 Tc (2,12 ·10 5). aastat).
Ühendites on tehneetsiumi oksüdatsiooniaste vahemikus 0 kuni +7, kõige stabiilsem on heptavalentne olek.
Elemendi avastamise ajalugu.
Elemendi nr 43 suunatud otsingud algasid perioodilisuse seaduse avastamisega D. I. Mendelejevi poolt aastal 1869. Perioodilisuse tabelis olid mõned lahtrid tühjad, kuna neile vastavad elemendid (nende hulgas oli 43. - ekamangaan) polnud veel teada. . Pärast perioodilise seaduse avastamist teatasid paljud autorid umbes saja aatommassiga mangaani analoogi eraldamisest erinevatest mineraalidest ja pakkusid sellele välja nimed: davy (Kern, 1877), lutsium (Barrier, 1896) ja nippoonium. (Ogawa, 1908), kuid kõiki neid teateid enam ei kinnitatud.
1920. aastatel alustas rühm saksa teadlasi professor Walter Noddacki juhtimisel ekamangaani otsimist. Olles jälginud elementide omaduste muutumise mustreid rühmade ja perioodide lõikes, jõudsid nad järeldusele, et element nr 43 peaks oma keemiliste omaduste poolest olema palju lähedasem mitte mangaanile, vaid selle perioodi naabritele: molübdeenile ja osmiumile, seega oli vaja seda otsida plaatina- ja molübdeenimaakides. Noddacki rühma eksperimentaalne töö jätkus kaks ja pool aastat ning 1925. aasta juunis teatas Walter Noddack elementide nr 43 ja 75 avastamisest, mida pakuti nimetada masuriumiks ja reeniumiks. 1927. aastal kinnitati lõpuks reeniumi avastamine ja kõik selle rühma jõud läksid masuriumi isoleerimisele. Walter Noddacki töötaja ja naine Ida Noddack-Tacke väitis isegi, et "varsti on masrium, nagu reenium, poodides müügil", kuid sellisel tormakal väitel ei olnud määratud tõeks saada. Saksa keemik W. Prandtl näitas, et paar pidas lisandeid masuumiks, millel polnud midagi pistmist elemendiga nr 43. Pärast Noddaksi ebaõnnestumist hakkasid paljud teadlased kahtlema elemendi nr 43 olemasolus looduses.
Veel 1920. aastatel märkas Leningradi ülikooli töötaja S.A. Shchukarev radioaktiivsete isotoopide jaotumises teatud mustrit, mille sõnastas lõpuks 1934. aastal saksa füüsik G. Matthauch. Mattauch-Shchukarevi reegli järgi ei saa looduses eksisteerida kahte stabiilset isotoopi, millel on sama massinumber ja tuumalaengud, mis erinevad ühe võrra. Vähemalt üks neist peab olema radioaktiivne. Element nr 43 asub molübdeeni (aatommass 95,9) ja ruteeniumi (aatommass 101,1) vahel, kuid kõik massinumbrid 96 kuni 102 on hõivatud stabiilsete isotoopidega: Mo-96, Mo-97, Mo-98, Ru-99 , Mo-100, Ru-101 ja Ru-102. Seetõttu ei saa elemendil nr 43 olla mitteradioaktiivseid isotoope. See aga ei tähenda, et seda Maalt leida ei võiks: uraan ja toorium on ju samuti radioaktiivsed, kuid säilinud tänu oma pikale poolestusajale tänapäevani. Ja veel, nende varud vähenesid Maa eksisteerimise ajal (umbes 4,5 miljardit aastat) 100 korda. Lihtsad arvutused näitavad, et radioaktiivne isotoop võib meie planeedile jääda märkimisväärses koguses ainult siis, kui selle poolestusaeg ületab 150 miljonit aastat. Pärast Noddaki grupi otsingute ebaõnnestumist kadus lootus sellist isotoopi leida praktiliselt. Tehneetsiumi stabiilseima isotoobi poolestusaeg on praegu teadaolevalt 2,6 miljonit aastat, seega oli elemendi nr 43 omaduste uurimiseks vaja see uuesti luua. Noor itaalia füüsik Emilio Gino Segre võttis selle ülesande 1936. aastal. Aatomite kunstliku tootmise põhimõttelist võimalust demonstreeris 1919. aastal suur inglise füüsik Ernest Rutherford.
Pärast Rooma ülikooli lõpetamist ja nelja-aastase ajateenistuse läbimist töötas Segre Enrico Fermi laboris, kuni sai pakkumise Palermo ülikooli füüsikaosakonna juhatajaks. Muidugi lootis ta sinna minnes jätkata tööd tuumafüüsika alal, kuid labor, kus ta pidi töötama, oli väga tagasihoidlik ega soodustanud teadussaavutusi. 1936. aastal läks ta tööreisile USA-sse, Berkeley linna, kus California ülikooli kiirguslaboris töötas juba mitu aastat maailma esimene laetud osakeste kiirendi tsüklotron. Berkeleys töötades tekkis tal idee analüüsida molübdeeniplaati, mis aitas kõrvale suunata vesiniku raske isotoobi deuteeriumi tuumade kiirt. "Meil oli põhjust arvata," kirjutas Segre, "et molübdeen peaks pärast deuteroonidega pommitamist muutuma elemendiks number 43..." Tõepoolest, molübdeeni aatomi tuumas on 42 prootonit ja deuteeriumis. tuum – 1. Kui need osakesed saaksid ühineda, saaksid nad 43. elemendi tuuma. Looduslik molübdeen koosneb kuuest isotoobist, mis tähendab, et kiiritatud plaadis võib olla mitu uue elemendi isotoopi. Segre lootis, et vähemalt mõned neist on piisavalt pikaealised, et pärast Itaaliasse naasmist taldrikul ellu jääda, kus ta kavatses otsida elementi nr 43. Ülesande tegi veelgi keerulisemaks asjaolu, et sihtmärgi valmistamisel kasutati molübdeeni. ei olnud spetsiaalselt puhastatud ja plaadil võivad tekkida tuumareaktsioonid, mis hõlmavad lisandeid.
Kiirguslabori juhataja Ernest Lawrence lubas Segrel taldriku endaga kaasa võtta ning 30. jaanuaril 1937 asusid Palermos tööle Emilio Segre ja mineraloog Carlo Perrier. Esialgu tuvastasid nad, et toodud molübdeeni proov eraldas beetaosakesi, mis tähendab, et radioaktiivsed isotoobid olid selles tõepoolest olemas, kuid nende hulgas oli element nr 43, kuna tuvastatud kiirguse allikad võisid olla tsirkooniumi, nioobiumi, ruteeniumi isotoobid. , reenium, fosfor ja molübdeen ise ? Sellele küsimusele vastamiseks lahustati osa kiiritatud molübdeenist vees (vesinikkloriid- ja lämmastikhappe segu) ning radioaktiivne fosfor, nioobium ja tsirkoonium eemaldati keemiliselt ning seejärel sadestati välja molübdeensulfiid. Ülejäänud lahus oli endiselt radioaktiivne, see sisaldas reeniumi ja võib-olla elementi nr 43. Nüüd jäi kõige keerulisem - eraldada need kaks sarnaste omadustega elementi. Segre ja Perrier said selle ülesandega hakkama. Nad leidsid, et kui reeniumsulfiid sadestatakse kontsentreeritud vesinikkloriidhappe lahusest vesiniksulfiidiga, jäi osa aktiivsusest lahusesse. Pärast ruteeniumi ja mangaani isotoopide eraldamise kontrollkatseid sai selgeks, et beetaosakesi saavad emiteerida ainult uue elemendi aatomid, mida kutsuti tehneetsiumiks kreekakeelsest sõnast tecnh ós - "kunstlik". See nimi kinnitati lõpuks 1949. aasta septembris Amsterdamis toimunud keemikute kongressil. Kogu töö kestis üle nelja kuu ja lõppes 1937. aasta juunis, mille tulemusena saadi tehneetsiumi vaid 10–10 grammi.
Kuigi Segre ja Perrier käes oli mikrokogustes elementi nr 43, suutsid nad siiski kindlaks teha mõned selle keemilised omadused ja kinnitasid perioodilise seaduse alusel ennustatud tehneetsiumi ja reeniumi sarnasust. On selge, et nad tahtsid uue elemendi kohta rohkem teada saada, kuid selle uurimiseks vajasid nad tehneetsiumi massi ja kiiritatud molübdeen sisaldas liiga vähe tehneetsiumi, mistõttu tuli leida sobivam kandidaat selle elemendi tarnimiseks. Tema otsinguid kroonis edu 1939. aastal, kui O. Hahn ja F. Strassmann avastasid, et uraan-235 lõhustumisel tuumareaktoris neutronite mõjul tekkinud "fragmendid" sisaldasid üsna märkimisväärses koguses pikaealist isotoopi. 99 Tc. Järgmisel aastal suutsid Emilio Segre ja tema kaastöötaja Wu Jianxiong selle puhtal kujul isoleerida. Iga kilogrammi selliste "fragmentide" kohta on kuni kümme grammi tehneetsium-99. Algul oli tuumareaktorijäätmetest saadav tehneetsium väga kallis, tuhandeid kordi kallim kui kuld, kuid tuumaenergeetika arenes väga kiiresti ja 1965. aastaks langes “sünteetilise” metalli hind 90 dollarile grammi eest, selle globaalne toodang oli ei arvutata enam milligrammides, vaid sadades grammides. Selle elemendi sellistes kogustes suutsid teadlased põhjalikult uurida tehneetsiumi ja selle ühendite füüsikalisi ja keemilisi omadusi.
Tehneetsiumi leidmine loodusest. Hoolimata asjaolust, et tehneetsiumi pikima elueaga isotoobi - 97 Tc poolestusaeg (T 1/2) on 2,6 miljonit aastat, mis näib välistavat täielikult selle elemendi tuvastamise võimaluse maakoores, saab tehneetsiumi aastal tekkis Maal pidevalt tuumareaktsioonide tulemusena. 1956. aastal väitsid Boyd ja Larson, et maakoores leidub sekundaarset päritolu tehneetsiumi, mis tekib molübdeeni, nioobiumi ja ruteeniumi aktiveerimisel kõva kosmilise kiirgusega.
Tehneetsiumi moodustamiseks on veel üks viis. Ida Noddack-Tacke ennustas ühes oma väljaandes uraani tuumade iseenesliku lõhustumise võimalust ning 1939. aastal kinnitasid Saksa radiokeemikud Otto Hahn ja Fritz Strassmann seda eksperimentaalselt. Üks spontaanse lõhustumise saadusi on elemendi nr 43 aatomid. 1961. aastal suutis Kuroda, töödeldes umbes viis kilogrammi uraanimaaki, veenvalt tõestada tehneetsiumi olemasolu selles koguses 10–9 grammi kohta. kilogrammi maaki.
1951. aastal pakkus Ameerika astronoom Charlotte Moore, et tehneetsiumi võib taevakehades esineda. Aasta hiljem avastas inglise astrofüüsik R. Merrill kosmoseobjektide spektreid uurides tehneetsiumi mõnedes Andromeeda ja Cetuse tähtkujude tähtedes. Tema avastust kinnitasid hiljem sõltumatud uuringud ja tehneetsiumi kogus mõnel tähel erineb vähe naabruses asuvate stabiilsete elementide: tsirkooniumi, nioobiumi, molübdeeni ja ruteeniumi sisaldusest. Selle fakti selgitamiseks pakuti välja, et tehneetsium tekib tänapäeval tähtedes tuumareaktsioonide tulemusena. See tähelepanek lükkas ümber kõik arvukad teooriad elementide eeltähe tekke kohta ja tõestas, et tähed on ainulaadsed keemiliste elementide tootmise “tehased”.
Tehneetsiumi saamine.
Tänapäeval saadakse tehneetsiumi kas tuumkütuse ümbertöötlemise jäätmetest või tsüklotronis kiiritatud molübdeeni sihtmärgist.
Aeglaste neutronite põhjustatud uraani lõhustumisel moodustub kaks tuumafragmenti - kerge ja raske. Saadud isotoopides on neutronite ülejääk ja beeta-lagunemise või neutronite emissiooni tulemusena muutuvad need muudeks elementideks, põhjustades radioaktiivsete muundumiste ahelaid. Tehneetsiumi isotoobid moodustuvad mõnes neist ahelatest:
235 U + 1 n = 99 Mo + 136 Sn + 1 n
99 Mo = 99 m Tc + b – (T 1/2 = 66 tundi)
99 m Tc = 99 Tc (T 1/2 = 6 tundi)
99 Tc = 99 Ru (stabiilne) + 227 – (T 1/2 = 2,12 10 5 aastat)
See ahel sisaldab isotoopi 99m Tc, tehneetsium-99 tuumaisomeeri. Nende isotoopide tuumad on oma nukleoonse koostise poolest identsed, kuid erinevad radioaktiivsete omaduste poolest. 99m Tc tuumal on suurem energia ja kaotades selle g-kiirguse kvanti kujul, läheb see 99 Tc tuuma.
Tehnoloogilised skeemid tehneetsiumi kontsentreerimiseks ja sellega kaasnevatest elementidest eraldamiseks on väga mitmekesised. Need hõlmavad destilleerimise, sadestamise, ekstraheerimise ja ioonvahetuskromatograafia etappide kombinatsiooni. Tuumareaktorite kasutatud tuumkütuseelementide (kütuseelementide) töötlemise kodumaine skeem näeb ette nende mehaanilise purustamise, metallkesta eraldamise, südamiku lahustamise lämmastikhappes ning uraani ja plutooniumi ekstraheerimise. Sel juhul jääb tehneetsium pertehnetaadi iooni kujul lahusesse koos teiste lõhustumisproduktidega. Selle lahuse juhtimisel läbi spetsiaalselt valitud anioonvahetusvaigu, millele järgneb desorptsioon lämmastikhappega, saadakse pertehnhappe (HTcO 4) lahus, millest pärast neutraliseerimist sadestatakse tehneetsium (VII) sulfiid vesiniksulfiidiga:
2HTcO4 + 7H2S = Tc2S7 + 8H2O
Tehneetsiumi sügavamaks puhastamiseks lõhustumisproduktidest töödeldakse tehneetsiumsulfiidi vesinikperoksiidi ja ammoniaagi seguga:
Tc2S7 + 2NH3 + 7H2O2 = 2NH4TcO4 + 6H2O + 7S
Seejärel ekstraheeritakse lahusest ammooniumpertehnetaat ja järgnev kristallimine annab keemiliselt puhta tehneetsiumi preparaadi.
Metallist tehneetsiumi saadakse tavaliselt ammooniumpertehnetaadi või tehneetsiumdioksiidi redutseerimisel vesinikuvoolus temperatuuril 800–1000 °C või pertehnetaatide elektrokeemilise redutseerimise teel:
2NH4TcO4 + 7H2 = 2Tc + 2NH3 + 8H2O
Tehneetsiumi eraldamine kiiritatud molübdeenist oli varem metalli tööstusliku tootmise peamine meetod. Seda meetodit kasutatakse nüüd tehneetsiumi saamiseks laboris. Tehneetsium-99m tekib molübdeen-99 radioaktiivsel lagunemisel. Suur erinevus 99m Tc ja 99 Mo poolestusaegades võimaldab viimast kasutada tehneetsiumi perioodiliseks eraldamiseks. Selliseid radionukliidide paare nimetatakse isotoopide generaatoriteks. Maksimaalne 99m Tc akumuleerumine 99 Mo/ 99m Tc generaatoris toimub 23 tundi pärast iga isotoopide eraldamise operatsiooni lähteainest molübdeen-99, kuid 6 tunni pärast on tehneetsiumisisaldus pool maksimumist. See võimaldab tehneetsium-99m isoleerida mitu korda päevas. Tütarisotoobi eraldamise meetodil põhinevaid 99m Tc generaatoreid on 3 peamist tüüpi: kromatograafiline, ekstraheerimine ja sublimatsioon. Kromatograafilised generaatorid kasutavad tehneetsiumi ja molübdeeni jaotuskoefitsientide erinevust erinevatel sorbentidel. Tavaliselt kinnitatakse molübdeen oksiidkandjale molübdaadi (MoO 4 2–) või fosfomolübdaadiiooni (H 4 3–) kujul. Kogunenud tütarisotoop elueeritakse soolalahusega (nukleaarmeditsiinis kasutatavatest generaatoritest) või lahjendatud happelahustega. Ekstraheerimisgeneraatorite valmistamiseks lahustatakse kiiritatud sihtmärk kaaliumhüdroksiidi või karbonaadi vesilahuses. Pärast ekstraheerimist metüületüülketooni või muu ainega eemaldatakse ekstraktant aurustamisega ja järelejäänud pertehnetaat lahustatakse vees. Sublimatsioonigeneraatorite toime põhineb molübdeeni ja tehneetsiumi kõrgemate oksiidide lenduvuse suurel erinevusel. Kui kuumutatud kandevgaas (hapnik) läbib 700–800°C kuumutatud molübdeentrioksiidi kihi, viiakse aurustunud tehneetsiumheptoksiid seadme külma ossa, kus see kondenseerub. Igal generaatoritüübil on oma iseloomulikud eelised ja puudused, seetõttu toodetakse kõiki ülaltoodud tüüpi generaatoreid.
Lihtne aine.
Tehneetsiumi põhilisi füüsikalis-keemilisi omadusi uuriti isotoobil massinumbriga 99. Tehneetsium on hõbehalli värvi plastiline paramagnetiline metall. Sulamistemperatuur umbes 2150°C, keemistemperatuur »4700°C, tihedus 11,487 g/cm3. Tehneetsiumil on kuusnurkne kristallvõre ja alla 150 Å paksuste kilede puhul on sellel näokeskne kuupvõre. Temperatuuril 8K muutub tehneetsium II tüüpi ülijuhiks ().
Metallilise tehneetsiumi keemiline aktiivsus on lähedane selle alarühma naabri reeniumi aktiivsusele ja sõltub jahvatusastmest. Seega tuhmub kompaktne tehneetsium aeglaselt niiskes õhus ja ei muutu kuivas õhus, samal ajal kui pulbriline tehneetsium oksüdeerub kiiresti kõrgemaks oksiidiks:
4Tc + 7O 2 = 2Tc 2 O 7
Tehneetsium reageerib kergelt kuumutamisel väävli ja halogeenidega, moodustades ühendeid oksüdatsiooniastmega +4 ja +6:
Tc + 3F 2 = TcF 6 (kuldkollane)
Tc + 3Cl 2 = TcCl 6 (tumeroheline)
Tc + 2Cl 2 = TcCl 4 (punakaspruun)
ja 700 ° C juures interakteerub süsinikuga, moodustades TcC karbiidi. Tehneetsium lahustub oksüdeerivates hapetes (lämmastik- ja kontsentreeritud väävelhape), broomvees ja vesinikperoksiidis:
Tc + 7HNO3 = HTcO4 + 7NO2 + 3H2O
Tc + 7Br2 + 4H2O = HTcO4 + 7HBr
Tehneetsiumiühendid.
Hepvalentse ja neljavalentse tehneetsiumi ühendid pakuvad suurimat praktilist huvi.
Tehneetsiumdioksiid TcO 2 on oluline ühend kõrge puhtusastmega tehneetsiumi saamise tehnoloogilises skeemis. TcO 2 on must pulber tihedusega 6,9 g/cm 3, toatemperatuuril õhus stabiilne, sublimeerub temperatuuril 900–1100° C. Kuumutamisel temperatuurini 300° C reageerib tehneetsiumdioksiid intensiivselt õhuhapnikuga (moodustab Tc 2 O 7), fluori, kloori ja broomiga (koos oksohaliidide moodustumisega). Neutraalsetes ja aluselistes vesilahustes oksüdeerub see kergesti tehneethappeks või selle sooladeks.
4TcO2 + 3O2 + 2H2O = 4HTcO4
Tehneetsium(VII)oksiid Tc 2O 7 – kollakasoranž kristalne aine, vees kergesti lahustuv, moodustades värvitu tehnihappe lahuse:
Tc2O7 + H2O = 2HTcO4
Sulamistemperatuur 119,5° C, keemistemperatuur 310,5° C. Tc 2 O 7 on tugev oksüdeerija ja taandub kergesti isegi orgaaniliste ainete aurudega. Toimib tehneetsiumiühendite valmistamise lähteainena.
Ammooniumpertehnetaat NH 4TCO 4 – värvitu, vees lahustuv aine, vaheprodukt metalltehneetsiumi valmistamisel.
Tehneetsium(VII)sulfiid- tumepruuni värvi raskesti lahustuv aine, tehneetsiumi puhastamise vaheühend, mis kuumutamisel laguneb, moodustades disulfiidi TcS 2. Tehneetsium (VII) sulfiid saadakse vesiniksulfiidiga sadestamisel heptavalentsete tehneetsiumiühendite happelistest lahustest:
2NH4TcO4 + 8H2S = Tc2S7 + (NH4)2S + 8H2O
Tehneetsiumi ja selle ühendite kasutamine. Tehneetsiumi stabiilsete isotoopide puudumine takistab ühelt poolt selle laialdast kasutamist ja teisalt avab sellele uusi horisonte.
Korrosioon põhjustab inimkonnale tohutut kahju, "süües" kuni 10% kogu sulatatud rauast. Kuigi roostevaba terase valmistamise retseptid on teada, ei ole selle kasutamine majanduslikel ja tehnilistel põhjustel alati soovitatav. Mõned kemikaalid – inhibiitorid, mis muudavad metallpinna korrodeerivate ainete suhtes inertseks, aitavad kaitsta terast roostetamise eest. 1955. aastal tegi Cartledge kindlaks tehniliste hapete soolade ülikõrge passiveerimisvõime. Edasised uuringud on näidanud, et pertehnetaadid on raua ja süsinikterase kõige tõhusamad korrosiooniinhibiitorid. Nende toime avaldub juba kontsentratsioonil 10 –4 –10 –5 mol/l ja püsib kuni 250° C. Tehneetsiumiühendite kasutamine terase kaitseks on piiratud suletud tehnoloogiliste süsteemidega, et vältida radionukliidide sattumist keskkond. Tänu oma kõrgele vastupidavusele g-radiolüüsile on tehneethappe soolad aga suurepärased korrosiooni ennetamiseks vesijahutusega tuumareaktorites.
Paljud tehneetsiumi kasutusalad on tingitud selle radioaktiivsusest. Seega kasutatakse 99 Tc isotoopi standardsete b-kiirgusallikate valmistamiseks vigade tuvastamiseks, gaasi ioniseerimiseks ja standardsete standardite tootmiseks. Tänu oma pikale poolestusajale (212 tuhat aastat) võivad nad töötada väga pikka aega ilma aktiivsuse olulise vähenemiseta. Nüüd on 99m Tc isotoop tuumameditsiinis juhtival kohal. Tehneetsium-99m on lühiealine isotoop (poolväärtusaeg 6 tundi). Isomeerse ülemineku ajal 99 Tc-le kiirgab see ainult g-kiiri, mis tagab piisava läbitungimisvõime ja oluliselt väiksema patsiendidoosi võrreldes teiste isotoopidega. Pertehnetaadi ioonil puudub teatud rakkude suhtes väljendunud selektiivsus, mis võimaldab seda kasutada enamiku elundite kahjustuste diagnoosimiseks. Tehneetsium eritub organismist väga kiiresti (ühe päeva jooksul), seega võimaldab 99m Tc kasutamine lühikeste ajavahemike järel korduvalt uurida sama objekti, vältides selle ülekiiritamist.
Juri Krutjakov
Riigieelarveline õppeasutus
Erialane kõrgharidus
"Siberi Riiklik Meditsiiniülikool"
Tervise- ja sotsiaalarengu ministeerium
Farmaatsiateaduskond
Farmatseutilise keemia osakond
Ondar Ainara Demjanovna
Tehneetsium 99 – sisaldab radiofarmatseutilisi aineid. Analüüsi ja rakenduse omadused
Kursuse töö
IV kursuse üliõpilane
_______ A. D. Ondar
Õpetaja
_______ M. S. Larkina
Tomsk - 2012
Sisu:
Sissejuhatus………………………………………………………………………… 3-4
- Radioaktiivsed ravimid…………………………………………………………5-7
Tehneetsium-99 sisaldavad radiofarmatseutilised preparaadid…8
- Tehneetsiumi avastamise ajalugu……………………………………8-10
- Tehneetsium-99m saamise meetodid ja tehnoloogiad……………..11-12
- Kromatograafilised generaatorid tehneetsium-99m…………..12-13
Tehneetsium-99m sublimatsioonigeneraatorid…………………….14
Ekstraheerimistoodang 99m Ts………………………………15-16
- Tehneetsium-99 baasil valmistatud preparaadid. Analüüs ja rakendamine…………….17-22
- Radiofarmatseutiliste preparaatide analüüsi üldmeetodid.23-33
- Ettevalmistused Tehneetsium-99………………………………………………………………………………………………………………………
- Tehneetsiumi (99 Ts) kolloidse reeniumsulfiidi süstimine……..34-36
Tehneetsiumi (99 Ts) kolloidse väävli süstimine………………..37-39
Tehneetsiumi (99 Tc) kolloidse tina süstimine…………………..40-42
Tehneetsiumi (99 Tc) etüfeniini süstimine…………………………….43-46
Tehneetsiumi (99 Tc) eksametazüümi süstimine……………………….47-50
Tehneetsium (99 Tc) glükonaadi süstimine………………………………51-53
Viited…………………………………………………………………………… 56-57
Sissejuhatus.
Edusammud aatomituumafüüsika vallas avaldavad väga suurt mõju peaaegu kõigi inimteadmiste harude arengule. Aatomienergia valdamine on andnud väga erinevate erialade teadlastele uusi teadusliku uurimistöö vahendeid ja meetodeid. Teaduslike teadmiste võimalused on mõõtmatult suurenenud. Alates selle loomisest on teaduslik meditsiin füüsikast ja keemiast ammutanud uusi ideid ja vahendeid haiguste ennetamiseks ja nende vastu võitlemiseks. See teadusharu on rikastatud uute, väga väärtuslike meetoditega eluprotsesside uurimiseks, haiguste diagnoosimiseks ja raviks.
Meditsiinifüüsika on teadus süsteemist, mis koosneb füüsilistest seadmetest ja kiirgusest, meditsiini- ja diagnostikaseadmetest ja tehnoloogiatest.
Meditsiinifüüsika eesmärk on nende süsteemide uurimine haiguste ennetamiseks ja diagnoosimiseks, samuti patsientide ravimiseks füüsika, matemaatika ja tehnoloogia meetodite ja vahenditega. Haiguste olemusel ja taastumismehhanismil on paljudel juhtudel biofüüsiline seletus.
Õigeaegse ja täpse diagnoosi probleem jääb 21. sajandi kliinilise meditsiini üheks peamiseks probleemiks. Erinevate elundite ja kudede kliiniliste ja instrumentaalsete diagnostikavahendite kompleksis on üks juhtivaid kohti radionukleotiidide (radioisotoopide) uurimismeetoditel. (1)
Tänu radionukleotiidide mitmekesisusele ja suurele hulgale isotoopi sihtorganisse toimetavatele „sõidukitele“ on tänapäeval võimalik uurida mis tahes kehasüsteeme.
Radiofarmatseutilisi preparaate kasutav diagnostika võimaldab avastada elundite talitlushäireid palju varem kui teiste diagnostiliste testidega (röntgen, kompuutertomograafia ja tuumamagnetresonantstomograafia, ultraheli) tuvastatud anatoomilised muutused. Selline varajane diagnoosimine võimaldab varajast ravi siis, kui see on kõige tõhusam ja võimalik soodne prognoos, mis on eriti oluline onkoloogiliste, südame- ja neuroloogiliste haiguste puhul.
- Radioaktiivsed ravimid.
Radioaktiivsed ravimid jagunevad:
- Suletud radiofarmatseutilised preparaadid;
- Avatud radiofarmatseutilised preparaadid.
Diagnostilistel eesmärkidel kasutatakse radioisotoope, mis organismi sattudes osalevad uuritavates ainevahetustüüpides või uuritavate elundite ja süsteemide aktiivsuses ning on samal ajal registreeritavad radiomeetriliste meetoditega. Sellistel radioaktiivsetel ravimitel on reeglina lühike efektiivne poolväärtusaeg, mille tulemuseks on katsealuse keha ebaoluline kokkupuude kiirgusega.
Pahaloomuliste kasvajate kiiritusravis kasutatavate radioaktiivsete ravimite valimise kriteeriumiks on võime luua kasvaja piirkonnas vajalik ioniseeriva kiirguse terapeutiline annus minimaalse mõjuga ümbritsevale tervele koele. See efekt saavutatakse radiofarmatseutiliste preparaatide kasutamisega erinevates agregatsiooniseisundites ja kehasse viimise viisides (lahused, suspensioonid, graanulid, nõelad, traat, pealekandmissidemed jne) ning kasutades selleks kõige sobivamaid isotoope, mis on seotud nende tüübi ja energiaga. kiirgust.
Rohkem kui 50% maailma radionukliidide aastatoodangust kulutatakse selle vajadustele. Nagu teate, sisaldab elusorganism lisaks 5 põhielemendile (hapnik, vesinik, süsinik, lämmastik ja kaltsium) veel 67 Mendelejevi perioodilisuse tabeli elementi. Seetõttu on praegu raske ette kujutada kliinikut siin või välismaal, kus ei kasutataks erinevaid radioaktiivseid ravimeid ja nendega märgistatud ühendeid haiguse diagnoosimiseks. Radionukliide kasutatakse tuumameditsiinis peamiselt radiofarmatseutiliste ainetena erinevate inimorganite haiguste varajaseks diagnoosimiseks ja ravieesmärkidel. Diagnostiliste radiofarmatseutiliste ravimite eripäraks on farmakoloogilise toime puudumine. Kiiritus meditsiinis on suunatud patsiendi tervendamisele. Siiski on annused sageli ebamõistlikult suured. Patsient peab uuringu ajal saama minimaalse annuse. Sellega seoses on radiofarmatseutiliste ravimite arendajate üks olulisemaid ülesandeid patsientide kiirgusdooside vähendamine erinevate radionukliide kasutavate uuringute käigus, see tähendab selliste radionukliidide ja nendega märgistatud ühendite väljavalimine, mille kasutamine võimaldab saada. vajalik diagnostiline teave võimalikult väikese kiirgusdoosiga patsientidele.
Radionukliide on meditsiinilistel eesmärkidel süstemaatiliselt kasutatud alates 40ndate algusest. Just siis kehtestati kilpnäärme erinevates patoloogilistes seisundites radioaktiivse joodi range jaotumise muster. Järgnevalt võimaldas radioaktiivsete nukliididega märgistatud ühendite kasutamine määrata primaarsete kasvajate asukohta ja suurust, tuvastada kasvajaprotsesside levikut ning jälgida medikamentoosse ravi efektiivsust. Tänu suurele hulgale radionukliididele ja nendega märgistatud ravimitele on tänapäeval võimalik uurida peaaegu kõiki inimkeha füsioloogilisi ja morfoloogilisi süsteeme: südame-veresoonkonna ja vereloome, uriini- ja vee-soolade ainevahetust, hingamis- ja seedesüsteemi, luu- ja lümfisüsteemi jne. .
- Tehneetsium 99 sisaldavad radiofarmatseutilised preparaadid.
Ühendites on tehneetsiumi oksüdatsiooniaste vahemikus 0 kuni +7, kõige stabiilsem on heptavalentne olek.
- Tehneetsiumi avastamise ajalugu.
1920. aastatel alustas grupp saksa teadlasi professor Walter Noddacki juhtimisel ekamangaani otsimist, kuid see ei õnnestunud.
Pärast Noddaki grupi otsingute ebaõnnestumist kadus lootus sellist isotoopi leida praktiliselt. Tehneetsiumi stabiilseima isotoobi poolestusaeg on praegu teadaolevalt 2,6 miljonit aastat, seega oli elemendi nr 43 omaduste uurimiseks vaja see uuesti luua. Noor itaalia füüsik Emilio Gino Segre võttis selle ülesande 1936. aastal. Aatomite kunstliku tootmise põhimõttelist võimalust demonstreeris 1919. aastal suur inglise füüsik Ernest Rutherford.
Pärast Rooma ülikooli lõpetamist juhtis ta Palermo ülikooli füüsikaosakonda. Laboratoorium, kus ta töötas, oli väga tagasihoidlik ega soodustanud teaduslikke saavutusi. 1936. aastal läks ta ärireisile USA-sse Berkeleysse, kus tuli ideele analüüsida molübdeeniplaati, mis aitas kõrvale tõrjuda vesiniku raske isotoobi deuteeriumi tuumade kiirt. "Meil oli põhjust arvata," kirjutas Serge, "et molübdeen peaks pärast deuteroonidega pommitamist muutuma elemendiks number 43..." Tõepoolest, molübdeeni aatomi tuumas on 42 prootonit ja 1 prootonit. deuteeriumi tuum.ühenda, siis saadakse 43. elemendi tuum. Looduslik molübdeen koosneb kuuest isotoobist, mis tähendab, et kiiritatud plaadis võib olla mitu uue elemendi isotoopi.
30. jaanuaril 1937 alustasid Palermos tööd Emilio Serge ja mineraloog Carlo Perrier. Esialgu tegid nad kindlaks, et toodud molübdeeniproov eraldub? - osakesed, mis tähendab, et radioaktiivsed isotoobid olid selles tõesti olemas, kuid kas element nr 43 oli nende hulgas, kuna tuvastatud kiirguse allikad võisid olla tsirkooniumi, nioobiumi, ruteeniumi, reeniumi, fosfori ja molübdeeni enda isotoobid? Sellele küsimusele vastamiseks lahustati osa kiiritatud molübdeenist vees (vesinikkloriid- ja lämmastikhappe segu) ning radioaktiivne fosfor, nioobium ja tsirkoonium eemaldati keemiliselt ning seejärel sadestati välja molübdeensulfiid. Ülejäänud lahus oli endiselt radioaktiivne, sisaldades reeniumi ja võib-olla elementi nr 43. Nüüd jäi alles kõige keerulisem – eraldada need kaks sarnaste omadustega elementi. Serge ja Perrier said selle ülesandega hakkama. Nad leidsid, et kui reeniumsulfiid sadestatakse kontsentreeritud vesinikkloriidhappe lahusest vesiniksulfiidiga, jäi osa aktiivsusest lahusesse. Pärast ruteeniumi ja mangaani isotoopide eraldamise kontrollkatseid sai selgeks, et? – osakesi saavad emiteerida ainult uue elemendi aatomid, mida kreekakeelsest sõnast nimetati tehneetsiumiks??????? - "kunstlik". See nimi kinnitati lõpuks 1949. aasta septembris Amsterdamis toimunud keemikute kongressil. Kogu töö kestis üle nelja kuu ja lõppes 1937. aastal ning tulemuseks oli vaid 10–10 grammi tehneetsiumi.
Kuigi Serge'il ja Perrier'l oli käes ebaoluline kogus elementi nr 43, suutsid nad siiski kindlaks teha osa selle keemilistest omadustest ning kinnitasid perioodilise seaduse alusel ennustatud tehneetsiumi ja reeniumi sarnasust. On selge, et nad tahtsid uue elemendi kohta rohkem teada saada, kuid selle uurimiseks vajasid nad tehneetsiumi massi ja kiiritatud molübdeen sisaldas liiga vähe tehneetsiumi, mistõttu tuli leida sobivam kandidaat selle elemendi tarnimiseks. Tema otsinguid kroonis edu 1939. aastal, kui O. Hahn ja F. Strassmann avastasid, et uraan-235 lõhustumisel tuumareaktoris neutronite mõjul tekkinud "fragmendid" sisaldasid üsna märkimisväärses koguses pikaealist isotoopi. 99 Tc. Järgmisel aastal suutsid Emilio Serge ja tema kaastöötaja Wu Jianxiong selle puhtal kujul isoleerida. Iga kilogrammi selliste "fragmentide" kohta on kuni kümneid gramme tehneetsium-99.
- Tehneetsium-99m saamise meetodid ja tehnoloogiad.
Suur nõudlus 99m Tc järele on tingitud suhteliselt lühikesest poolestusajast (6,02 tundi) ja madalast gammakiirguse energiast (0,1405 MeV), mis tagab madala ekspositsioonidoosi (0,5–5% lubatud tasemest) ja samal ajal piisava läbitungimisvõime. radiomeetriliste mõõtmiste jaoks. Lisaks võimaldavad 99m Tc keemilised omadused saada erinevaid meditsiinis kasutatavaid lihtsaid ja keerulisi kompleksühendeid.
Tehneetsium-99m moodustub molübdeen-99 b-lagunemise tulemusena vastavalt skeemile:
Sel juhul muundatakse 87,5% 99 Mo tuumast 99m Tc-ks ja 12,5% 99 Tc-ks, millele järgneb nende üleminek stabiilseks ruteeniumiks.
Generaatoripaari 99 Mo/99m Tc puhul on täidetud järgmised seosed:
, (1)
, (2)
kus N1, N2 ja A1, A2 on tuumade arv ja aktiivsus vastavalt 99 Mo ja 99m Tc; l 1 ja l 2 – lagunemiskonstandid 99 Mo ja 99m Tc; t – lagunemisaeg; (A 1) 0 – algaktiivsus 99 Mo. Maksimaalse akumulatsiooni 99m Тс kestus sellises süsteemis on tmax = 22,89 tundi, mis määrab selle lähteisotoobist eraldumise perioodilisuse.
99m Tc eraldamiseks 99 Mo-st kasutatakse spetsiaalseid seadmeid, mida nimetatakse tehneetsiumi generaatoriteks. Kasutatava eraldusmeetodi alusel jaotatakse generaatorid kolme põhitüüpi: sorptsioon (kromatograafiline), sublimatsioon ja ekstraheerimine.
- Tehneetsium-99m kromatograafilised generaatorid.
Kromatograafilise generaatori töötas välja Tucker D. 1958. aastal. See koosneb kromatograafilisest kolonnist, mis on täidetud sorbendi või ioonivahetusvaiguga, millega on ühendatud eluendi varustamiseks ja eluaadi kogumiseks mõeldud sidekanalid ning mis asetatakse kaitsemahutisse (joonis 1). . 1).
Riis. 1. Tehneetsium-99m kromatograafilise generaatori skeem:
1 – veerg; 2 – kiirguskaitse; 3 – generaatori korpus; 4 – eluendi liin; 5 – eluaadi liin; 6 – kaitsekork; 7 – filter; 8 – generaatori äärik; 9 – pudel eluendiga; 10 – kaitsev meditsiiniline konteiner evakueeritud pudeliga
Kolonn on "laetud" lahusega, mis sisaldab molübdeen-99. Järgnev 99m Tc eraldamine (elueerimine) sellest naatriumpertehnetaadi, 99m Tc lahuse kujul viiakse läbi füsioloogilise lahuse pumbamisega läbi kolonni.
Kromatograafiageneraatori jõudlusnäitajad sõltuvad järgmistest peamistest teguritest:
- paigalduse disainifunktsioonid;
sorbeeritud vormi koostis - 99 Mo sisaldav lahus;
sorbendi olemus ja struktuur, selle valmistamise tehnoloogia;
elueerimislahuse koostis ja elueerimistehnika.
- Tehneetsium-99m sublimatsioonigeneraatorid
Üks esimesi tööstuslikke sublimatsioonigeneraatoreid, mis toodab 99 m Tc, töötati välja Austraalias Lucas Heightsis. Eraldamine viidi läbi horisontaalse ahjuga paigaldises hapnikuvoolus temperatuuril 850 °C. Sihtmärgiks oli molübdeenanhüdriid. See paigaldus võimaldas saada kuni 75 Ci 99m Tc 20 ml mahus füsioloogilises lahuses madala aktiivsusega 99 Mo (1 Ci/g), mis kaalub 200 g. Tehneetsiumi saagis ei ületanud 20–40%. Hilisemad uuringud näitasid, et 99m Tc saagis suureneb sublimatsiooniaja pikenedes ja väheneb sihtmassi suurenemisega. Seda tähelepanekut kasutades töötas Colombetti L. J. välja väikese generaatori, mille toiteallikaks on 99 Mo, lagunemissaadus, kliiniliste laborite jaoks. Selle tehase eraldamise efektiivsus oli 70–80%.
Eraldatud 99m Tc radiokeemiline vorm kõrgel temperatuuril ja hapniku juuresolekul vastab Tc(VII) pertehnetaadile. Sublimatsiooni paigaldamise lihtsus ja muude reaktiivide, eriti orgaaniliste reaktiivide kasutamise vajaduse puudumine selles protsessis vähendab kromatograafilisele tehnoloogiale omaste 99m Tc redutseeritud või komplekssete vormide moodustumise tõenäosust. Sublimatsioonimeetodi peamiseks puuduseks on 99m Tc vabanemise madalam efektiivsus võrreldes kõigi teiste praegu kasutatavate meetoditega.
- Ekstraheerimistoodang 99 m Tf.
Traditsiooniline tehnoloogiline skeem 99m Тс kaevandamise tootmiseks sisaldab järgmisi põhitoiminguid:
- kiiritatud 99 Mo sihtmärgi lahustamine KOH või NaOH lahuses oksüdeerivate ainete (H 2 O 2, NaOCl) juuresolekul, millele järgneb K 2 CO 3 lisamine saadud lahusesse väljasoolavana;
ekstraheerimine 99m Тс orgaanilise ekstraktandiga;
ekstraktandi destilleerimine ja 99m Tc-d sisaldava kuiva jäägi lahustamine füsioloogilises lahuses.
Ekstraheerimisgeneraatori tööpõhimõtet saab illustreerida joonisel fig. 2. Seade koosneb segistiga ekstraktorist (1), millesse juhitakse 99 Mo algne leeliselahus ja ekstraktor. Ekstraheerimisgeneraatori tööpõhimõtet saab illustreerida joonisel fig. 2.
Joonis 2. Tehneetsium-99m ekstraheerimisgeneraatori skeem mehaanilise faasisegamisega.
Ekstraheerimisgeneraatori tööpõhimõtet saab illustreerida joonisel fig. 2. Seade koosneb segistiga ekstraktorist (1), millesse juhitakse 99 Mo algne leeliselahus ja ekstraktor. Pärast segu segamist ja orgaanilise faasi eraldamist viiakse see sisselasketoru abil aurustisse (2), mille ots asub faasiliidese kohal. Ekstraktant destilleeritakse aurustisse (3).
Üldjuhul sõltub ekstraheerimisgeneraatori 99m Tc saagis ekstraheerimisprotsessi efektiivsusest ja 99m Tc-ga ekstrakti kao suurusest selle valikul. Ekstraheerimise efektiivsus sõltub jaotuskoefitsiendist 99m Тс vesi-orgaanilise faasi süsteemis, segamise intensiivsusest ja faaside kokkupuuteajast. Kadude vähendamise probleem lahendatakse peamiselt ekstraktori diameetri kitsendamisega valikualal ja andurite abil ekstraktsioonitaseme juhtimiseks. Madala kadude taseme tagavad ka tsentrifugaalekstraktorid (NPO Radium Institute).
- Tehneetsium-99 baasil valmistatud preparaadid. Analüüs ja rakendamine.
Tuleb märkida, et tehneetsium-99m preparaat, mis saadakse otse mis tahes konstruktsiooniga generaatoritest, on 0,9% naatriumkloriidi lahus, mis sisaldab 99m Tc naatriumpertehnetaadi Na 99m TcO 4 kujul, kus enam kui 99% tehneetsiumi aatomitest on kõrgeim oksüdatsiooniaste (VII ). Ravimi diagnostiline kasutamine selles keemilises vormis piirdub kilpnäärme ja süljenäärmete stsintigraafiaga. Seetõttu segatakse praktikas mitmesuguste 99m Tc radiofarmatseutiliste preparaatide saamiseks esmane naatriumpertehnetaadi lahus spetsiaalsete reaktiivide komplektidega, mille tulemusena moodustuvad mitmesugused 99m Tc kompleksühendid, mis on teatud uuritavate elundite suhtes selektiivsed. Kuna 99m Tc (VII) ise ei ole kompleksi moodustumisele kalduv, viiakse see esmalt üle madalamasse oksüdatsiooniastmesse (+IV või +V), mis hõlbustab erinevate agregeeritud struktuuride teket metall-metall sidemetega, oksoühenditega jne.
Pertehnetaadi vähendamiseks kasutatakse erinevaid redutseerivaid aineid, millest enim kasutatakse kahevalentset tina (SnCl 2). Mõnel juhul toimub tehneetsiumi redutseerimise protsess järk-järgult 5-valentse tehneetsiumi vaheühendite moodustumisega, mida saab seejärel redutseerida kolme- või monovalentsesse olekusse. 99m Tc radiofarmatseutiliste preparaatide saamise protsessi Sn 2+ ioonide juuresolekul saab ligikaudselt iseloomustada järgmise skeemi abil:
Siin on L aine tehneetsiumiga märgistamiseks.
Tabel 1.
Diagnostilistes uuringutes kasutatavad tehneetsium-99m radiofarmatseutilised preparaadid
| Märgistatud osakesed |
|
| 99 m Tc-albumiini makroagregaadid, 10–50 µm (Macrotech) |
kopsuperfusioon |
| 99m Tc-DTPA, aerosool 1–4 µm |
ventilatsioon |
| 99m Tc-väävelkolloid, 0,1–1,0 µm |
maks, põrn, luuüdi |
| 99m Tc-SC, filtreeritud, 0,1–0,3 µm |
lümfikollektorid, rinnavähk (BC), melanoom |
| 99m Tc-HAS (nanokolloid) 0,02 µm |
sentinell-lümfisõlmed, rinnavähk, melanoom |
Radioaktiivsed gaasid |
|
| 99m Tc-technegas, 0,004–0,25 µm |
Ventilatsioon |
Märgistatud kelaadid |
|
| 99m Tc-MDP, HDP |
kasvajate metastaasid luudesse, osteo- sarkoom, neuroblastoom |
| 99m Tc-DTPA |
ajukasvajad, neerude verevool ja neerustsintigraafia |
| 99m Tc-MAG3 |
neeru stsintigraafia |
| 99m Tc-DMSA |
Neeru stsintigraafia, medullaarne kilpnäärme kartsinoom |
| 99m Tc-Ceretec (HMPAO) |
aju perfusioon |
| 99m Tc-Sestamibi ja tetrafosmiin (Technetril) |
müokardi perfusioon, rinnavähk, ajukasvajad |
Radionukliididega märgistatud vererakud |
|
| 99m Tc-erütrotsüüdid |
väljutusfraktsioon, hemangioomi äratundmine ja seedetrakti verejooks |
| Radiofarmatseutilised ained retseptoritega seondumiseks |
|
| 99m Tc-P829, Neotec |
pahaloomulised kopsukasvajad, neuroendokriinsed kasvajad |
| 99m Tc-P280, Acutect |
verehüüvete visualiseerimine, süvaveenide tromboosi diagnoosimine |
| 99m Tc-disofeniin ja Choletec |
hepatobilistsintigraafia |
Märgistatud monoklonaalsed antikehad |
|
| 99m Tc-CEA-Scan, IMMU = 4Fab ' |
jämesoole pahaloomulised kasvajad |
| 99 m Tc-Verluma, NR-LU-10-Fab |
pahaloomuline kopsukasvaja |
Tehneetsiumi radiofarmatseutiliste preparaatide valmistamiseks kliinikutes kasutatavad reaktiivikomplektid sisaldavad tavaliselt mõõdetud koguseid redutseerivat ainet ja kompleksi moodustavaid (või kolloidseid) aineid. Mõnel juhul sisaldavad reaktiivid puhvrit või stabiliseerivaid lisandeid. Tavaliselt on selliste standardkomplektide kõlblikkusaeg 6–12 kuud, kui on täidetud sobivad säilitustingimused.
Venemaal on tehneetsium-99m generaatorite reaktiivikomplektide peamine tootja föderaalvalitsuse Medbioextremi osariigi ühtse ettevõtte Medradiopreparati tehas. Välismaal toodavad sarnaseid tooteid firmad “Amercham”, “Malincrodt” jne. Tänapäeval toodetakse Venemaal radiofarmatseutiliste preparaatide 99m Tc valmistamiseks järgmisi reaktiivide komplekte:
- Pentatekh, 99 m Tc-kompleks pentatsiiniga (CaNO 3 - DTPA sool) neerude glomerulaarfiltratsiooni määra määramiseks, neerude gamma-stsintigraafia, radionukliidangiograafia ja ajukasvajate visualiseerimine.
Pirfotech, 99 m Tc-kompleks pürofosfaadiga skeletistsintigraafia, ägeda müokardiinfarkti, pahaloomuliste munasarjakasvajate jaoks, erütrotsüütide in vivo märgistamiseks.
Citratekh, 99 m Tc-kompleks tsitraadiga neerude stsintigraafia ja radionukliidangiograafia jaoks.
Koren, 99 m Tc-kolloidne reeniumsulfiidil põhinev lahus maksa, põrna ja luuüdi stsintigraafiaks.
Technefor, 99 m Tc-kompleks oksabiforiga (oksa-bis(etüleennitrilo)tetrametüleenfosfoonhape) skeleti stsintigraafia jaoks.
Technefit, 99 m Tc-fütaadi kolloidlahus maksa, põrna ja luuüdi stsingigraafiaks.
Technemek, 99 m Tc-kompleks dimerkaptosuktsiinhappega neerude stsingigraafiaks (skaneerimiseks).
Bromesiid, 99 m Tc-kompleks koos Br-3-metüülfenüülkarbamoüüliminoäädikhappega maksa, sapipõie ja sapiteede dünaamiliseks stsintigraafiaks.
Technetril, 99 m Tc-kompleks metoksüisobutüülisonitriiliga müokardi perfusiooni ja kasvaja kuvamise uurimiseks.
Technemag, 99 m Tc-kompleks merkaptoatsetüültriglütseriiniga neerude dünaamilise stsintigraafia jaoks.
Teoksiim, 99 m Tc-kompleks heksametüleenpropüleenamiinoksiimiga aju perfusiooni uurimiseks.
Carbomek, 99 m Tc-kompleks Tc(V) dimerkaptosuktsiinhappega medullaarse kilpnäärmevähi, lümfoomide ja muude kasvajate diagnoosimiseks.
Macrotech, 99 m Tc-albumiini makroagregaadid visualiseerimiseks
kopsud.
Tänapäeval kaalutakse kolme peamist võimalust sihtotstarbeliste radiofarmatseutiliste preparaatide saamiseks. Niinimetatud integreeritud lähenemine hõlmab tehneetsium-99m kunstliku kelaadi loomist koos retseptori ligandi lisamisega selle koostisse minimaalse suuruse muutusega ja ligandi spetsiifilisuse säilitamisega. Reeglina väheneb selle lähenemisviisiga märgistatud ühendi retseptoriga seondumise efektiivsus märgistamata retseptoritega märgatavalt. Teise võimalusena pakutakse välja bifunktsionaalne lähenemine, mis hõlmab pH-kelaadi lisamist kõrge spetsiifilisusega retseptori ligandile. Samuti pakutakse välja kombineeritud lähenemine, mis seisneb suurenenud retseptoriga seondumisega makrotsüklilise metallopeptiidi saamises, mis sisaldab N4, N3S või doonorrühma N2S2.
- Radiofarmatseutiliste preparaatide analüüsi üldmeetodid.
- Füsioloogiline (bioloogiline) jaotus
Üldiselt viiakse test läbi järgmiselt.
Kõigile kolmele loomale manustatakse uuritavat ravimit intravenoosselt. Kui see on oluline, siis FSP näitab: looma tüüp, sugu, tõug ja kaal ja/või vanus. Uuritavate radiofarmatseutiliste preparaatide süstimine vastab kliinilisele (keemilise koostise poolest). Vajadusel lahustatakse toode vastavalt tootja juhistele. Mõnel juhul on vaja ravimit vahetult enne manustamist lahjendada.
Manustamiseks kasutatakse tavaliselt intravenoosset teed sabaveeni. Valitud juhtudel võib kasutada ka teisi veene, nagu reieluu-, kägi- või peeniseveen, või muid manustamisviise. Loomad, kellel täheldatakse ravimi eemaldamist veresoontest kudedesse (süstimise ajal või tuvastatakse pärast koe aktiivsuse mõõtmist), lükatakse katsest välja. Kohe pärast manustamist paigutatakse iga loom eraldi puuri, mis võimaldab koguda väljaheiteid (looma kehapinna saastumine ei ole lubatud).
Teatud ajal pärast süstimist loomad teatud viisil surmatakse ja tükeldatakse. Valitud elundite ja kudede aktiivsust mõõdetakse vastava aparaadiga, mida kirjeldatakse privaatses FSP-s. Seejärel arvutatakse bioloogiline jaotus, väljendades aktiivsuse akumuleerumise protsenti igas valitud elundis ja koes. Selleks saab elundi aktiivsust seostada süstitud aktiivsusega, mis arvutatakse standardse või süstla sisu mõõtmise teel enne ja pärast süstimist. Mõne radiomärgistusaine puhul võib olla sobivam määrata valitud koe kaalutud proovi aktiivsus (aktiivsus/mass).
Ravim vastab testi nõuetele, kui aktiivsuse jaotus vähemalt kahel loomal kolmest vastab kehtestatud kriteeriumidele.
- Autentimine radionukliidi abil
Radionukliidi autentsuse kontrollimiseks kasutatakse iga spektri kuju ja kvantitatiivseid omadusi, samuti T 1/2 väärtust.
Rangelt reprodutseeritavates tingimustes võetud instrumentaalsed spektrid võivad olla ka radionukliidide individuaalsed omadused; neid kasutatakse kõikidel asjakohastel juhtudel radiofarmatseutiliste preparaatide radionukliidide tuvastamiseks.
Preparaadis sisalduva radionukliidi ehtsus loetakse kinnitatuks, kui antud radiofarmatseutilisest preparaadist valmistatud allikaga võetud ioniseeriva kiirguse instrumentaalne spekter on identne võrdlusallika või sama radionukliidi võrdluslahusest valmistatud allikaga saadud spektriga, ja võetakse samadel tingimustel. Loomulikult eeldatakse, et spektrit tuleks korrigeerida radionukliidide lisandite panuse suhtes, kui neid esineb radiofarmatseutilistes preparaatides.
Radionukliidide identifitseerimine toimub:
- spektri järgi (gamma-, beeta- ja röntgenkiirgus);
poolsummutuskihiga (beetakiirgus);
poolestusajaga (mis tahes kiirgus).
Spektromeetria
Gamma-spektromeetrit kasutatakse radionukliidide tuvastamiseks gamma- või röntgenikiirguse energia ja intensiivsuse järgi.
Germaaniumi pooljuhtdetektorit kasutatakse eelistatavalt gamma- ja röntgenspektromeetria jaoks.
Kasutatakse ka stsintillatsioonidetektorit - NaI-Tl, kuid sellel on madalam energialahutusvõime.
Gammadetektor kalibreeritakse standardsete allikate abil, kuna tuvastamise efektiivsus sõltub gamma- ja röntgenikiirguse energiast, samuti allika kujust ning detektori ja allika vahelisest kaugusest.
Seda omadust kasutatakse allikas leiduvate radionukliidide tuvastamiseks ja kvantifitseerimiseks, mis annab hinnangu radionukliidse lisandi olemasolule, tuvastades teisi oodatavatest piike.
- Pool summutuskiht
Antud radionukliidi d 1/2 tegeliku väärtuse määramiseks tehakse sarnased mõõtmised sama suuruse, kuju ja paksusega ning ligikaudu sama aktiivsusega allikaga, mis on valmistatud selle radionukliidi proovilahusest.
Pool elu
- Aktiivsuse mõõtmine
Kui radionukliidi lagunemismuster on teada, saab konkreetse proovi aktiivsust absoluutselt mõõta, kuid praktikas tuleb täpsete tulemuste saamiseks teha palju kohandusi. Seetõttu tehakse mõõtmised tavaliselt esmase standardallika abil.
Tegevustulemused näitavad erinevusi, mis on peamiselt tingitud harvaesinevast tuumatransformatsioonist. Ajaühikus toimuvate üleminekute arvu erinevuste kompenseerimiseks tuleb registreerida piisav arv impulsse. Näiteks on vaja vähemalt 10 000 impulssi, et saada suhteline standardhälve mitte üle 1% (usaldusvahemik: 1 sigma).
Kõik radioaktiivsuse mõõtmise tulemused esitatakse koos mõõtmise kuupäeva ja vajadusel kellaajaga. See märge tuleb teha, võttes arvesse ajavööndit (GMT, CET) (Greenwichi aeg, Kesk-Euroopa aeg). Radioaktiivsus muul ajal arvutatakse eksponentsiaalvõrrandi abil või määratakse tabelitest.
- Radionukliidide puhtuse ja radionukliidide lisandite määramine
Radiofarmatseutilises preparaadis sisalduvate radionukliidide erineva poolestusaja tõttu on radionukliidide puhtus aja jooksul erinev.
Radionukliidide analüüs hõlmab järgmisi etappe: radionukliidide lisandite tuvastamine ja aktiivsuse määramine. Tuvastatud lisandite aktiivsuse mõõtmine toimub sarnaselt punktis “Aktiivsuse mõõtmine” kirjeldatule, kasutades sobivaid beeta- ja gamma-loenduriga radiomeetrilisi seadmeid, spektromeetreid, juhuslikult aktiivsuse mõõtmise seadmeid ja muid seadmeid. Konkreetsed analüüsimeetodid üksikute radionukliidide lisandite jaoks on toodud vastavas privaatses FS-is või FSP-s nendel juhtudel, kui analüüsi saab teha ravimi säilivusaja jooksul.
Avastatud lisandi aktiivsus on antud protsendina preparaadis oleva peamise radionukliidi aktiivsusest teatud kuupäeval.
Radionukliidsed lisandid, mille aktiivsus ei ületa 0,01% peamise radionukliidi aktiivsusest kogu säilivusaja jooksul, ei ole eraviisilistes FSP-des loetletud, välja arvatud erijuhtudel, vaid viide kogu lisandi piiri kohta farmakopöa monograafia on kohustuslik.
- Radiokeemilise puhtuse ja radiokeemiliste lisandite määramine
- radionukliidide tootmine;
järgnevad keemilised operatsioonid;
mittetäielik ettevalmistav eraldamine;
ladustamisest tingitud keemilised muutused.
Kõige sagedamini kasutatakse õhukese kihi kromatograafiat ja paberkromatograafiat. Paber- ja õhekihikromatograafias kantakse proov, mille maht on FSP-s määratud, lähtejoonele, nagu on kirjeldatud üldistes kromatograafiameetodites. Eelistatav on analüüsiks preparaati mitte lahjendada, kuid väga oluline on vältida sellise aktiivsuse rakendamist, mis põhjustab kokkusattumuste tõttu mõõtmiskadusid. Seetõttu kasutatakse analüüsiks sellist kogust ravimit, et saaks statistiliselt usaldusväärseid mõõtmistulemusi nende lisandite puhul, mille aktiivsus on vähemalt 0,5% rakendatud kogusest. Samas peaks analüüsitava proovi aktiivsus olema selline, et salvestuspaigaldise surnud ajast tingitud valearvestuste parandus ei ületaks 1-2%.
Pärast eraldamist kromatogramm kuivatatakse ja radioaktiivsete tsoonide asukoht määratakse autoradiograafiaga või aktiivsuse mõõtmisega kromatogrammi pikkuses, kasutades sobivaid kollimeeritud loendureid või riba lõikamist ja riba iga lõigu aktiivsuse mõõtmist. . Täppide ja alade asukohta saab keemiliselt tuvastada, võrreldes sama kemikaali (mitteradioaktiivse) vastavate lahustega, kasutades sobivat tuvastamismeetodit.
- Komponendid
- Steriilsus
Tavaliselt peab radiofarmatseutiliste preparaatide puhul steriliseerimise jälgimine tagama ravimi steriilsuse ning steriilsuse testimine hõlmab iga kümnenda autoklaavitud ravimite partii (olenevalt steriliseerimisprotsessi valideerimisest) ja iga aseptilistes tingimustes valmistatud või kuivas kohas steriliseeritud ravimite partii testimist. kütta ahi.
- Parim enne kuupäev
- ravimi keemilise ja radiokeemilise koostise stabiilsus;
ravimi aktiivsuse vähenemine aja jooksul vastavalt radioaktiivse lagunemise seadusele;
pikaealiste radionukliidlisandite suhtelise sisalduse suurenemine, mille poolestusaeg on pikem kui peamisel radionukliidil.
tabel 2
Radiofarmatseutiliste ravimite kontrollimise sagedus nende säilivusaja määramisel
Lõigetes märgitud aegumiskuupäevaga ravimite puhul. 3 ja 4, esitage veel kord analüüsiandmed väljaspool nende piire. Ajavahemik aegumiskuupäevast käesoleva analüüsi kuupäevani on arendaja äranägemisel 10-50% säilivusajast.
- Säilitamine
Vajadusel näitab era-FSP ravimile konkreetsed säilitustingimused, mis tulenevad selle spetsiifilistest omadustest ja selle kvaliteedi säilimise tagamisest (temperatuuritingimused jne).
Ettevaatusabinõud
- Ettevalmistused Tehneetsium-99.
Rhenii sulfidi colloidalis et technetii (99mTc) solutio iniectabilis.
Definitsioon. Tehneetsium (99 Tc) kolloidne reeniumsulfiidi süstimine on tehneetsium-99m-ga märgistatud reeniumsulfiidmitsellide steriilne pürogeenivaba kolloidne dispersioon. See on stabiliseeritud želatiiniga. Süste sisaldab vähemalt 90,0% ja mitte rohkem kui 110,0% tehneetsium-99m deklareeritud radioaktiivsusest etiketil märgitud kuupäeval ja kellaajal. Vähemalt 92,0% radioaktiivsusest vastab tehneetsium-99m kolloidsel kujul. Süstelahuse pH-d saab reguleerida sobiva puhvri, näiteks tsitraatpuhverlahuse lisamisega. Süstelahus sisaldab kolloidset reeniumsulfiidi muutuvas koguses, kuid mitte rohkem kui 0,22 mg reeniumi protsentides, lähtudes valmistamismeetodist. See valmistatakse naatriumpertehnetaadi (99 Tc) süstimisest (jaotusega või ilma), kasutades sobivaid steriilseid pürogeenivabu koostisosi ning arvutades radionukliidide lisandite suhte valmistamiskuupäeval ja -tunnil.
Kirjeldus. Helepruun vedelik. Tehneetsium-99m poolväärtusaeg on 6,02 tundi ja kiirgab gammakiirgust.
Identifitseerimine.
A. G-spektri määramine sobiva instrumendi abil. Spekter ei tohiks oluliselt erineda standardse tehneetsium-99m spektrist, kui võrrelda seadet kasutades otseselt standardi või normatiivdokumendi andmetega. Tehneetsium-99m ja molübdeen-99 standardlahused on pädevate asutuste otsusel laboritele kättesaadavad. Kõige kuulsama g-fotoni tehneetsium-99m energia on 0,140 MeV.
B. Uurige kromatogrammi radiokeemilise puhtuse testis. Radioaktiivsuse jaotus aitab kaasa süstimise määramisele.
C. 1 ml-le lisatakse 5 ml vesinikkloriidhapet R, 5 ml 50 g/l tiouurea R lahust ja 1 ml tinakloriidi 200 g/l lahust vesinikkloriidhappes R. Ilmub kollane värv.
TESTID. RN. Süstimise pH peaks olema vahemikus 4,0 kuni 7,0.
Reenium. Katselahus. Kasutage uuringuks 1 ml süsti. Katselahus. Valmistatakse lahus, mis sisaldab 100 mikrogrammi kaaliumperrenaati R (vastab 60 ppm Re) ja 240 mikrogrammi naatriumtiosulfaati R, lahjendatakse veega R ja mõõdetakse spekter. Katselahus. 1 ml süstelahusele lisatakse 5 ml vesinikkloriidhapet R, 5 ml 50 g/l tiouurea R lahust ja 1 ml tinakloriidi R 200 g/l lahust vesinikkloriidhappes.
jne.................