Lühitoimeline beeta 2 agonist on ravim. B2-agonistid: roll ja koht bronhiaalastma ravis. Beeta-agonistide kõrvaltoimed
Tsiteerimiseks: Sinopalnikov A.I., Klyachkina I.L. b2-agonistid: roll ja koht bronhiaalastma ravis // eKr. 2002. nr 5. S. 236
Vene Föderatsiooni kaitseministeeriumi riiklik kraadiõppe instituut, Moskva
Sissejuhatus Bronhiaalastma (BA) ravi võib tinglikult jagada kahte põhivaldkonda. Esimene on sümptomaatiline ravi, mis leevendab kiiresti ja tõhusalt bronhospasmi, mis on BA juhtiv kliiniline sümptom. Teine on põletikuvastane ravi, mis aitab kaasa haiguse peamise patogeneetilise mehhanismi, nimelt hingamisteede limaskesta põletiku (AP) muutumisele.
Astma sümptomaatilise kontrolli vahendite hulgas on kesksel kohal ilmselgelt b2-agonistid, mida iseloomustab väljendunud bronhodilataator (ja bronhoprotektiivne toime) ja minimaalne arv soovimatuid kõrvaltoimeid, kui neid õigesti kasutada.
Lühiajalugu b 2 -agonistid B-agonistide kasutamise ajalugu 20. sajandil on järjest suureneva b 2 -adrenergilise selektiivsuse ja pikema toimeajaga ravimite järjekindel väljatöötamine ja kasutuselevõtt kliinilises praktikas.
Esmakordne sümpatomimeetikum adrenaliin (epinefriini) kasutati AD patsientide ravis 1900. aastal. Alguses kasutati epinefriini laialdaselt nii süstitavas vormis kui ka inhalatsioonidena. Arstide rahulolematus toime lühikese kestusega (1-1,5 tundi), ravimi suure hulga negatiivsete kõrvalmõjudega oli aga stiimuliks "atraktiivsemate" ravimite edasiseks otsimiseks.
1940. aastal ilmus isoproterenool - sünteetiline katehhoolamiin. See hävis maksas sama kiiresti kui adrenaliin (ensüümi katehhool-o-metüültransferaas - COMT osalusel) ja seetõttu iseloomustas seda lühiajaline toime (1–1,5 tundi) ja selle tulemusena tekkisid metaboliidid. isoproterenooli (metoksüprenaliini) biotransformatsioonil oli b-adrenergiline blokeeriv toime. Samal ajal ei esinenud isoproterenoolil selliseid adrenaliinile omaseid kõrvaltoimeid nagu peavalu, uriinipeetus, arteriaalne hüpertensioon jne. Isoproterenooli farmakoloogiliste omaduste uurimine viis adrenoretseptorite heterogeensuse tuvastamiseni. Viimasega seoses osutus adrenaliin universaalseks otseseks a-b-agonistiks ja isoproterenool - esimene lühitoimeline mitteselektiivne b-agonist.
Esimene selektiivne b2-agonist võeti kasutusele 1970. aastal. salbutamool , mida iseloomustab minimaalne ja kliiniliselt ebaoluline aktiivsus a- ja b1-retseptorite suhtes. Ta omandas õigustatult "kullastandardi" staatuse mitmetes b 2 -agonistides. Salbutamoolile järgnes teiste b2-agonistide (terbutaliin, fenoterool jne) kasutuselevõtt kliinilises praktikas. Need ravimid osutusid sama tõhusaks kui bronhodilataatorid kui mitteselektiivsed b-agonistid, kuna sümpatomimeetikumide bronhodilateeriv toime avaldub ainult b2-adrenergiliste retseptorite kaudu. Samal ajal näitavad b2-agonistid oluliselt vähem väljendunud stimuleerivat toimet südamele (batmotroopne, dromotroopne, kronotroopne) võrreldes b1-b2-agonisti isoproterenooliga.
Mõned erinevused b2-agonistide selektiivsuses ei oma tõsist kliinilist tähtsust. Fenoterooli kardiovaskulaarsete kõrvaltoimete suurem esinemissagedus (võrreldes salbutamooli ja terbutaliiniga) võib olla seletatav ravimi suurema efektiivse annusega ja osaliselt ka kiirema süsteemse imendumisega. Uued ravimid säilitasid oma toimekiiruse (toime ilmneb esimese 3-5 minuti jooksul pärast sissehingamist), mis on iseloomulik kõigile varasematele b-agonistidele, kusjuures nende toime kestus pikenes märgatavalt kuni 4-6 tunnini ( raske astma korral vähem väljendunud). See parandas astmasümptomite kontrolli all hoidmise võimet päevasel ajal, kuid "ei päästnud" öistest hoogudest.
Võimalus võtta üksikuid b 2 -agoniste suukaudselt (salbutamool, terbutaliin, formoterool, bambuterool) lahendas mingil määral öiste astmahoogude ohjeldamise probleemi. Kuid vajadus võtta oluliselt suuremaid annuseid (peaaegu 20 korda rohkem kui sissehingamisel) aitas kaasa a- ja b1-adrenergiliste retseptorite stimuleerimisega seotud kõrvaltoimete tekkele. Lisaks ilmnes ka nende ravimite madalam terapeutiline efektiivsus.
Pikaajaliselt inhaleeritavate b 2 -agonistide – salmeterooli ja formoterooli – ilmumine muutis oluliselt BA-ravi võimalusi. Esimest korda ilmus turule salmeterool - väga selektiivne b 2 -agonist, mille toimeaeg on vähemalt 12 tundi, kuid toime algab aeglaselt. Varsti liitus ta formoterool , mis on samuti väga selektiivne b 2 -agonist, millel on 12-tunnine toime, kuid mille bronhodilataatori toime on sarnane salbutamooliga. Juba esimestel prolongeeritud b 2 -agonistide kasutamise aastatel täheldati, et need aitavad kaasa BA ägenemiste vähenemisele, hospitaliseerimiste arvu vähenemisele ja ka inhaleeritavate kortikosteroidide (IGCS) vajaduse vähenemisele.
Kõige tõhusamaks astmaravimite, sealhulgas b2-agonistide manustamisviisiks peetakse sissehingamist. Selle tee olulised eelised on ravimite otsene manustamine sihtorganisse (mis tagab suures osas bronhodilataatorite toime kiiruse) ja soovimatute mõjude minimeerimine. Praegu teadaolevatest manustamisviisidest on kõige sagedamini kasutatavad mõõdetud annusega aerosoolinhalaatorid (MAI), harvemini mõõdetud doosiga inhalaatorid (DPI) ja nebulisaatorid. Suukaudseid b2-agoniste tablettide või siirupite kujul kasutatakse üliharva, peamiselt täiendava ravimina sagedaste öiste astmasümptomite või inhaleeritavate lühitoimeliste b2-agonistide suure vajaduse korral patsientidel, kes saavad suuri ICS-i annuseid (ekvivalent kuni 1000 mikrogrammi beklometasooni päevas või rohkem).
Toimemehhanismid b 2 -agonistid b2-agonistid põhjustavad bronhodilatatsiooni peamiselt DP silelihaste b2-adrenergiliste retseptorite otsese stimuleerimise tulemusena. Selle mehhanismi kohta on tõendeid saadud kui in vitro(isoproterenooli mõjul toimus inimese bronhide ja kopsukoe segmentide lõdvenemine) ja in vivo(DP-resistentsuse kiire langus pärast bronhodilataatori sissehingamist).
b-adrenergiliste retseptorite stimuleerimine viib adenülaattsüklaasi aktiveerumiseni, mis moodustab kompleksi G-valguga (joonis 1), mille mõjul suureneb rakusisese tsüklilise adenosiin-3,5-monofosfaadi (cAMP) sisaldus. Viimane viib spetsiifilise kinaasi (proteiini kinaas A) aktiveerimiseni, mis fosforüülib mõningaid rakusiseseid valke, mille tulemuseks on rakusisese kaltsiumi kontsentratsiooni langus (selle aktiivne “pumpamine” rakust rakuvälisesse ruumi), fosfoinositiidi hüdrolüüsi pärssimine, müosiini kerge ahela kinaaside pärssimine ja lõpuks avanevad suured kaltsiumi poolt aktiveeritud kaaliumikanalid, põhjustades silelihasrakkude repolarisatsiooni (lõõgastumist) ja kaltsiumi sekvestreerumist rakuvälisesse depoosse. Peab ütlema, et b2-agonistid võivad seostuda kaaliumikanalitega ja põhjustada otseselt silelihasrakkude lõdvestumist, sõltumata rakusisese cAMP kontsentratsiooni suurenemisest.
Joonis 1. B 2 -agonistide bronhe laiendava toimega seotud molekulaarsed mehhanismid (selgitused tekstis). K Ca - suur kaltsiumi aktiveeritud kaaliumikanal; ATP - adenosiintrifosfaat; cAMP - tsükliline adenosiin-3,5-monosfaat
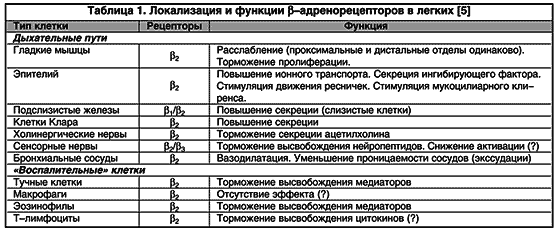
b2-agoniste peetakse funktsionaalseteks antagonistideks, mis põhjustavad bronhokonstriktsiooni vastupidist arengut, olenemata toimunud ahendavast efektist. See asjaolu näib olevat äärmiselt oluline, kuna paljudel vahendajatel (põletiku vahendajatel ja neurotransmitteritel) on bronhokonstriktor.DP erinevates osades lokaliseeritud b-adrenergiliste retseptorite (tabel 1) mõju tulemusena ilmnevad b2-agonistide täiendavad toimed, mis selgitavad ravimite profülaktilise kasutamise võimalust. Nende hulka kuuluvad vahendajate vabanemise pärssimine põletikurakkudest, kapillaaride läbilaskvuse vähenemine (bronhide limaskesta turse tekke vältimine), kolinergilise ülekande pärssimine (kolinergilise refleksi bronhokonstriktsiooni vähenemine), lima tootmise moduleerimine submukoossete näärmete poolt ja järelikult mukotsiliaarse kliirensi optimeerimine (joonis 2).

Riis. 2. B 2 -agonistide otsene ja kaudne bronhodilateeriv toime (selgitused tekstis). E - eosinofiil; TK - nuumrakk; CN - kolinergiline närv; HmC – silelihasrakk
G. Anderseni mikrokineetilise difusiooni teooria kohaselt seostatakse b 2 -agonistide toime kestust ja algusaega nende füüsikalis-keemiliste omadustega (peamiselt molekuli lipofiilsus / hüdrofiilsus) ja toimemehhanismi iseärasustega. Salbutamool - hüdrofiilne ühend. Rakuvälise ruumi vesikeskkonnas tungib see kiiresti retseptori "südamikusse" ja pärast sellega suhtlemise lõppemist eemaldatakse difusiooni teel (joonis 3). Salmeterool , mis on loodud kõrge lipofiilse ravimi salbutamooli baasil, tungib kiiresti depoofunktsiooni täitvate hingamisteede rakkude membraanidesse ja seejärel difundeerub aeglaselt läbi retseptori membraani, põhjustades selle pikaajalist aktiveerumist ja hilisemat toime algust. Lipofiilsus formoterool vähem kui salmeteroolil, mistõttu see moodustab plasmamembraanis depoo, kust difundeerub rakuvälisesse keskkonda ning seondub seejärel samaaegselt b-adrenoretseptori ja lipiididega, mis määrab nii toime avaldumise kiiruse kui ka tõusu kiiruse. selle kestuses (joon. 3). Salmeterooli ja formoterooli pikaajaline toime on seletatav nende võimega püsida pikka aega silelihasrakkude rakumembraanide kaksikkihis b 2 -adrenergiliste retseptorite vahetus läheduses ja suhelda viimastega.

Riis. 3. b 2 -agonistide toimemehhanism (selgitused tekstis)
Uurides in vitro spasmiline lihas lõdvestub formoterooli lisamisel kiiremini kui salmeterool. See kinnitab, et salmeterool on formoterooliga võrreldes osaline β2-retseptori agonist.
Rasekaaslased Selektiivsed b 2 -agonistid on kahe optilise isomeeri - R ja S - ratseemilised segud (50:50). On kindlaks tehtud, et R-isomeeride farmakoloogiline aktiivsus on 20-100 korda kõrgem kui S-isomeeridel. On näidatud, et salbutamooli R-isomeeril on bronhodilateerivad omadused. Samal ajal on S-isomeeril vastupidised omadused: põletikuvastane toime, DP hüperreaktiivsuse suurenemine, bronhospasmi suurenemine, lisaks metaboliseerub see palju aeglasemalt. Hiljuti loodi uus ravim, mis sisaldab ainult R-isomeeri ( levalbuterool
). Siiani on see olemas ainult nebulisaatorite lahuses ja sellel on parem terapeutiline toime kui ratseemiline salbutamool, kuna levalbuteroolil on samaväärne toime annuses, mis on võrdne 25% ratseemilise seguga (antagonistlikku S-isomeeri ei ole ja kõrvaltoimed vähenevad).
Selektiivsus b 2 -agonistid Selektiivsete b2-agonistide kasutamise eesmärk on pakkuda bronhodilatatsiooni ja samal ajal vältida a- ja b1-retseptorite stimuleerimisest põhjustatud kõrvaltoimeid. Enamikul juhtudel ei põhjusta b2-agonistide mõõdukas kasutamine kõrvaltoimete teket. Selektiivsus ei suuda aga nende arenguriski täielikult kõrvaldada ja sellele on mitu seletust.
Esiteks on selektiivsus b2-adrenergiliste retseptorite suhtes alati suhteline ja annusest sõltuv. A- ja b1-adrenergiliste retseptorite kerge aktiveerumine, mis on tavaliste keskmiste terapeutiliste annuste juures märkamatu, muutub kliiniliselt oluliseks ravimi annuse või selle päeva jooksul manustamise sageduse suurenemisega. Astma ägenemiste, eriti eluohtlike seisundite ravimisel tuleb arvestada b 2 -agonistide annusest sõltuva toimega, kui korduvad lühiajalised (mitu tundi) inhalatsioonid on 5-10 korda suuremad kui lubatud ööpäevane annus. .
b2 retseptorid on DP-s laialdaselt esindatud (tabel 1). Nende tihedus suureneb bronhide läbimõõdu vähenedes ja BA-ga patsientidel on b 2 retseptorite tihedus hingamisteedes suurem kui tervetel inimestel. Nuumrakkude, neutrofiilide, eosinofiilide ja lümfotsüütide pinnal leidub arvukalt b2-adrenerglisi retseptoreid. Ja samal ajal leidub b2-retseptoreid erinevates kudedes ja elundites, eriti vasakus vatsakeses, kus need moodustavad 14% kõigist b-adrenergilistest retseptoritest ja paremas aatriumis - 26% kõigist b-adrenergilistest retseptoritest. retseptorid. Nende retseptorite stimuleerimine võib põhjustada kõrvaltoimeid, sealhulgas tahhükardiat, kodade laperdust ja müokardi isheemiat. Skeletilihaste b 2 retseptorite stimuleerimine võib põhjustada lihaste värisemist. Suurte kaaliumikanalite aktiveerimine võib kaasa aidata hüpokaleemia tekkele ja selle tulemusena QT-intervalli pikenemisele ja südame rütmihäiretele, sh. Tappev. Ravimi suurte annuste süsteemsel manustamisel võib täheldada metaboolset toimet (vabade rasvhapete, insuliini, glükoosi, püruvaadi ja laktaadi sisalduse suurenemine vereseerumis).
Vaskulaarsete b 2 -retseptorite stimuleerimisel areneb vasodilatatsioon ja diastoolse vererõhu langus on võimalik. Südame soovimatud toimed on eriti väljendunud raske hüpoksia korral BA ägenemise ajal - venoosse tagasivoolu suurenemine (eriti ortopnea asendis) võib põhjustada Bezold-Jarischi sündroomi arengut koos järgneva südameseiskusega.
Ühendus vahel b 2 -agonistid ja põletik DP-s Seoses lühitoimeliste b2-agonistide laialdase kasutamisega, aga ka pikaajaliselt inhaleeritavate b2-agonistide kasutuselevõtuga kliinilisse praktikasse, on eriti aktuaalseks muutunud küsimus, kas neil ravimitel on põletikuvastane toime. Kahtlemata võib b 2 -agonistide põletikuvastast toimet, mis aitab kaasa bronhide ägeda põletiku modifikatsioonile, pidada nuumrakkudest põletikuliste vahendajate vabanemise pärssimiseks ja kapillaaride läbilaskvuse vähenemiseks. Samas leiti regulaarselt b 2 -agoniste tarvitavatel BA-haigetel bronhide limaskesta biopsia käigus, et põletikuliste rakkude, sh. ja aktiveeritud (makrofaagid, eosinofiilid, lümfotsüüdid) ei vähene.
Samal ajal võib teoreetiliselt regulaarne b2-agonistide tarbimine põhjustada isegi põletiku süvenemist DP-s. Seega võimaldab b 2 -agonistide põhjustatud bronhodilatatsioon sügavamalt hingata, mis võib põhjustada ulatuslikumat kokkupuudet allergeenidega.
Lisaks võib b2-agonistide regulaarne kasutamine varjata arenevat ägenemist, lükates seeläbi edasi tõelise põletikuvastase ravi alustamist või intensiivistumist.
Võimalik kasutusrisk b 2 -agonistid Tolerantsus Inhaleeritavate b2-agonistide sagedane regulaarne kasutamine võib põhjustada nende suhtes tolerantsuse (desensibiliseerumise) väljakujunemist. cAMP akumuleerumine aitab kaasa retseptori üleminekule mitteaktiivsesse olekusse. B-adrenergiliste retseptorite liiga intensiivne stimuleerimine aitab kaasa desensibilisatsiooni tekkele (retseptorite tundlikkuse vähenemine retseptori lahtiühendamise tagajärjel G-valgust ja adenülaattsüklaasist). Säilitades liigset stimulatsiooni, väheneb retseptorite arv rakupinnal (“alla” reguleerimine). Tuleb märkida, et DP silelihaste b-retseptoritel on üsna märkimisväärne reserv ja seetõttu on nad desensibiliseerimise suhtes vastupidavamad kui mittehingavate tsoonide (näiteks skeletilihaste või ainevahetust reguleerivate) retseptorid. On kindlaks tehtud, et tervetel inimestel tekib kiiresti taluvus salbutamooli suurte annuste, kuid mitte fenoterooli ja terbutaliini suhtes. Samal ajal ilmneb BA-ga patsientidel harva tolerantsus b 2 -agonistide bronhodilateeriva toime suhtes, tolerantsus nende bronhoprotektiivse toime suhtes areneb palju sagedamini.
B 2 -agonistide bronhoprotektiivse toime vähenemine nende regulaarsel ja sagedasel kasutamisel kehtib võrdselt nii lühitoimeliste kui ka pikaajaliselt kasutatavate ravimite puhul, isegi inhaleeritavate kortikosteroidide baasravi taustal. Samal ajal ei räägi me bronhoprotektsiooni täielikust kadumisest, vaid selle esialgse taseme kergest langusest. H. J. van der Woude jt. leidis, et astmahaigete poolt formoterooli ja salmeterooli regulaarse kasutamise taustal viimase bronhodilateeriv toime ei vähene, formoteroolil on bronhoprotektiivne toime suurem, kuid salbutamooli bronhodilateeriv toime on palju vähem väljendunud.
Desensibiliseerimine areneb pikka aega, mitme päeva või nädala jooksul, erinevalt tahhüfülaksiast, mis areneb väga kiiresti ja ei ole seotud retseptorite funktsionaalse seisundiga. See asjaolu seletab ravi efektiivsuse vähenemist ja nõuab b 2 -agonistide kasutamise sageduse piiramist.
Paljud teadlased seostavad geenide geneetilise polümorfismiga individuaalset varieeruvust reaktsioonis b2-agonistidele ja tolerantsuse kujunemist nende bronhodilateeriva toime suhtes. b2-adrenergilise retseptori geen paikneb 5q kromosoomil. Oluline mõju BA kulgemisele ja ravi efektiivsusele on b2-adrenergiliste retseptorite aminohappejärjestuse muutumisel, eriti aminohapete liikumisel koodonites 16 ja 27. Geeni polümorfismi mõju ei laiene bronhoprotektiivse toime varieeruvusele. Ausalt öeldes tuleb märkida, et need andmed ei ole kõigis töödes kinnitatud.
b 2 -agonistid ja suremus BA-ga patsientidel
Tõsised kahtlused inhaleeritavate b-agonistide ohutuses tekkisid 20. sajandi 60ndatel, kui paljudes riikides, sealhulgas Inglismaal, Austraalias ja Uus-Meremaal, puhkes astmahaigete seas "surmade epideemia". Samal ajal tehti ettepanek, et sümpatomimeetilise ravi ja AD suurenenud suremuse vahel on seos. Põhjuslikku seost b-agonistide (isoproterenooli) kasutamise ja suurenenud suremuse vahel toona ei tuvastatud ning neid oli retrospektiivsete uuringute tulemuste põhjal peaaegu võimatu tõestada. Seos fenoterooli kasutamise ja astmasse suremuse suurenemise vahel Uus-Meremaal 1980. aastatel on tõestatud, kuna leiti, et seda ravimit määrati surmaga lõppenud astma korral sagedamini kui hästi kontrollitud haiguse korral. Seda seost kinnitas kaudselt ka suremuse vähenemine, mis langes kokku fenoterooli laialdase kasutamise kaotamisega (koos teiste b 2 -agonistide müügi üldise kasvuga). Sellega seoses on soovituslikud Kanadas tehtud epidemioloogilise uuringu tulemused, mille eesmärk oli uurida võimalikku seost surmajuhtumite sageduse ja välja kirjutatud ravimite vahel. On näidatud, et surmajuhtumite esinemissageduse suurenemine on seotud suurte annustega raviga mis tahes olemasoleva inhaleeritava b2-agonistiga. Surmaga lõppenud tulemuse risk oli kõrgeim fenoterooli puhul, kuid võrreldes salbutamooli samaväärsete annustega ei erinenud suremus oluliselt.
Samal ajal ei saa usaldusväärselt tõestada seost suurtes annustes b2-agonistidega ravi ja AD-sse suremuse suurenemise vahel, kuna raskema ja halvasti kontrollitud AD-ga patsiendid kasutavad suurema tõenäosusega suuri b2-annuseid. agonistid ja vastupidi, harvem tõhusate põletikuvastaste ravimite abiga. Lisaks varjavad b2-agonistide suured annused BA suureneva fataalse ägenemise märke.
Annustamisrežiim Sissehingatavad lühitoimelised b 2 -agonistid Ei ole kahtlust, et inhaleeritavad lühitoimelised b2-agonistid on valitud ravimid astma situatsiooniliseks sümptomaatiliseks kontrolliks, samuti treeningust põhjustatud astma (AFA) sümptomite tekke ennetamiseks. Inhaleeritavate b-agonistide regulaarne kasutamine võib viia piisava kontrolli kadumiseni haiguse kulgemise üle. Näiteks uuringus M.R. Sears et al. Uus-Meremaal uuriti bronhide hüperreaktiivsust, hommikust PSV-d, igapäevaseid sümptomeid ja inhaleeritavate kortikosteroidide vajadust patsientidel, kes kasutasid tellitavaid b 2 agoniste, võrreldes patsientidega, kes kasutasid fenoterooli regulaarselt 4 korda päevas. Fenoterooli regulaarse manustamisega patsientide rühmas täheldati astma sümptomite halba kontrolli, lisaks esines sagedamini ja raskemaid ägenemisi võrreldes patsientide rühmaga, kes kasutasid b 2 -agoniste "nõudmisel" kuue kuu jooksul. Viimase puhul paranesid välise hingamise funktsiooni parameetrid, hommikune PSV, vähenes reaktsioon metakoliiniga bronhoprovokatsioonitestile. Bronhide hüperreaktiivsuse suurenemine lühitoimeliste b2-agonistide regulaarse tarbimise taustal on tõenäoliselt tingitud S-enantomeeride olemasolust ravimi ratseemilises segus.
Salbutamooli puhul ei olnud selliseid mustreid võimalik kindlaks teha, kuigi nagu fenoterooli puhul, kaasnes selle regulaarsel tarbimisel bronhide hüperreaktiivsuse kerge tõus. On tõendeid selle kohta, et salbutamooli regulaarse kasutamisega kaasneb AFU episoodide sageduse suurenemine ja põletiku raskuse suurenemine DP-s.
Lühitoimelisi b 2 -agoniste tuleks kasutada (ka monoteraapia osana) ainult "nõudmisel". On ebatõenäoline, et tavaliselt soovitatud b2-agonistide annustamisskeem "nõudmisel" võib halvendada kontrolli astma kulgemise üle, kuid ravimi suurte annuste kasutamisel muutub kontrolli halvenemine reaalseks. Lisaks muutuvad paljud patsiendid agonistide suhtes eriti tundlikuks polümorfismi b2-adrenergiliste retseptorite juuresolekul, mis viib kontrolli kiirema halvenemiseni. Astmahaigete suurenenud surmariski ja inhaleeritavate b2-agonistide suurte annuste kasutamise vahel kindlaks tehtud seos peegeldab ainult haiguse tõsidust. Samuti on võimalik, et inhaleeritavate b2-agonistide suurtel annustel on AD kulgemisele kahjulik mõju. B 2 -agonistide suurtes annustes (üle 1,4 aerosoolpurgi kuus) saavad patsiendid vajavad kindlasti tõhusat põletikuvastast ravi, sh. ja selleks, et vähendada b2-agonistide annust. Bronhodilataatorite vajaduse suurenemisega (rohkem kui kolm korda nädalas) on näidustatud täiendav põletikuvastaste ravimite retsept ning b 2 -agonistide kasutamisel rohkem kui 3-4 korda päevas sümptomite leevendamiseks nende annus on näidatud.
Lühitoimeliste b 2 -agonistide vastuvõtmine bronhoprotektsiooni eesmärgil on samuti piiratud "mõistlike piiridega" (mitte rohkem kui 3-4 korda päevas). B 2 -agonistide bronhoprotektiivsed omadused võimaldavad paljudel kõrge kvalifikatsiooniga astmahaigetel sportlastel võistelda rahvusvahelisel tasemel (reeglid lubavad kasutada lühitoimelisi b 2 -agoniste AFU ennetamiseks tingimusel, et haigus on meditsiiniliselt kinnitatud) . Näiteks 1984. aasta olümpiamängudel Los Angeleses osales 67 AFU sportlast, kellest 41 said erineva nimetusega medalid. On teada, et suukaudsed b 2 -agonistid suurendavad efektiivsust, suurendades lihasmassi, valkude ja lipiidide anabolismi ning psühhostimulatsiooni. C. Goubarti jt uuringus. on näidatud, et inhaleeritavate b 2 -agonistide mõju tervetel sportlastel piirdub vaid kerge bronhodilatatsiooniga, mis aga võib oluliselt kaasa aidata hingamise kohanemise parandamisele treeningu alguses.
Pikatoimelised inhaleeritavad b 2 -agonistid
Praegu saadaval olevad pikendatud inhaleeritavad b2-agonistid – formoterool ja salmeterool avaldavad oma toimet 12 tunni jooksul samaväärse bronhodilataatori toimega. Sellest hoolimata on nende vahel erinevusi. Esiteks on see formoterooli (DPI kujul) kiirus, mis on võrreldav salbutamooli (PAI kujul) toime alguse ajaga, mis võimaldab formoterooli kasutada kiirabiautona, mitte lühiajaliselt. toimivad b2-agonistid. Samal ajal on formoterooli kasutamisel kõrvaltoimeid oluliselt vähem kui salbutamooli kasutamisel. Neid ravimeid võib kasutada monoteraapiana kerge astmaga patsientidel AFU bronhoprotektoritena. Kui kasutate formoterooli rohkem kui 2 korda nädalas "nõudmisel", on vaja ravile lisada ICS-i.
Tuleb märkida, et regulaarne monoteraapia pikatoimeliste β2-agonistidega ei ole soovitatav, kuna siiani puuduvad usaldusväärsed tõendid nende põletikuvastase ja haigust modifitseeriva toime kohta.
ICS-i ja bronhodilataatorite kombineeritud kasutamise otstarbekuse kohta on teaduslikke tõendeid. Kortikosteroidid suurendavad b 2 retseptorite ekspressiooni ja vähendavad potentsiaalset desensibilisatsiooni, samas kui pikaajalised b 2 agonistid suurendavad kortikosteroidi retseptorite tundlikkust ICS-i suhtes.
Seni läbi viidud uuringud näitavad pikaajalise inhaleeritavate b2-agonistide varasema määramise võimalust. Näiteks patsientidel, kellel ei ole piisavat astmakontrolli 400–800 µg ICS-i võtmise ajal, tagab salmeterooli täiendav manustamine täielikuma ja piisava kontrolli võrreldes ICS-i annuse suurendamisega. Formoterool näitab sarnast toimet ja aitab samal ajal vähendada haiguse ägenemiste sagedust. Need ja mitmed teised uuringud viitavad sellele, et pikatoimeliste inhaleeritavate b2-agonistide lisamine madala keskmise annusega ICS-ravile patsientidel, kellel ei ole piisavat astmakontrolli, võrdub steroidide annuse kahekordistamisega.
Praegu soovitatakse pikaajaliselt inhaleeritavaid b 2 -agoniste kasutada ainult patsientidel, kes saavad samaaegselt ICS-i. Fikseeritud kombinatsioonid, nagu salmeterool flutikasooniga (Seretide) ja formoterool budesoniidiga (Symbicort), tunduvad paljutõotavad. Samal ajal märgitakse paremat vastavust, välistatud on ainult ühe ravimi kasutamise oht haiguse pikaajalise ravi raames.
Kirjandus:1. National Institutes of Health, National Heart, Lung and Blood Institute. Eksperdipaneeli aruanne 2: juhised astma diagnoosimiseks ja raviks. Bethesda, Md: riiklikud terviseinstituudid, riiklik südame-, kopsu- ja vereinstituut; aprill 1997. NIH väljaanne 97-4051.
2. Lawrence D.R., Benitt P.N. Kliiniline farmakoloogia. 2 köites. Moskva: meditsiin; 1991. aastal
3. Mashkovsky M.D. Ravimid. Moskva: meditsiin; 1984. aasta
4. Näidake M. B2-agoniste alates farmakoloogilistest omadustest kuni igapäevase kliinilise praktikani. Rahvusvahelise töötoa aruanne (28.-29. veebruaril 200 Londonis, Ühendkuningriigis toimunud seminari põhjal)
5 Barnes P.J. b-agonistid, antikolinergilised ained ja muud mittesteroidsed ravimid. In: Albert R., Spiro S., Jett J., toimetajad. Terviklik hingamisteede meditsiin. Ühendkuningriik: Harcourt Publishers Limited; 2001.lk.34.1-34-10
6. Täiskasvanute astma käsitlevate juhiste ajakohastamine (toimetus). BMJ 2001; 323:1380-1381.
7. Jonson M. b2-adrenoretseptori agonistid: optimaalne farmakoloogiline profiil. Artiklis: b 2 -agonistide roll astma ravis. Oxford: Meditsiinigrupp; 1993.lk. 6-8.
8 Barnes P.J. beeta-adrenergilised retseptorid ja nende reguleerimine. Am J Respir Crit Care Med. 1995; 152:838-860.
9. Kume H., Takai A., Tokuno H., Tomita T. Ca 2 + -sõltuva K+-kanali aktiivsuse reguleerimine hingetoru müotsüütides fosforüülimise teel. Loodus 1989; 341:152-154.
10 Anderson G.P. Pika toimeajaga inhaleeritavad beeta-adrenoretseptori agonistid: formoterooli ja salmeterooli võrdlev farmakoloogia. Agents Actions Suppl. 1993; 43:253-269.
11. Stiles GL, Taylor S, Lefkowitz RJ. Inimese südame beeta-adrenergilised retseptorid: alatüübi heterogeensus, mis on piiritletud otsese radioligandi sidumisega. elu sci. 1983; 33:467-473.
12. Eelnev JG, Cochrane GM, Raper SM, Ali C, Volans GN. Suukaudse salbutamooliga enesemürgitus. BMJ. 1981; 282:1932.
13. Handley D. Beeta-agonistide (S)-isomeeride astmataoline farmakoloogia ja toksikoloogia. J Allergy Clinic Immunol. 1999; 104: S69-S76.
14. Jonson M., Coleman R. Beeta-2-adrenoretseptori agonistide toimemehhanismid. In: Bisse W., Holgate S., juhtkirjad. Astma ja riniit. Blackwelli teadus; 1995. lk 1278-1308.
15. Burggsaf J., Westendorp R.G.J., in’t Veen J.C.C.M et al. Inhaleeritava salbutamooli kardiovaskulaarsed kõrvaltoimed hüpoksilistel astmahaigetel. Rindkere 2001; 56:567-569.
16. Van Shayck C.P., Bijl-Hoffland I.D., Closterman S.G.M. et al. Lühi- ja pikatoimeliste b2-agonistide potentsiaalne maskeeriv toime düspnoe tajumisele astma korral. ERJ 2002; 19:240-245.
17. Van der Woude H.J., Winter T.N., Aalbers R. Salbutamooli vähenenud bronhodilateeriv toime metakoliini põhjustatud mõõduka kuni raske bronhokonstriktsiooni leevendamisel suure annusega ravi ajal pikatoimeliste b2-agonistidega. Rindkere 2001; 56:529-535.
18. Nelson H.S. Kliiniline kogemus levalbuterooliga. J Allergy Clinic Immunol. 1999; 104:S77-S84.
19. Lipworth BJ, Hall IP, Tan S, Aziz I, Coutie W. Geneetilise polümorfismi mõjud b2-adrenoretseptorite ex vivo ja in vivo funktsioonile astmahaigetel. Chest 1999;115:324-328.
20. Lipworth BJ, Kopelman G.H., Wheatley A.P. et al. b 2 -adrenoretseptori promootori polümorfism: laiendatud halotüübid ja funktsionaalsed toimed perifeerse vere mononukleaarsetes rakkudes. Rindkere 2002; 57:61-66.
21. Lima JJ, Thomason DB, Mohamed MH, Eberle LV, Self TH, Johnson JA. B2-adrenergilise retseptori geneetiliste polümorfismide mõju albuterooli bronhodilataatori farmakodünaamikale. Clin Pharm Ther 1999; 65:519-525.
22. Kotani Y, Nishimura Y, Maeda H, Yokoyama M. b 2 -adrenergilise retseptori polümorfismid mõjutavad astmahaigete hingamisteede reaktsioonivõimet salbutamoolile. J Asthma 1999; 36:583-590.
23. Taylor D.R., Sears M.R., Cockroft D.W. Beeta-agonistide vaidlus. Med Clin North Am 1996; 80:719-748.
24. Spitzer WO, Suissa S, Ernst P jt. Beeta-agonistide kasutamine ja astmast põhjustatud surma- ja surmaoht. N Engl J Med 1992; 326:501-506.
25. Sears MR, Taylor DR, Print CG jt. Regulaarne inhaleeritav beeta-agonisti ravi bronhiaalastma korral. Lancet 1990; 336:1391-1396.
26. Handley D. Beeta-agonistide (S)-isomeeride astmataoline farmakoloogia ja toksikoloogia. J Allergy Clinic Immunol. 1999; 104:S69-S76.
27. Nelson H.S. Kliiniline kogemus levalbuterooliga. J Allergy Clin Immunol 1999;104:S77-S84.
28. Liggett S.B. B2-adrenergilise retseptori polümorfismid astma korral. Olen J Respir Cri. Care Med 1997; 156:S 156-162.
29. Voy R.O. USA olümpiakomitee kogemus treeningust põhjustatud bronhospasmiga. Med Sci Exerc 1986; 18:328-330.
30. Lafontan M, Berlan M, Prud'hon M. Les agonistes beeta-adrenergiques. Toimemehhanismid: lipomobilisatsioon ja anabolism. Reprod Nutr Develop 1988; 28:61-84
31. Martineau L, Horan MA, Rothwell NJ et al. Salbutamool, b2-adrenoretseptori agonist, suurendab noorte meeste skeletilihaste tugevust. ClinSci 1992; 83:615-621.
32 Hind AH, Clissold SP. Salbutamool 1980. aastatel. Selle kliinilise efektiivsuse ümberhindamine. Narkootikumid 1989; 38:77-122.
33. Goubault C, Perault M-C, Leleu jt. Inhaleeritava salbutamooli mõju mitte-astmahaigetele sportlastele, Thorax 2001; 56:675-679.
34. Seberova E, Hartman P, Veverka J jt. Turbuhaler®-i manustatud formoteroolil oli pMDI poolt manustatud salbutamooli toime kiire algus. Ameerika Rindkereühingu 1999. aasta rahvusvahelise konverentsi programm ja kokkuvõtted; 23.–28. aprill 1999; San Diego, California Abstraktne A637.
35. Wallin A., Sandstrom T., Soderberg M. et al. Tavalise inhaleeritava formoterooli, budesoniidi ja platseebo mõju limaskesta põletikule ja kerge astma kliinilistele näitajatele. Am J Respir Crit Care Med. 1998; 158:79-86.
36. Greening AP, Ind PW, Northfield M, Shaw G. Lisatud salmeterool versus suurem annus kortikosteroidi astmahaigetel, kellel esinevad olemasoleva inhaleeritava kortikosteroidi sümptomid. Allen & Hanburys Limited Ühendkuningriigi õpperühm. Lancet. 1994; 334:219-224.
Iga ravim kuulub konkreetsesse farmakoloogilise rühma. See tähendab, et mõnel ravimil on sama toimemehhanism, näidustused ja kõrvaltoimed. Üks peamisi farmakoloogilisi rühmi on beeta-agonistid. Neid ravimeid kasutatakse laialdaselt hingamisteede ja kardiovaskulaarsete patoloogiate ravis.
Mis on B-agonistid?
Beeta-agonistid on ravimite rühm, mida kasutatakse erinevate haiguste raviks. Organismis seostuvad nad spetsiifiliste retseptoritega, mis paiknevad bronhide, emaka, südame ja veresoonte kudede silelihastes. See interaktsioon põhjustab beetarakkude stimuleerimist. Selle tulemusena aktiveeruvad mitmesugused füsioloogilised protsessid. Kui B-agonistid seonduvad retseptoritega, stimuleeritakse selliste bioloogiliste ainete nagu dopamiini ja adrenaliini tootmist. Nende ühendite teine nimi on beeta-agonistid. Nende peamine mõju on südame löögisageduse tõus, vererõhu tõus ja bronhide juhtivuse paranemine.

Beeta-agonistid: toime kehas
Beeta-agonistid jagunevad B1- ja B2-agonistideks. Nende ainete retseptorid asuvad siseorganites. Kui beeta-agonistid on nendega seotud, aktiveerivad nad kehas paljusid protsesse. Eristatakse järgmisi B-agonistide toimeid:
- Suurenenud südame automatism ja paranenud juhtivus.
- Pulsi tõus.
- Lipolüüsi kiirendamine. B1-agonistide kasutamisel ilmuvad verre vabad rasvhapped, mis on triglütseriidide lagunemise saadused.
- Vererõhu tõus. See toime on tingitud reniin-angiotensiin-aldosterooni süsteemi (RAAS) stimuleerimisest.
Adrenomimeetikumide seondumine B1 retseptoritega viib loetletud muutusteni organismis. Need paiknevad südamelihases, veresoontes, rasvkoes ja neerurakkudes.

B2-retseptoreid leidub bronhides, emakas, skeletilihastes ja kesknärvisüsteemis. Lisaks leidub neid südames ja veresoontes. Beeta-2-agonistid põhjustavad järgmisi toimeid:
- Bronhide juhtivuse paranemine. See tegevus on tingitud silelihaste lõdvestumisest.
- Glükogenolüüsi kiirendamine lihastes. Selle tulemusena tõmbuvad skeletilihased kiiremini ja tugevamalt kokku.
- Müomeetriumi lõdvestamine.
- Glükogenolüüsi kiirendamine maksarakkudes. See toob kaasa veresuhkru taseme tõusu.
- Südame löögisageduse tõus.
Millised ravimid kuuluvad B-agonistide rühma?
Arstid määravad sageli beeta-agoniste. Sellesse farmakoloogilise rühma kuuluvad ravimid jagunevad lühi- ja kiiretoimelisteks ravimiteks. Lisaks eraldatakse ravimid, millel on selektiivne toime ainult teatud organitele. Mõned ravimid toimivad otse B1- ja B2-retseptoritele. Tuntumad ravimid beetaagonistide rühmast on ravimid Salbutamol, Fenoterol, Dopamine. B-agoniste kasutatakse kopsu- ja südamehaiguste ravis. Samuti kasutatakse mõnda neist intensiivravi osakonnas (ravim "Dobutamiin"). Harvemini kasutatakse selle rühma ravimeid günekoloogilises praktikas.

Beeta-agonistide klassifikatsioon: ravimite tüübid
Beeta-agonistid on farmakoloogiline rühm, mis hõlmab suurt hulka ravimeid. Seetõttu on need jagatud mitmeks rühmaks. B-agonistide klassifikatsioon hõlmab:
- Mitteselektiivsed beeta-agonistid. Sellesse rühma kuuluvad ravimid "Orciprenaliin" ja "Isoprenaliin".
- Selektiivsed B1-agonistid. Neid kasutatakse kardioloogia- ja intensiivraviosakondades. Selle rühma esindajad on ravimid Dobutamiin ja Dopamiin.
- Selektiivsed beeta-2-agonistid. Sellesse rühma kuuluvad ravimid, mida kasutatakse hingamisteede haiguste raviks. Selektiivsed B2-agonistid jagunevad omakorda lühitoimelisteks ja pikaajalise toimega ravimiteks. Esimesse rühma kuuluvad ravimid "Fenoterool", "Terbutaliin", "Salbutamool" ja "Heksoprenaliin". Pikatoimelised ravimid on formoterool, salmeterool ja indakaterool.
Näidustused B-agonistide kasutamiseks
B-agonistide kasutamise näidustused sõltuvad ravimi tüübist. Mitteselektiivseid beeta-agoniste praegu praktiliselt ei kasutata. Varem kasutati neid teatud tüüpi arütmiate, südamejuhtivuse halvenemise ja bronhiaalastma raviks. Arstid eelistavad nüüd välja kirjutada selektiivseid B-agoniste. Nende eeliseks on see, et neil on palju vähem kõrvaltoimeid. Lisaks on selektiivseid ravimeid mugavam kasutada, kuna need mõjutavad ainult teatud organeid.
Näidustused B1-agonistide määramiseks:
- Mis tahes etioloogiaga šokk.
- Ahenda.
- Dekompenseeritud südamedefektid.
- Harva - raske isheemiline südamehaigus.

B2-agonistid on ette nähtud bronhiaalastma, kroonilise obstruktiivse kopsuhaiguse korral. Enamikul juhtudel kasutatakse neid ravimeid aerosoolide kujul. Mõnikord kasutatakse ravimit "Fenoterool" günekoloogilises praktikas sünnituse aeglustamiseks ja raseduse katkemise vältimiseks. Sel juhul manustatakse ravimit intravenoosselt.
Millistel juhtudel on B-adrenergilised agonistid vastunäidustatud?

B2-agonistid on vastunäidustatud järgmistel juhtudel:
- Beeta-agonistide talumatus.
- Rasedus, mida komplitseerib verejooks, platsenta irdumine, raseduse katkemise oht.
- Alla 2-aastased lapsed.
- Põletikulised protsessid müokardis, rütmihäired.
- Diabeet.
- Aordi stenoos.
- Arteriaalne hüpertensioon.
- Äge südamepuudulikkus.
- türeotoksikoos.
Ravim "Salbutamol": kasutusjuhised
Salbutamool on lühikese toimeajaga B2 agonist. Seda kasutatakse bronhide obstruktsiooni sündroomi korral. Kõige sagedamini kasutatakse aerosoolides, 1-2 annust (0,1-0,2 mg). Lastel on eelistatav hingata läbi nebulisaatori. Samuti on ravimi tabletivorm. Täiskasvanute annus on 6-16 mg päevas.
"Salbutamool": ravimi hind
Ravimit kasutatakse kerge bronhiaalastma monoteraapiana. Kui patsiendil on haiguse keskmine või raske staadium, kasutatakse pikatoimelisi ravimeid (pika toimeajaga beeta-agoniste). Need on bronhiaalastma põhiraviks. Astmahoo kiireks leevendamiseks kasutatakse ravimit "Salbutamol". Ravimi hind on 50 kuni 160 rubla, olenevalt tootjast ja viaalis sisalduvast annusest.
Bronhodilataatorite rühma kuuluvad sümpatomimeetikumid (beeta-2-agonistid), antikolinergilised ained (M-antikolinergilised ained), metüülksantiinid (teofülliinid).
Beeta-2-agonistid jagatakse toime kestuse järgi lühi- ja pikatoimelisteks ravimiteks.
Lühitoimelised beeta-2-agonistid on kõige tõhusamad bronhodilataatorid sümptomite (vilistav hingamine, pigistustunne rinnus ja köha) ja hädaolukorra lahendamiseks. Nad suudavad kiiresti laiendada ahenenud bronhe. Nende sissehingamisel ilmneb bronhodilateeriv toime 5-10 minuti pärast. Määrake need mitte rohkem kui 4 korda päevas.
Pikaajalise toimega beeta-2 agonistide toime ilmneb hiljem. Seoses sellega ei ole need ravimid ette nähtud bronhospasmihoogude leevendamiseks, vaid neid võib soovitada pikemaajaliseks püsiraviks astmahoo ja haiguse ägenemise ennetamiseks ning on ka alternatiiviks inhaleeritavate kortikosteroidide annuste suurendamisele. Nende puuduseks on see, et neid ravimeid võtvad patsiendid on määratud kiiretoimelist inhaleeritavat kortikosteroidi alati kaasas kandma, kui beeta-2 agonisti ennetav toime ebaõnnestub ja neil tekivad hingamisprobleemid. Neid ravimeid võib kasutada täiendava ravina mõõduka kuni raske astma korral. Arvamused pikaajalise sümpatomimeetikumide pikaajalise kasutamise otstarbekuse kohta on aga üsna vastuolulised. Mõned teadlased usuvad, et selliste ravimite pidev kasutamine pikka aega võib halvendada prognoosi haiguse enda käigus, teised kardavad tahhüfülaksia kiiremat arengut, kuid see pole üheselt mõistetav ja nõuab täiendavat uurimist. sümpatomimeetikumid on nende kõrge efektiivsus ja selektiivsus. Selliste ravimite kõrvaltoimed kardiovaskulaarsüsteemile on viidud miinimumini. Enamiku beeta-2-agonistide peamine puudus on lühike toimeaeg (4-6 tundi), mis nõuab sagedast kasutamist päevasel ajal ja ravimi madalat kontsentratsiooni veres öösel.
Peamiste beeta-2-agonistide preparaatide võrdlusomadused on esitatud tabelis 2.
Bronhiaalastma ravis kasutatavate peamiste beeta-2-agonistide võrdlusomadused.
M-kolinolüütikumid (antikolinergikud) ei ole astma ägenemise ravis esmavaliku ravimid, nende efektiivsus astma korral jääb alla sümpatomimeetikumidele. Antikolinergilistel ravimitel on mitmeid toimeid, mis raskendavad nende kasutamist: nad põhjustavad ninaneelu ja ülemiste hingamisteede limaskestade kuivust, vähendavad bronhide näärmete sekretsiooni ja epiteeli ripsmete liikuvust, st pärsivad bronhide evakueerimisfunktsioon, südamelöökide arvu suurendamine, pupillide laienemise stimuleerimine, naha punetus. Seetõttu on antikolinergilistel ravimitel AD stabiilse kulgemise korral beeta-2-agonistidega võrreldes tagasihoidlikum koht. Venemaal on kõige levinum antikolinergiline ravim ipratroopiumbromiid (Atrovent®). Selle ravimi eelisteks on see, et sellel on pikem toimeaeg kui sümpatomimeetikumidel, selle toime kogukestus on umbes, toime algust täheldatakse 5 minuti pärast ja toime maksimum saabub 1,5 tunni pärast.
Kolinergilisi ravimeid kasutatakse peamiselt:
Bronhiidi sümptomite ülekaaluga,
"köha astmaga" (köha kui astmahoo ekvivalent),
Füüsilisest tegevusest, külmast, tolmu, gaaside sissehingamisest põhjustatud bronhide obstruktsiooniga;
Bronhoobstruktiivse sündroomiga koos raske bronhorröaga ("märg astma"),
BA-ga patsientidel, kellel on vastunäidustused beeta-2-agonistide määramiseks;
Psühhogeense astma ja hormonaalsete omadustega (premenstruaalne astma, astma kombinatsioon türeotoksikoosiga) on antikolinergiliste ja rahustavate ainete kompleksi kasutamisel eelis beeta-2-agonistide ees;
Öise astma korral
Atmosfääri saasteainete ja keemiliste ärritajate poolt põhjustatud astma korral
Mõnel juhul kasutatakse antikolinergikuid koos beeta-2-agonistidega. Kombineeritud ravimeid kasutatakse BA ravis aga harva, kuna ravi tavaliste ravimitega, nagu beeta-2 agonistid või ipratroopiumbromiid, on tõhusam ja võimaldab iga ravimi selektiivset doseerimist. Eeliseks on see, et sellisel kombinatsioonil on sünergia ja see vähendab koostisosade kõrvaltoimete riski. Kombineeritud ravi annab ka suurema bronhodilateeriva toime võrreldes monoteraapiaga ja võib oluliselt pikendada selle kestust. Peamised ipratroopiumi ja beeta-2-agonistidega kombineeritud preparaadid on ipratroopium/fenoterool (Berodual®) ja ipratroopium/salbutamool (Combivent®). Neid ravimeid kasutatakse peamiselt raskete astmahoogude kompleksravi osana - sissehingamisel läbi nebulisaatori.
Metüülksantiinidest kasutatakse bronhiaalastma ravis teofülliini ja aminofülliini.
Nende ravimite üleannustamisel tekkida võivate mitmete kõrvaltoimete tõttu on vajalik teofülliini kontsentratsiooni jälgimine veres. Aminofülliini (teofülliini ja etüleendiamiini segu, mis lahustub 20 korda paremini kui teofülliin ise) manustatakse intravenoosselt väga aeglaselt (vähemalt 20 minutit). Intravenoosne aminofülliin mängib olulist rolli raskete astmahoogude leevendamisel, mis taluvad beeta-2-agonistide pihustatud vorme. Aminofülliini kasutatakse ka südamepuudulikkusega patsientidel koos astma või bronhiidiga, kellel on kopsuvereringe hüpertensioon. Organismis vabastab aminofülliin vaba teofülliini.
Kaasaegsed beeta-2-adrenomimeetikumid ja põletikuvastased ravimid "pressisid" teofülliini ravimeid astma ravis. Näidustused valdavaks kasutamiseks astma korral on järgmised:
Astma rünnaku perioodil intravenoosse tilk-infusioonina 5-10 ml 2,4% lahust koos kaaliumipreparaatide ja (kui on näidustatud) kortikosteroididega soolalahuses;
Individuaalselt tiitritud teofülliini preparaadid (0,1–0,5 g) on efektiivsed öiste astmahoogude ravis;
Kroonilise astma korral võib teofülliini preparaatide pikaajaline kasutamine oluliselt vähendada beeta-2-agonistide annust ja vähendada astma sümptomite raskust.
Bronhodilataatorite turu analüüsiga saate tutvuda Tööstusturu-uuringute Akadeemia aruandes "Venemaa bronhiaalastma ravi ravimite turg".
Tööstusturu-uuringute Akadeemia
Ravimid
Vahendid, mis stimuleerivad rögaeritust
Refleksi toimega ravimid
Nende hulka kuuluvad termopsise, istoda, vahukommi, lagritsa, näsaravimid. Suukaudsel manustamisel on selle rühma ravimitel mõõdukas ärritav toime mao retseptoritele, mis suurendab refleksiivselt süljenäärmete ja bronhide limaskestade sekretsiooni. Nende ravimite toime on lühiajaline, seetõttu on vajalik sagedased väikesed annused (iga 2-4 tunni järel). Köhalahtistitest on ette nähtud rikkalik aluseline jook, vahukommi tõmmised ja dekoktid, termopsis - kuni 10 korda päevas. Expektorante kasutatakse nii haiguse ägenemise kui ka remissiooni perioodil.
Resorptiivsed ravimid: naatrium- ja kaaliumjodiid, naatriumvesinikkarbonaat ja muud soolapreparaadid. Nad suurendavad bronhide sekretsiooni, põhjustavad bronhisekreedi vedeldamist ja hõlbustavad seeläbi rögaeritust.
Tabletid ja dražeed 8, 12, 16 mg. Ravim viaalis.
Siirup. Lahus suukaudseks manustamiseks. Täiskasvanutele määratakse 8-16 mg 4 korda päevas.
Tabletid 8 mg 100 tk pakendis. Lahus suukaudseks manustamiseks. Eliksiir. Määrake 8-16 mg 4 korda päevas.
Tabletid 30 mg 20 tk pakendis. Kapslid retard 75 mg, 10 ja 20 tk pakendis. Suukaudseks manustamiseks mõeldud lahus 40 ja 100 ml viaalides. Siirup 100 ml viaalides. Tavaline ravimi ööpäevane annus tablettidena on 60 mg. Võtke 1 tablett 2-3 korda päevas koos väikese koguse vedelikuga koos toiduga. Toimeainet prolongeeritult vabastavad kapslid (retard kapslid) määratakse 1 hommikul. Lahust määratakse esimese 2-3 päeva jooksul 4 ml 3 korda päevas ja seejärel 2 ml 3 korda päevas. Siirupi kujul olevat ravimit soovitatakse täiskasvanutele esimesel 2-3 päeval, 10 ml 3 korda päevas ja seejärel 5 ml 3 korda päevas.
Tabletid 30 mg 50 tk pakendis. Siirup 100 ml viaalides. Määrake 30 mg 2-3 korda päevas.
Samuti on suur hulk kombineeritud ravimeid: Dr IOM, bronholitiin, bronchicum jne.
Praegu on ilmunud ravim, millel on nii põletikuvastane kui ka bronhe laiendav toime. Seda ravimit nimetatakse erespaliks (fenspiriidiks). Erespalomi ravis väheneb hingamisteede obstruktsiooni aste, väheneb eritunud röga hulk, mis on seotud nii moodustumise kui ka sekretsiooni vähenemisega, see tähendab, et ravim toimib liigse lima moodustumise vähendamise mõttes. Saadaval 80 mg tablettidena (30 tabletti pakendis). Ravim on ette nähtud 2-3 tabletti päevas.
Aerosoolravi fütontsiidide ja antiseptikumidega saab läbi viia ultraheliinhalaatorite abil, mis loovad optimaalse osakese suurusega homogeensed aerosoolid, mis tungivad bronhipuu perifeersetesse osadesse. Ravimite kasutamine aerosoolidena tagab nende kõrge lokaalse kontsentratsiooni ja ravimi ühtlase jaotumise bronhipuus. Aerosoolide, antiseptikumide furatsiliini, rivanooli, klorofüllipti, sibula- või küüslaugumahla (lahjendatud novokaiini 0,25% lahusega vahekorras 1:30), kuusetõmmise, pohlalehtede kondensaadi, dioksidiini abil saab sisse hingata. Aerosoolteraapiale järgneb posturaalne drenaaž ja vibratsioonimassaaž.
Kroonilise bronhiidi remissiooniperioodidel võetakse ägenemiste vältimiseks sekundaarseid ennetusmeetmeid. Ravimite eelistatuim ja ohutum manustamisviis on sissehingamine, mis tavaliselt ei põhjusta tõsiseid kõrvalnähte. Selle manustamisviisi korral siseneb bronhodilataator kohe bronhidesse. Inhalaatoreid on palju ja mõõdetud annused on kõige levinumad.
Selleks, et tagada ravimi maksimaalne tungimine hingamisteedesse, on väga oluline kasutada doseeritud inhalaatorit õigesti.
Inhalaatori kasutamise tehnika on järgmine:
Raputage inhalaatorit (ühtlase osakeste suurusega aerosooli saamiseks); eemaldage kaitsekork (paljud patsiendid unustavad seda teha); kallutage oma pead veidi tahapoole (ülemiste hingamisteede pisut sirgendamiseks ja ravimite vaba liikumise tagamiseks bronhidesse); keerake inhalaator tagurpidi (huulik peab olema allapoole); hingake täis.
Sissehingamist alustades vajutage inhalaatori põhja ja hingake ravim sügavalt sisse (vajutage ainult üks kord purgi põhjale). Hoidke hinge kinni 5-10 sekundit (nii et ravim settib bronhide seinale). Hinga rahulikult. Vajadusel korrake manipuleerimist.
Oluline on mõista, et vaatamata heale tervisele on regulaarne ravi vajalik. See on tingitud asjaolust, et protsessi progresseerumine toimub märkamatult, järk-järgult, paljude aastate jooksul. Seega, kui patsiendil on väljendunud heaolu muutused (õhupuudus vähese füüsilise koormuse ja puhkeolekus), on bronhide muutuste protsess juba märkimisväärselt väljendunud. Seetõttu on protsessi progresseerumise peatamiseks vaja ravi alustada võimalikult varakult, see tähendab kohe diagnoosi kindlakstegemise hetkest.
Veel üks punkt, millele tahaksin tähelepanu juhtida, on see, et kroonilise obstruktiivse bronhiidi ravi ei ole õhupuuduse ajutine vähendamine ega episoodiline ravi ühegi ravimiga. Haiguse ravi on teraapia, mida tehakse regulaarselt mitu kuud ja aastaid. Vaid nii saab haiguse progresseerumist pidurdada ning säilitada rahuldav tervislik seisund ja hea kehaline aktiivsus pikka aega.
Kuna kroonilise obstruktiivse bronhiidi tekkes ja progresseerumises mängib peamist rolli bronhide ahenemine, kasutatakse haiguse püsivaks raviks peamiselt bronhe laiendavaid ravimeid. Ideaalne bronhodilataator kroonilise obstruktiivse bronhiidi raviks peaks vastama järgmistele nõuetele: kõrge efektiivsus; kõrvaltoimete minimaalne arv ja raskusaste; tõhususe säilitamine vaatamata pikaajalisele kasutamisele.
Tänapäeval vastavad neile nõuetele kõige enam inhaleeritavad antikolinergilised ravimid. Need toimivad peamiselt suurtele bronhidele. Selle rühma ravimeid iseloomustab väljendunud bronhodilateeriv toime ja minimaalne kõrvaltoimete arv. See sisaldab atroventi, troventooli, truventi.
Need ravimid ei põhjusta värinaid (treemorit), ei mõjuta südame-veresoonkonna süsteemi. Atrovent-ravi alustatakse tavaliselt 2 inhalatsiooniga 4 korda päevas. Bronhiaobstruktsiooni vähenemine ja sellest tulenevalt heaolu paranemine toimub mitte varem kui 7-10 päeva pärast ravi algust. Ravimi dovdokhovi annust on võimalik suurendada päevas. Selle rühma ravimeid kasutatakse põhiliseks pikaajaliseks bronhodilateerivaks raviks. Eelistatav on kasutada vahetükiga mõõdetud annusega inhalaatorit.
Doseeritud aerosool. 300 annust 20 mikrogrammi.
Lühitoimelised inhaleeritavad B-2 agonistid
Neil on ka bronhodilateeriv toime. Need ravimid kroonilise obstruktiivse bronhiidi korral on vähem tõhusad kui antikolinergilised ravimid. Selle rühma preparaate soovitatakse kasutada mitte rohkem kui 3-4 korda päevas või profülaktikana enne füüsilist tegevust. Inhaleeritavate lühitoimeliste beeta-2-agonistide kombineeritud kasutamine kroonilise obstruktiivse bronhiidiga patsientidel on efektiivsem kui ravi sama rühma bronhodilataatoritega.
Ettevaatus on vajalik beeta-2-agonistide rühma ravimite kasutamisel eakatel, eriti südame-veresoonkonna haiguste korral.
Kõrvaltoimed: võimalik käte värisemine, sisemine värisemine, pinge, südamepekslemine, iiveldus, oksendamine.
Selle rühma kõige levinumad ravimid on järgmised.
Berotek (fenoterool). Mõõdetud aerosool sissehingamiseks. 300 inhalatsiooniannust 200 mcg.
Berotek-100 (fenoterool). (Boehringer Ingelheim, Saksamaa). Mõõdetud aerosool, mis sisaldab ravimi väiksemat annust, mcg.
Mõõdetud aerosool 100 mcg annuse kohta.
Ventolin (salbutamool). Aerosoolinhalaator 100 mikrogrammi annuse kohta.
On olemas ravim, mis on nende kahe ravimirühma kombinatsioon.
Berodual (20 mikrogrammi ipratroopiumbromiidi + 50 mikrogrammi fenoterooli). Berodualis sisalduvatel kahel bronhodilataatoril on koos tugevam toime kui kummalgi neist eraldi. Kui kombineeritud ravi inhaleeritavate antikolinergiliste ravimite ja lühitoimeliste beeta-2 agonistidega on ebaefektiivne, võib arst teile soovitada mõnda muud ravimirühma.
Metüülksantiinide rühma peamine esindaja on teofülliin. Sellel on nõrgem bronhodilateeriv toime võrreldes inhaleeritavate antikolinergiliste ja beeta-2-agonistidega. Kuid lisaks bronhodilataatorile on selle rühma ravimitel mitmeid muid omadusi: nad hoiavad ära või vähendavad hingamislihaste väsimust; aktiveerida ripsepiteeli motoorset võimet; stimuleerida hingamist.
Kõrvaltoimed: mao limaskesta ärritus, valu epigastimaalses piirkonnas, iiveldus, oksendamine, kõhulahtisus, agiteeritus, unetus, ärevus, peavalu, värisemine, südamepekslemine, rütmihäired, vererõhu langus.
Teofülliini rühma ravimitest pakuvad suurimat huvi selle laiendatud vormid.
Selles rühmas on välja pakutud suur hulk ravimeid. Neid määrab arst. Annus ja raviskeem sõltuvad haiguse tõsidusest ja mõnest muust individuaalsest tegurist.
I põlvkonna ravimid (2 korda päevas)
Tabletid 0,3 g 50 tk pakendis.
Aeglane täitmine Tabletid 0,1 ja 0,2 g 100 tk pakendis.
Retard kapslid 0,1, 0,2, 0,3 g, 20, 60 ja 100 tk pakendis.
Kapslid 0,125 ja 0,25 g Pakendis 40 tk.
Tabletid 0,2 ja 0,3 g 100 tk pakendis.
II põlvkonna ravimid (võetakse üks kord päevas)
Retard kapslid 0,375 ja 0,25 g 20, 50, 100 tk pakendis.
Teine rühm ravimeid, mida võib soovitada kasutada põhiravina, on glükokortikosteroidid. Kroonilise obstruktiivse bronhiidi korral on need ette nähtud juhtudel, kui hingamisteede obstruktsioon jääb suitsetamisest loobumisest ja optimaalsest bronhodilataatorravist hoolimata raskeks ja põhjustab puude. Arst määrab need ravimid tavaliselt tablettide kujul käimasoleva bronhodilataatoriravi taustal. Selle rühma kõige levinum on prednisoloon.
Kõik ülaltoodud ravimid on põhiteraapia, st kui need on välja kirjutatud, tuleb neid regulaarselt pikka aega võtta. Ainult sel juhul võite loota ravi edule. Soovime veel kord rõhutada suitsetamisest loobumise vajadust kui üht seisundit oluliselt raskendavat ja haiguse progresseerumist kiirendavat tegurit.
Kroonilise bronhiidi korral kasutatakse meetodeid keha mittespetsiifilise resistentsuse suurendamiseks. Sel eesmärgil kasutatakse adaptogeene - eleutherococcus ekstrakti 40 tilka 3 korda päevas, ženšenni tinktuuri 30 tilka 3 korda päevas, aralia tinktuure, Rhodiola rosea, pantocrine samades annustes, saparal 0,05 g 3 korda päevas. Nende ravimite toime on mitmetahuline: neil on positiivne mõju immuunsüsteemi toimimisele, ainevahetusprotsessidele, suurendatakse organismi vastupanuvõimet ebasoodsatele keskkonnamõjudele ja nakkustegurite mõjule.
Allikas: Traditsioonilise ja alternatiivse meditsiini entsüklopeedia
Ravi ja ennetamine
kiiresti mõjutada bronhide obstruktsiooni, parandades patsientide heaolu lühikese aja jooksul. β2-agonistide pikaajalisel kasutamisel tekib nende suhtes resistentsus, pärast ravimite võtmise pausi taastub nende bronhodilateeriv toime. β2-adrenergiliste stimulantide efektiivsuse vähenemist ja sellest tulenevalt bronhide läbilaskvuse halvenemist seostatakse β2-adrenergiliste retseptorite desensibiliseerumisega ja nende tiheduse vähenemisega pikaajalise kokkupuute tõttu agonistidega, samuti agonistide tekkega. "tagasilöögi sündroom", mida iseloomustab terav bronhospasm. "Tagasilöögi sündroom" on põhjustatud bronhide β2-adrenergiliste retseptorite blokeerimisest ainevahetusproduktide poolt ja bronhipuu äravoolufunktsiooni rikkumisest, mis on tingitud "kopsu sulgemise" sündroomi tekkest. KOK-i β2-agonistide kasutamise vastunäidustused on ülitundlikkus ravimi mis tahes komponendi suhtes, tahhüarütmiad, südamerikked, aordi stenoos, hüpertroofiline kardiomüopaatia, dekompenseeritud suhkurtõbi, türeotoksikoos, glaukoom, raseduse katkemise oht. Selle rühma ravimeid tuleb eriti ettevaatlikult kasutada eakatel patsientidel, kellel on kaasuv südamehaigus.
Lühikese (salbutamool, fenoterool) ja pikaajalise (formoterool, salmeterool) toimega b2-agonistide omadused.
Doseeritud inhalaator 100 mcg/inhalatsiooniannus zamkg/6-8 h (maksimaalselt mg päevas) Diskhalermkg/blisterkg/6-8 h (maksimaalselt 1600 mcg/päevas Nebulisaator 2,5-5,0 mg iga 6 tunni järel
Kõige sagedamad kõrvaltoimed on: treemor Peavalu erutus hüpotensioon õhetus hüpokaleemia tahhükardia pearinglus
Doseeritud inhalaator 100 mcg/inhalatsiooniannus x kg/6-8 tundi (maksimaalselt mg päevas) Nebulisaator 0,5-1,25 mg iga 6 tunni järel
Toime algus: 5-10 min Maksimaalne toime: min Toime kestus: 3-6 h
Kõrvaltoimete jälgimine Sümptomite analüüs Vererõhu jälgimine Südame löögisageduse jälgimine Elektrolüütide seire
12 mcg/kapsel 12 mcg/12 tundi (maksimaalselt 48 mcg/päevas)
Toime algus: min Toime kestus: 12 tundi
Mõõteannusega inhalaator 25 mcg/inhaleeritav annus zamkg/12 h (maksimaalselt 100 mcg/24 h) Diskhaler 50 mcg/blister 50 mcg/12 h Diskus 50 mcg/inhaleeritav annus 50 mcg/12 h
Toime algus: 10-2 minutit Toime kestus: 12 tundi
Lisatud ravile kahe esimese ravimirühma ebapiisava efektiivsusega, vähendavad need süsteemset pulmonaalset hüpertensiooni ja suurendavad hingamislihaste tööd.
Nendel ravimitel on väljendunud põletikuvastane toime, kuigi KOK-iga patsientidel on see palju vähem väljendunud kui astmahaigetel. KOK-i ägenemiste raviks kasutatakse lühikesi (10-14 päeva) süsteemsete steroidide kuure. Nende ravimite pikaajaline kasutamine ei ole soovitatav kõrvaltoimete (müopaatia, osteoporoos jne) ohu tõttu.
On näidatud, et need ei mõjuta bronhide läbilaskvuse progresseeruvat vähenemist KOK-iga patsientidel. Nende suured annused (nt flutikasoonpropionaat 1000 mikrogrammi päevas) võivad parandada patsientide elukvaliteeti ja vähendada raske ja üliraske KOK-i ägenemiste sagedust.
Hingamisteede põletiku suhtelise steroidresistentsuse põhjused KOK-i korral on intensiivse uurimise objektiks. Võib-olla on see tingitud asjaolust, et kortikosteroidid pikendavad neutrofiilide eluiga, pärssides nende apoptoosi. Glükokortikoidiresistentsuse aluseks olevad molekulaarsed mehhanismid ei ole hästi teada. On teatatud steroidide sihtmärgiks oleva histooni deatsetülaasi aktiivsuse vähenemisest suitsetamise ja vabade radikaalide mõjul, mis võib vähendada glükokortikoidide inhibeerivat toimet "põletikuliste" geenide transkriptsioonile ja nõrgendada nende antiaktiivsust. - põletikuline toime.
SÜNDROOMID JA HINGAMISTEED HAIGUSED.
5.1 BRONHIAALSE ASTMA UURIMINE
Bronhiaalastma on kroonilisel allergilisel põletikul ja bronhide hüperreaktiivsusel põhinev haigus, mis kliiniliselt väljendub ajas muutuva bronhide obstruktsioonina. Korduvad episoodid, obsessiivne mitteproduktiivne köha, eriti öösel ja/või varahommikul, on bronhipuu tavalise, kuid varieeruva obstruktsiooni sümptomid, mis on osaliselt pöörduvad spontaanselt või kaovad ravi mõjul.
Tuntud on neli hingamisteede obstruktsiooni mehhanismi:
silelihaste spasmid;
Hingamisteede limaskesta turse;
Hüpersekretsioon koos limaskestade pistikute moodustumisega;
Bronhide seina skleroos koos pika ja raske haiguse kulgemisega.
Seega on BA krooniline allergiline hingamisteede põletik, mis põhjustab bronhide hüperreaktiivsust, bronhide ahenemisest tingitud bronhide obstruktsiooni, limaskesta turset ja viskoosse sekretsiooni obstruktsiooni, mis kliiniliselt väljendub hingamisteede sümptomitega.
AD diagnostilised kriteeriumid
BA diagnoos haiglaeelses staadiumis tehakse kaebuste, haiguse anamneesi ja kliinilise läbivaatuse põhjal.
1. Kaebused ja haiguslugu.
Astmahoogude või õhupuuduse esinemine, vilistav hingamine, köha ja nende kadumine spontaanselt või pärast bronhodilataatorite ja põletikuvastaste ravimite kasutamist. Nende sümptomite seos astma riskifaktoritega (vt astma riskifaktorid). Patsiendil või tema lähedastel on anamneesis väljakujunenud astma või muud allergilised haigused.
2. Kliiniline läbivaatus.
Sundasend, abihingamislihaste osalemine hingamistegevuses, kuivad räiged, mida kuuldakse eemalt ja/või kopsude kohal auskultatsiooni ajal.
Maksimaalse voolumõõturi või spiromeetri juuresolekul (kaasa arvatud patsient) registreeritakse märkimisväärne bronhide obstruktsioon – sunnitud väljahingamise maht 1 sekundis (FEV1) või maksimaalne väljahingamise voolukiirus (PSV) on alla 80% õigest või normaalväärtusest.
Astma ägenemise kriteeriumid
Astma ägenemine võib esineda ägeda rünnaku või bronhide obstruktsiooni pikaajalise seisundi kujul.
Astmahoog on ägedalt arenenud ja/või progresseeruvalt süvenev väljahingamise hingeldus, vaevaline ja/või vilistav hingamine, spasmiline köha või nende sümptomite kombinatsioon, millega kaasneb väljahingamise tippvoolukiiruse järsk vähenemine.
Ägenemist bronhide obstruktsiooni pikaajalise seisundi vormis iseloomustab pikaajaline (päevad, nädalad, kuud) hingamisraskused koos kliiniliselt väljendunud bronhiaalobstruktsiooni sündroomiga, mille vastu võivad korduda erineva raskusastmega BA ägedad rünnakud.
Bronhiaalastma ägenemised on peamine hädaabikõnede ja patsientide haiglaravi põhjus.
Astma ägenemist hinnatakse kliiniliste tunnuste ja (tippvoolumõõturi olemasolul) funktsionaalsete hingamisteede testide põhjal. Ägenemine võib olla kerge, mõõdukas, raske ja astmaatilise seisundi vormis.
Tabel 1. Astma ägenemise raskusastme klassifikatsioon * .
Järsult vähendatud, sundasend
Järsult vähenenud või puudub
Ei muutunud, vahel erutus
Erutus, hirm, "hingamispaanika"
Teadvuse segadus, kooma
Piiratud, räägib üksikuid fraase
Normaalne hingamissagedus ärkvel lastel (hingamissagedus minutis)
Normaalne või kiirendatud kuni 30% normist
Raske väljahingamise düspnoe. Rohkem kui 30-50% normist
Väljendunud väljahingamise düspnoe üle 50% normist
Tahhüpnoe või bradüpnoe
Lisahingamislihaste kaasamine;
kägiõõne tagasitõmbamine
Ei hääldata
Paradoksaalne rindkere-kõhu hingamine
Hingamine auskultatsioonil
Vilistav hingamine, tavaliselt väljahingamise lõpus
Tugev vilistav hingamine sisse- ja väljahingamisel või mosaiikne hinge kinnipidamine
Tugev vilistav hingamine või vähenenud juhtivus
Hingamishelide puudumine, "vaikne kops"
Normaalne südame löögisagedus ärkvel lastel (bpm)
PSV ** (% normist või parim individuaalne näitaja)
Bronhodilataatorite võtmise sagedus viimases
Kasutatud ei ole või madalaid/keskmisi annuseid. Efektiivsus on ebapiisav, vajadus on suurenenud võrreldes individuaalse normiga
Kasutatud on suuri annuseid.
* – ägenemise raskust näitab vähemalt mitme parameetri olemasolu
** - PSV - kasutatakse täiskasvanutel ja üle 5-aastastel lastel
***-Praegu määratakse peamiselt haiglas
Tabel 2. Laste hingamisfunktsiooni näitajate standardid
Haiglaeelse ravi taktika määrab täielikult BA ägenemise raskusaste, seetõttu on SS ja NMP arsti poolt diagnoosi koostamisel vaja näidata BA ägenemise raskusastet.
Arsti taktikal bronhiaalastma hoo ravimisel on mitmeid üldpõhimõtteid:
Uurimisel peab arst hindama ägenemise raskust vastavalt kliinilistele andmetele, määrama PSV (kui on olemas tippvoolumõõtur).
Võimaluse korral piirake kokkupuudet põhjuslikult oluliste allergeenide või vallandajatega.
Vastavalt anamneesile täpsustage eelnev ravi:
bronhospasmolüütilised ravimid, manustamisviisid; annus ja vastuvõtu sagedus;
viimase ravimi võtmise aeg; kas patsient saab süsteemseid kortikosteroide, millistes annustes.
Välistage tüsistused (nt kopsupõletik, atelektaas, pneumotooraks või pneumomediastinum).
Sõltuvalt rünnaku tõsidusest osutage kiirabi.
Hinnake teraapia mõju (õhupuudus, pulss, vererõhk. PSV tõus> 15%).
Ravimi valik, annus ja manustamisviis
Astma ägenemisega patsientide kaasaegne ravi hõlmab ainult järgmiste ravimirühmade kasutamist:
1. Lühitoimeliste adrenergiliste retseptorite selektiivsed beeta-2-agonistid (salbutamool, fenoterool).
2. Antikolinergilised ained (ipratroopiumbromiid); nende kombineeritud ravim berodual (fenoterool + ipratroopiumbromiid).
Selektiivsed lühitoimelised beeta-2 agonistid.
Need ravimid, millel on bronhospasmolüütiline toime, on esmavaliku ravimid astmahoogude ravis.
SALBUTAMOL (ventoliin, salben, ventoliini udukesed ja 0,1% salgimi lahus nebulisaatorraviks) on selektiivne beeta-2 adrenoretseptori agonist.
Salbutamooli bronhodilateeriv toime ilmneb 4-5 minuti pärast. Ravimi toime suureneb järk-järgult minuti jooksul maksimumini. Poolväärtusaeg on 3-4 tundi ja toimeaeg 4-5 tundi.
Rakendusviis : Kasutades nebulisaatorit, 2,5 ml pihustid, mis sisaldavad 2,5 mg salbutamoolsulfaati soolalahuses. Inhaleerimiseks lahjendamata kujul on ette nähtud 1-2 udu (2,5 - 5,0 mg). Kui paranemist ei toimu, tehakse korduvad salbutamooli 2,5 mg inhalatsioonid iga 20 minuti järel ühe tunni jooksul. Lisaks kasutatakse ravimit PDI (spacer), spacer või dishaler (100 mikrogrammi 1-2 hingetõmbe sissehingamise kohta) või tsüklohaleri (200 mcg 1 sissehingamise kohta) kujul.
FENOTEROL (Berotek) ja Berotek lahus nebulisaatorraviks on lühitoimeline selektiivne beeta-2-agonist. Bronhodilateeriv toime ilmneb 3-4 minutiga ja saavutab maksimaalse toime 45 minuti pärast. Poolväärtusaeg on 3-4 tundi ja fenoterooli toime kestus on 5-6 tundi.
Kasutusviis: Nebulisaatori kasutamine - 0,5-1,5 ml fenoterooli lahust soolalahuses 5-10 minutit. Kui paranemist ei toimu, korrake ravimi sama annuse sissehingamist iga 20 minuti järel. Lapsed 0,5-1,0 ml (10-20 tilka) 1 inhalatsiooni kohta. Berotekit kasutatakse ka PAI kujul (100 mcg 1-2 hingetõmbeks).
Kõrvalmõjud. Beeta-2-agonistide kasutamisel on võimalik käte värisemine, agiteeritus, peavalu, südame löögisageduse kompenseeriv tõus, südame rütmihäired, arteriaalne hüpertensioon. Kõrvaltoimeid on rohkem oodata kardiovaskulaarsüsteemi haigustega patsientidel, vanematel vanuserühmadel ja lastel; bronhospasmolüütikumi korduva kasutamise korral sõltuvad ravimi annusest ja manustamisviisist.
Suhtelised vastunäidustused inhaleeritavate beeta-2-agonistide kasutamine - türotoksikoos, südamerikked, tahhüarütmia ja raske tahhükardia, äge koronaarpatoloogia, dekompenseeritud suhkurtõbi, ülitundlikkus beeta-agonistide suhtes.
Ipratroopiumbromiid (atrovent) on antikolinergiline aine, mille biosaadavus on väga madal (alla 10%), mis tagab ravimi hea talutavuse. Ipratroopiumbromiidi kasutatakse beeta-2-agonistide ebaefektiivsuse korral täiendava vahendina nende bronhodilateeriva toime tugevdamiseks, individuaalse talumatuse korral beeta-2-agonistide suhtes kroonilise bronhiidiga patsientidel.
Kasutusviis: Sissehingamine - nebulisaatori abil - 1,0 - 2,0 ml (0,25 - 0,5 mg). Vajadusel korrake iga minuti järel PDI või vahetüki abil.
BERODUAL on kombineeritud bronhospasmolüütiline ravim, mis sisaldab kahte bronhodilataatorit, fenoterooli ja ipratroopiumbromiidi. Üks beroduali annus sisaldab 0,05 mg fenoterooli ja 0,02 mg ipratroopiumbromiidi.
Kasutusviis: Rünnaku peatamiseks nebulisaatori abil inhaleeritakse 1-4 ml beroduali lahust soolalahuses 5-10 minutit. Kui paranemist ei toimu, korrake sissehingamist 20 minuti pärast. Ravimi annus lahjendatakse soolalahuses. Vajadusel DAIVdohi abiga 5 minuti pärast - veel 2 annust, tuleb järgnev sissehingamine läbi viia mitte varem kui 2 tunni pärast.
raske ja eluohtlik astma ägenemine
astmahoo leevendamine hormoonsõltuva astmavormiga patsiendil
anamnestilised märgid vajaduse kohta kasutada glükokortikoide astma ägenemise leevendamiseks minevikus.
Kõrvalmõjud: arteriaalne hüpertensioon, agitatsioon, arütmia, haavandite verejooks
Vastunäidustused: mao ja kaksteistsõrmiksoole peptiline haavand, raske arteriaalne hüpertensioon, neerupuudulikkus.
Prednisoloon on hüdrokortisooni dehüdrogeenitud analoog ja kuulub sünteetiliste glükokortikosteroidhormoonide hulka. Poolväärtusaeg on 2-4 tundi, toimeaeg on tundi. Seda manustatakse täiskasvanutele parenteraalselt annuses vähemalt 60 mg, lastele - parenteraalselt või suukaudselt 1-2 mg / kg.
METÜLPREDNISOLOON (solumedrol, metipred) Prednisolooni halogeenimata derivaat, millel on suurem põletikuvastane toime (5 mg prednisolooni võrdub 4 mg metüülprednisolooniga) ja oluliselt väiksem mineralokortikoidne aktiivsus.
Ravimit iseloomustab lühike, nagu prednisolooni, poolväärtusaeg, nõrgem psüühika ja söögiisu stimulatsioon. Bronhiaalastma ägenemiste raviks kasutatakse seda nagu prednisolooni, kuid väiksemates annustes (põhineb metüülprednisolooni-prednisolooni vahekorras 4:5).
Inhaleeritavad glükokortikoidid (budesoniid) võivad olla tõhusad. Inhaleeritavaid glükokortikoide on soovitav kasutada läbi nebulisaatori.
BUDESONIDE (pulmicort) - suspensioon nebulisaatori jaoks plastmahutites 0,25-0,5 mg (2 ml).
Budesoniidi biotransformatsiooni käigus maksas moodustub see madala glükokortikosteroidse aktiivsusega metaboliite.
Pulmicorti suspensiooni nebulisaatori jaoks võib lahjendada soolalahusega, samuti segada salbutamooli ja ipratroopiumbromiidi lahustega. Täiskasvanute annus on 0,5 mg (2 ml), lastele - 0,5 mg (1 ml) kaks korda iga 30 minuti järel.
EUFILLIN on kombinatsioon teofülliinist (80%), mis määrab ravimi farmakodünaamika, ja etüleendiamiinist (20%), mis määrab selle lahustuvuse. Teofülliini bronhodilateeriva toime mehhanismid on hästi teada.
Vältimatu abi osutamisel manustatakse ravimit intravenoosselt, samal ajal kui toime algab kohe ja kestab kuni 6-7 tundi. Teofülliinile on iseloomulik kitsas terapeutiline laiuskraad, s.t. Isegi ravimi väikese üleannustamise korral võivad tekkida kõrvaltoimed. Poolväärtusaeg täiskasvanutel. Umbes 90% manustatud ravimist metaboliseerub maksas, metaboliidid ja muutumatul kujul (7-13%) erituvad neerude kaudu uriiniga. Noorukitel ja suitsetajatel kiireneb teofülliini metabolism, mis võib nõuda ravimi annuse ja infusioonikiiruse suurendamist. Maksafunktsiooni häired, südame paispuudulikkus ja vanadus, vastupidi, aeglustavad ravimi metabolismi, suurendavad kõrvaltoimete riski ja nõuavad annuse vähendamist ja aminofülliini intravenoosse infusiooni kiiruse vähendamist.
Näidustused kasutamiseks BA-s:
astmahoo leevendamiseks inhaleeritavate ainete puudumisel või täiendava ravina astma raske või eluohtliku ägenemise korral.
südame-veresoonkonna süsteemi poolt - vererõhu langus, südamepekslemine, südame rütmihäired, kardialgia
seedetraktist - iiveldus, oksendamine, kõhulahtisus;
kesknärvisüsteemi küljelt - peavalu, pearinglus, treemor, krambid.
Koostoime (vt tabel 3)
ravim ei sobi kokku glükoosilahusega.
Annus lastele: 4,5-5 mg/kg intravenoosselt (manustatakse mõne minuti jooksul) soolalahuses.
Nebulisaatorravi eesmärk on toimetada ravimi terapeutiline annus aerosooli kujul otse patsiendi bronhidesse ja saada lühikese aja jooksul (5-10 minutit) farmakodünaamiline reaktsioon.
Nebulisaatorravi viiakse läbi spetsiaalse seadmega, mis koosneb nebulisaatorist endast ja kompressorist, mis tekitab 2-5 mikroni suuruste osakeste voolu kiirusega vähemalt 4 l / min.
Sõna "nebulisaator" pärineb ladinakeelsest sõnast nebula, mis tähendab udu. Nebulisaator on seade vedeliku muundamiseks aerosooliks, milles on eriti peened osakesed, mis on võimelised tungima peamiselt perifeersetesse bronhidesse. See protsess viiakse läbi suruõhu mõjul läbi kompressori (kompressornebulisaator) või ultraheli mõjul (ultraheli nebulisaator).
Nebulisaatorravi, mis loob ravimi kõrge kontsentratsiooni kopsudes, ei nõua sissehingamise kooskõlastamist sissehingamise toiminguga, millel on PAI ees märkimisväärne eelis.
Sissehingamise efektiivsus sõltub aerosooli annusest ja selle määravad mitmed tegurid:
Toodetud aerosooli kogus
sissehingamise ja väljahingamise suhe
hingamisteede anatoomia ja geomeetria
Katseandmed näitavad, et 2–5 mikronise osakese läbimõõduga aerosoolid on optimaalsed hingamisteedesse sattumiseks ja seega soovitatavad. Väiksemad osakesed (alla 0,8 mikroni) sisenevad alveoolidesse, kus need imenduvad kiiresti või hingatakse välja ilma hingamisteedes viibimata, ilma ravitoimet andmata. Suuremad osakesed (üle 10 mikroni) settivad orofarünksis. Tänu nebulisaatorravile saavutatakse raviainete kõrgem terapeutiline indeks, mis määrab ravi efektiivsuse ja ohutuse.
vajadus kasutada suuri ravimeid;
ravimi sihipärane kohaletoimetamine hingamisteedesse;
kui tavapäraste ravimite annuste kasutamisel esineb tüsistusi ning inhaleeritavate kortikosteroidide ja teiste põletikuvastaste ravimite kasutamise sagedus on kõrge;
lastel, eriti esimestel eluaastatel;
Seisundi tõsidus (tõhusa inspiratsiooni puudumine)
pole vaja hingamist aerosooli sissevõtmisega kooskõlastada;
võimalus kasutada ravimi suuri annuseid ja saada lühikese aja jooksul farmakodünaamiline reaktsioon;
· meditsiinilise aerosooli pidev varustamine peenosakestega;
Seisundi kiire ja märkimisväärne paranemine tänu ravimaine tõhusale sisenemisele bronhidesse;
kerge sissehingamise tehnika.
Nebulisaatorravi preparaate kasutatakse spetsiaalsetes konteinerites, udukogudes, aga ka klaasviaalides toodetud lahustes. See võimaldab ravimit lihtsalt, õigesti ja täpselt doseerida.
Nebulisaatori kaudu sissehingamiseks peate:
valage vedelik udukogust või tilgutage lahus viaalist (ravimi ühekordne annus);
Lisage füsioloogilist soolalahust vajaliku mahuni 2-3 ml (vastavalt nebulisaatori juhistele;
kinnita huulik või näomask;
Lülitage kompressor sisse, ühendage nebulisaator ja kompressor;
Tehke sissehingamine, kuni lahus on täielikult tarbitud;
Lastel eelistatakse sissehingamist suu kaudu huuliku abil;
Esimeste eluaastate lastel võib kasutada liibuvat maski.
Nebulisaatori esmane desinfitseerimine toimub alajaamas. Selleks on vaja nebulisaator lahti võtta, loputada düüsid sooja vee ja pesuvahendiga ning kuivatada (harja ei saa kasutada). Seejärel steriliseeritakse nebulisaator ja düüsid autoklaavis temperatuuril 120 °C ja 1,1 atmosfääri (OST5).
Nebulisaatorite tehniline kontroll toimub kord aastas.
Tabel 3. Astma ägenemise ravi haiglaeelses staadiumis
ventolin 2,5 mg (1 udukogu) või salgim 2,5 mg (1/2 pudelit) läbi nebulisaatori 5-10 minutiks;
berodual 1-2 ml (20-40 tilka) läbi nebulisaatori 5-10 minutit;
.
ventolin 1,25-2,5 mg (1/2-1 udu) läbi nebulisaatori 5-10 minutiks või salgim 1,25-2,5 mg (1/4-1/2 viaal).
berodual 0,5 ml - 10 tilka. (alla 6-aastased lapsed) ja 1 ml - 20 tilka (üle 6-aastased lapsed) läbi nebulisaatori 5-10 minuti jooksul;
Hinnake ravi 20 minuti pärast
nom mõju, korrake sarnast bronhodilataatori sissehingamist.
ventolin 2,5-5,0 mg (1-2 udukest) või salgim 2,5-5,0 (1/2-1 viaal) mg nebulisaatori kaudu 5-10 minutiks
berodual 1-3 ml (20-60 tilka) läbi nebulisaatori 5-10 minutit;
suukaudne prednisoloon, IV 60-90 mg või metüülprednisoloon IV; või pulmicort läbi nebulisaatori MGK (1-2 udu) 5-10 minutit
Hinnake ravi 20 minuti pärast
Kui toime ei ole rahuldav, korrake sarnast bronhodilataatori sissehingamist
ventolin 2,5 mg (1 udukogu) läbi nebulisaatori 5-10 minutit või salgim (1/2 viaali)
berodual 0,5 ml - 10 tilka. alla 6-aastastel lastel ja 1 ml - 20 tilka (üle 6-aastastel lastel) läbi nebulisaatori 5-10 minuti jooksul;
prednisoloon - suukaudne; IV 1 mg/kg
pulmicort (1/2-1 nebulamkg) läbi nebulisaatori 5-10 minutit;
Hinnake ravi 20 minuti pärast
Kui toime ei ole rahuldav, korrake sarnast bronhodilataatori sissehingamist
Laste haiglaravi
ventolin, salgim või berodual samades annustes ja suukaudne prednisoloon, intramuskulaarne mg (või intravenoosne metüülprednisoloon ja pulmicort läbi nebulisaatori mcg 1-2 udu 5-10 minuti jooksul.
Ventolin või salgim või berodual samades annustes ja prednisoloon lastele - i.vmg või suukaudselt 1-2 mg/kg
pulmicort läbi nebulisaatori 000 mcg 5-10 minutit.
Hospitaliseerimine haiglas
ventolin, salgim või berodual samades annustes ja intravenoosne prednisoloon (või intravenoosne metüülprednisoloon ja pulmicort läbi nebulisaatori μg 1-2 udukest 5-10 minuti jooksul);
Kui see on ebaefektiivne, trahhea intubatsioon, mehaaniline ventilatsioon
ventolin või salgim või berodual samades annustes ja prednisoloon lastele - vähemalt mg IV või 1-2 mg/kg suukaudselt
pulmicort läbi nebulisaatori 5-10 minutit;
Hingetoru intubatsioon, IVL
2. Hospitaliseerimine intensiivraviosakonnas
* Raske ägenemise ja hingamisseiskuse ohu korral ravi ebaefektiivsuse tõttu on täiskasvanutele võimalik manustada subkutaanselt 0,1–0,5 ml adrenaliini. Lapsed 0,01 ml/kg, kuid mitte üle 0,3 ml
** Nebulisaatorite puudumisel või patsiendi püsival soovil on võimalik manustada 10 minuti jooksul intravenoosselt aminofülliini 2,4% lahust 10,0-20,0 ml.
*** Eluohtlikud nähud: tsüanoos, vaikne kops, hingamise nõrgenemine, üldine nõrkus, vanematel lastel on PSV alla 33%. Sel juhul kohene haiglaravi, beeta-2 agonistide kasutamine vajalikus annuses ja sageduses, suukaudne prednisoloon, hapnikravi
Ravi efektiivsuse kriteeriumid:
1. "Hea" loetakse vastuseks käimasolevale ravile, kui:
seisund on stabiilne, vähenenud on õhupuudus ja kuivad rähad kopsudes; PSV
suurenenud 60 l / min, lastel - 12-15% esialgsest.
2. Mittetäielikuks vastuseks käimasolevale ravile loetakse, kui:
seisund on ebastabiilne, sümptomid on samad, piirkonnad
halb hingamine, PSV suurenemine puudub.
3. „Halb” on reaktsioon käimasolevale ravile, kui:
endise astme või suurenemise sümptomid, PSV süveneb.
Tabel 4. Bronhiaalastma raviks
hingamisdepressioon, mis on tingitud tsentraalsest lihasrelaksandist
hingamiskeskuse depressioon
1. põlvkonna antihistamiinikumid
raskendavad bronhide obstruktsiooni, suurendades röga viskoossust, difenhüdramiini afiinsus H1-histamiini retseptorite suhtes on oluliselt madalam kui histamiinil endal, juba retseptoritega seondunud histamiin ei tõrju välja, vaid on ainult ennetav toime, histamiin ei mängivad juhtivat rolli bronhiaalastma rünnaku patogeneesis.
Toime ei ole tõestatud, on näidatud ainult piisavat rehüdratsiooni, et täita vedelikukadu higiga või suurenenud diureesi tõttu pärast aminofülliini kasutamist
Mittesteroidsed põletikuvastased ravimid (aspiriin)
vastunäidustatud "aspiriini" astma korral, aspiriini talumatuse oht
LEVIKUD RAVIVEAD.
Astma ägenemise korral ei ole mitteselektiivsete beeta-agonistide, nagu ipradol ja astmapent, kasutamine kõrvaltoimete suure riski tõttu ebasoovitav. Bronhiaobstruktsiooni ravis on traditsiooniliselt kasutatavad antihistamiinikumid (difenhüdramiin jne) ebaefektiivsed, kuna nende afiinsus H 1 -histamiini retseptorite suhtes on palju madalam kui histamiinil endal ja nad ei tõrju välja retseptoritega juba seondunud histamiini. Lisaks ei mängi histamiin astmahoo patogeneesis juhtivat rolli. Kuigi adrenaliini kasutamine on tõhus, on sellel tõsiseid kõrvaltoimeid. Praegu, kui selektiivsete agonistide valik on suur, on epinefriini kasutamine õigustatud ainult anafülaksia raviks. Korglikooni kasutamine on ebamõistlik parema vatsakese puudulikkuse ebaefektiivsuse tõttu. Korglikooni ja eufilliini kombinatsioon suurendab digitaalise arütmiate (sh ventrikulaarsete arütmiate) tekkeriski. Lisaks puudub seos annuse ja südameglükosiidide mõju vahel siinussõlme aktiivsusele, mistõttu on nende mõju siinusrütmis südame löögisagedusele ettearvamatu.
Kaasaegsete kontseptsioonide kohaselt on hüdratsioon suurte vedelikukoguste sisseviimisega ebaefektiivne (ainult rehüdratsioon täiendab vedelikukaotust higiga või suurenenud diureesi tõttu pärast aminofülliini kasutamist).
Narkootiliste analgeetikumide kasutamine on hingamiskeskuse rõhumise ohu tõttu absoluutselt vastuvõetamatu. Atropiini kasutamine ei ole soovitatav ka bronhide äravoolufunktsiooni võimaliku rikkumise tõttu, mis on tingitud mukotsiliaarse süsteemi pärssimisest ja sekretsiooni viskoossuse suurenemisest bronhides.
Magneesiumsulfaadil on teatud bronhodilataatorid, kuid selle kasutamine astmahoogude leevendamiseks ei ole soovitatav.
Astmahooga kaasnevad sageli tõsised emotsionaalsed häired (surmahirm jne), kuid trankvilisaatorite kasutamine, mis pärsivad hingamist tsentraalse lihaslõõgasti toime tõttu, on vastunäidustatud.
Lõpuks on ekslik taktika aminofülliini kasutamine pärast piisavat inhalatsiooniravi beeta-2-agonistidega, samuti korduvaid intravenoosseid süstimisi (eriti pikaajaliselt teofülliine saavatel patsientidel) - sellise ravi kõrvaltoimete (tahhükardia, arütmia) risk ületab aminofülliini manustamisest saadav kasu. Glükokortikoidide hiline manustamine (sageli ebapiisavates annustes) võib sellises olukorras olla tingitud liialdatud hirmust nende kasutamise ees.
NÄIDUSTUSED haiglaraviks:
Haiglaravi on näidustatud patsientidele, kellel on astma tõsine ägenemine ja hingamisseiskus; kiire vastuse puudumisel bronhodilateerivale ravile või patsiendi seisundi edasisele halvenemisele alustatud ravi taustal; pikaajalisel kasutamisel või hiljuti lõpetatud süsteemsete kortikosteroidide kasutamisel. Samuti tuleks haiglasse saata patsiendid, kes on viimase aasta jooksul mitu korda intensiivravi osakonnas viibinud; patsiendid, kes ei järgi astma raviplaani, ja patsiendid, kes põevad vaimuhaigusi.
Nebulisaatorravi efektiivsuse kliiniline näide .
Kopsupõletik (P) on valdavalt bakteriaalse etioloogiaga äge nakkushaigus, mida iseloomustavad kopsude respiratoorsete osade koldelised kahjustused koos intraalveolaarse eksudatsiooniga, mis tuvastatakse füüsilise ja/või röntgenuuringu käigus ning väljenduvad erineva raskusastmega palavikulise reaktsiooni ja mürgistusena.
ETIOLOOGIA JA PATOGENEES .
P on põhjustatud nakkustekitajatest. Levinumad on pneumokokid, gripibatsillid, streptokokid, stafülokokid, mükoplasmad ja klamüüdia. Antibiootikumide, eriti laia toimespektriga antibiootikumide laialdane ja mitte alati põhjendatud kasutamine on toonud kaasa resistentsete tüvede valiku ja antibiootikumiresistentsuse kujunemise. Viirused on samuti võimelised tekitama põletikulisi muutusi kopsudes, mõjutades trahheobronhiaalset puud, luues tingimused pneumotroopsete bakteriaalsete ainete tungimiseks kopsude hingamisteede osadesse.
Peamine nakatumistee on patogeenide tungimise tee õhu kaudu või mikroorganisme sisaldavate eritiste aspiratsioon ülemistest hingamisteedest.
Vähem levinud on patogeenide hematogeenne levikurada (kolmikklapi endokardiit, vaagnaveenide septiline tromboflebiit) ja nakkuse otsene levik naaberkudedest (maksaabstsess) või nakatumine läbitungivate rindkere haavadega.
KLIINILINE PILT JA KLASSIFIKATSIOON.
Sõltuvalt esinemise tingimustest, kliinilisest käigust ja patsiendi immunoloogilise reaktiivsuse seisundist eristatakse järgmisi P tüüpe:
Ambulatoorne (kodune, ambulatoorne)
Haigla (nosokomiaalne, haigla)
Immuunpuudulikkuse seisundite taustal
Seda klassifikatsiooni kasutatakse empiirilise teraapia õigustamiseks. P-i täpsustamine, võttes arvesse riskitegureid (krooniline alkoholimürgistus, KOK-i taustal, viirusnakkused, pahaloomulised ja süsteemsed haigused, krooniline neerupuudulikkus, eelnev antibiootikumravi jne), võimaldab arvestada kogu võimalike haigustekitajate ja suurendab antibiootikumravi alustamise sihtmärki
P kliinilise pildi määravad nii patogeeni omadused kui ka patsiendi seisund ning see koosneb kopsuvälistest sümptomitest ning kopsude ja bronhide kahjustuse tunnustest.
1) Bronhopulmonaarne: köha, õhupuudus, valu rinnus, röga, mõnikord hemoptüüs, löökpillide tuim, vesikulaarse või bronhiaalse hingamise nõrgenemine, krepitus, pleura hõõrdumise müra;
2) Ekstrapulmonaalne: hüpotensioon, nõrkus, tahhükardia, higistamine, külmavärinad, palavik, segasus, äge psühhoos, meningeaalsed sümptomid, kroonilise haiguse dekompensatsioon
Kroonilise alkoholimürgistuse või raskete kaasuvate haigustega (suhkurtõbi, südame paispuudulikkus, ajuinfarkt jne) või eakatel patsientidel võivad kopsuvälised sümptomid olla ülekaalus bronhopulmonaarsete sümptomite suhtes.
Kui P lokaliseerub kopsude alumistes osades ja kui protsessi on kaasatud diafragmaalne pleura (kruoposse kopsupõletiku - pleuropneumooniaga), võib valu kiirguda kõhuõõnde, simuleerides ägeda kõhu pilti.
Mõnel juhul tuleb pleuropneumooniat eristada kopsuinfarktist, mida iseloomustab ka äkiline valu, sageli hemoptüüs, lämbumine. Kuid haiguse alguses ei ole kõrge temperatuuri olemasolu ja joobeseisund patognoomilised. Nendel patsientidel on võimalik kindlaks teha võimalikud trombemboolia allikad (alajäsemete tromboflebiit, südamehaigused, infarktijärgne kardioskleroos). EKG registreerimisel ilmnevad parema südame ülekoormuse sümptomid (His-kimbu parema jala blokaad, märk S I -Q III.).
Spontaanse pneumotooraksi korral võib valusündroomi ägedat arengut kombineerida suureneva hingamispuudulikkusega (pingespontaanse pneumotooraksiga). Löökriistad paljastavad tümpaniidi, hingamise nõrgenemise, mõnikord mahu suurenemise ja rindkere vastava poole hingamisteede piiramise.
P tüsistused on pleuriit, abstsessi moodustumine, püopneumotooraks ja pleura empüeem, täiskasvanute respiratoorse distressi sündroom, nakkuslik-toksiline šokk, bronhoobstruktiivne sündroom, vaskulaarne puudulikkus. Rasketel juhtudel koos raske joobeseisundiga võivad nõrgestatud patsientidel tekkida sepsis, infektsioosne endokardiit, müokardi- ja neerukahjustus.
Pneumokokkinfektsiooniga kohustuslikult seostatav lobar-kopsupõletik on üks raskemaid P vorme. Seda iseloomustavad: haiguse äge algus koos tohutute külmavärinatega, köha, valu rinnus hingamisel, roostes röga, selgelt väljendunud löökpillid ja kuulmise muutused. kopsud, kehatemperatuuri kriitiline langus; hüpotensiooni võimalik areng, äge vaskulaarne puudulikkus, hingamispuudulikkus - täiskasvanute sündroom, nakkus-toksiline šokk.
Stafülokoki P-ga, mida esineb sagedamini gripiepideemia ajal, tekib raske mürgistus ja mädased tüsistused.
Eakatel ja alkoholisõltuvusega inimestel põhjustab neid sageli gramnegatiivne taimestik, eriti Klebsiella pneumoniae. Nende P-ga kaasneb ulatuslik kopsukoe kahjustus koos hävimise, mädaste tüsistuste ja joobeseisundiga.
KÜSIMUSTE LOETELU PNEUMOONIGA PATSIENDILE.
1) Haiguse alguse aeg.
2) riskitegurite olemasolu, mis raskendavad P kulgu
Kroonilised haigused, halvad harjumused jne.
3) Epidemioloogilise ajaloo selgitamine.
Võimaliku nakkushaiguse tunnuste tuvastamine.
4) Temperatuuri tõusu kestus ja iseloom.
5) Köha, röga olemasolu, selle olemus, hemoptüüs.
6) Valu olemasolu rinnus, selle seos hingamisega, köhimine
7) Kas esineb õhupuudust, astmahooge
PNEUMOONIA DIAGNOSTIKAKRITEERIUMID.
1. Patsiendi kaebused köha, röga, valu rinnus, õhupuuduse kohta
2. Haiguse äge algus
3. Muutused kopsude löökpillides (löökpillide heli tuhmus) ja auskultatsioonis (vesikulaarse hingamise nõrgenemine, bronhide hingamine, krepitus, pleura hõõrdumise müra), bronhide obstruktsiooni ilmingud
4. Temperatuuri tõus
5. Mürgistuse sümptomid
Patsiendi uurimisel on vaja mõõta temperatuuri, hingamissagedust, vererõhku, südame löögisagedust; kõhu palpeerimiseks, kaasuvate haiguste dekompensatsiooni sümptomite tuvastamiseks.
Kui kahtlustate AMI-d, PE-d vanemas eas, samaaegse ateroskleroosiga, on vaja läbi viia EKG-uuring.
Pneumoonilise infiltratsiooni tuvastamine radiograafilise uuringu käigus kinnitab P diagnoosi.
Patsiendi seisundi raskusastme hindamisel ja ravi valikul on olulised laboratoorsed andmed (perifeerse vere analüüs, biokeemilised uuringud), veregaasi koostise määramine.
Röga tsütoloogiline uurimine võimaldab teil selgitada põletikulise protsessi olemust ja selle raskust.
Antibiootikumravi korrigeerimiseks on oluline röga, bronhide sisu, vere bakterioloogiline uuring, eriti raske P.
Kliiniline näide. 44-aastane patsient V. helistas SS-i ja NMP meeskonda, kuna tekkisid äkilised külmavärinad, palavik kuni 38,5, teravad valud paremal küljel, mida süvendavad hingamine ja liikumine. Alkoholi kuritarvitamise ajalugu.
Ta viidi ägeda koletsüstiidi diagnoosiga haiglasse. Vastuvõtuosakonnas läbivaatusel välistati kirurgiline patoloogia, kuid kopsude alumises osas selgus löökpillide heli tuhmus, samuti hingamise suurenemine ja bronhofoonia. Kiirabi arst kahtlustas kopsupõletikku. Röntgenuuring kinnitas alumise sagara pro-sided pleuropneumoonia diagnoosi. Seega antud juhul kiirgas parempoolse pleuropneumooniaga patsiendil pleura valu paremasse hüpohondriumisse ja jäljendas ägeda koletsüstiidi pilti.
LUTS-i arsti jaoks on suure tähtsusega P jaotus raskusastme järgi, mis võimaldab tuvastada haiglaeelses staadiumis haiglaravi ja intensiivravi vajavad patsiendid. Haiguse raskusastme peamised kliinilised kriteeriumid on hingamispuudulikkuse aste, mürgistuse raskusaste, tüsistuste esinemine, kaasuvate haiguste dekompensatsioon.
Raske kopsupõletiku kriteeriumid (Niederman et al., 1993).
1. NPV > 30 minutis.
2. Temperatuur üle 38,5 C
3. Ekstrapulmonaalsed infektsioonikolded
4. Teadvuse rikkumine
5. Mehaanilise ventilatsiooni vajadus
6. Šokiseisund (SBP alla 90 mmHg või DBP alla 60 mmHg)
7. Vajadus kasutada vasopressoreid kauem kui 4 tundi.
8. Diurees< 20 мл/ч или проявления острой почечной недостаточности.
Haiglaravile kuuluvad ka patsiendid, kellel on tüsistuste ja surma riskifaktorid.
Riskifaktorid, mis suurendavad kopsupõletikust tingitud tüsistuste ja suremuse tõenäosust (Niederman et al., 1993).
1. Krooniline obstruktiivne kopsuhaigus
2. Diabeet
3. Krooniline neerupuudulikkus
4. Vasaku vatsakese südamepuudulikkus
5. Krooniline maksapuudulikkus
6. Eelmise aasta haiglaravid.
7. Neelamise rikkumine
8. Kõrgemate närvifunktsioonide rikkumine
12. Vanus üle 65 aasta
Mõõduka ja raske P-ga patsiendid, kellel on keeruline kulg, riskifaktorite olemasolul kuuluvad haiglaravile. Mõnedel haiglaeelses staadiumis patsientidel võivad tekkida sümptomid, mis nõuavad LUTS-i arsti korrigeerimist.
ARSTI LUTS TAKTIKA ALGORITM PNEUMOONIAS
Arteriaalne hüpotensioon patsientidel, kellel on krupoosne P (pleuropneumoonia), tekib arterioolide ja väikeste arterite seinte silelihaste toonuse üldise vähenemise ja perifeerse koguresistentsuse vähenemise tõttu. Mõnede autorite arvates on selle põhjuseks veresoonte seina kohene reaktsioon sensibiliseeritud organismi anafülaktilise reaktsiooni ajal pneumokoki lagunemissaadustele, mis sel juhul ei toimi mitte toksiinide, vaid antigeenidena. Enne haiglaravi ei tohi alustada antibiootikumravi, määrata palavikku alandavaid või valuvaigisteid, sest see võib põhjustada vererõhu langust, mis on eriti ohtlik patsiendi transportimisel.
SBP säilimise tagamiseks 100 mm Hg tasemel. sisestatakse vedelikud (naatriumkloriidi, dekstroosi, dekstraani 40 isotoonilised lahused kogumahus 0 ml).
Äge hingamispuudulikkus – täiskasvanute respiratoorse distressi sündroom (ARDS). ARDS areneb sagedamini sepsise, bakteriaalse šokiga patsientidel, kellel on P immuunpuudulikkuse taustal (krooniline alkoholimürgistus, neutropeenia, narkomaania, HIV-nakkus). Vastusena infektsioonile tekib lokaalne põletikuline reaktsioon, mis põhjustab vasodilatatsiooni, veresoonte seina läbilaskvuse suurenemist, mitmete rakukomponentide (lüsosomaalsed ensüümid, vasoaktiivsed amiinid, prostaglandiinid) vabanemist ja komplemendi süsteemi aktiveerumine. neutrofiilide meelitamine kopsu mikrotsirkulatsiooni. Granulotsüüdid ja mononukleaarsed rakud kogunevad vigastuskohta ja moodustavad lokaalsete fibroblastide ja endoteelirakkudega konglomeraadi. Neutrofiilide adhesioon endoteeli külge stimuleerib kahjulike toksiliste ainete vabanemist. Kopsukapillaaride endoteeli kahjustuse tagajärjel tekib kopsuturse, mis kliiniliselt väljendub tugevas õhupuuduses ja raskes hüpokseemias, mis on vastupidav hapnikuravile, mis põhjustab suurenenud hapnikuvajadust. Patsiendid vajavad IVL-i. Diureetikumid on ARDS-iga patsientide kopsuturse korral ebaefektiivsed. Furosemiidi sisse- ja sisseviimine võib parandada gaasivahetust, vähendamata kopsuturse taset, mis võib olla tingitud kopsuverevoolu ümberjaotumisest (suurendab seda hästi ventileeritavates kopsupiirkondades).
Teraapia peamine eesmärk hingamispuudulikkuse ravis on kudede hapnikuga varustatuse säilitamine. ARDS-i puhul on hapnikutarbimine perifeerias otseselt võrdeline selle kohaletoimetamisega. Arteriaalse hüpotensiooni ja südame väljundi vähenemise korral on dobutamiini intravenoosne infusioon näidustatud annuses kg/kg min.
Perifeersed vasodilataatorid süvendavad kopsu hüpokseemiat, suurendades kopsusisest šuntimist. Arteriaalse hemoglobiini küllastumist hapnikuga hoitakse üle 90%, mis on piisav hapniku tarnimiseks perifeersetesse kudedesse. Praegu ei peeta tõestatuks, et glükokortikosteroidide kasutamine suurtes annustes nõrgendab kopsude põletikulist protsessi. Samal ajal suurendavad glükokortikosteroidide suured annused sekundaarse infektsiooni tekke riski.
Nakkuslik - toksiline šokk võib komplitseerida krupoosse (pleuropneumoonia), stafülokoki P. kulgu, esineb gramnegatiivse taimestiku poolt põhjustatud P.-l ja riskifaktoritega patsientidel. Ravi haiglaeelses etapis koosneb infusioonravist, dobutamiini kasutuselevõtust. Lisateavet leiate vastavast jaotisest.
Bronho-obstruktiivne sündroom- vaadake vastavat jaotist.
Pleura valu mõnikord väljendatud nii tugevalt, et need nõuavad valuvaigistite kasutuselevõttu. MSPVA-de rühma kuuluvate ravimite kõige ratsionaalsem kasutamine (paratsetamool 0,5 g per os, ibuprofeen - 0,2 g per os; aspiriin 0,5 - 1,0 g per os või parenteraalselt lüsiinmonoatsetüülsalitsülaadi kujul 2,0 g; diklofenak - 0,07 g per os parenteraalselt IM sügavale tuharalihasesse 0,075 g). Endiselt laialdaselt valuvaigistina kasutatav analgin põhjustab tõsiseid kõrvaltoimeid (äge anafülaksia, hematopoeesi pärssimine) palju sagedamini ja seetõttu ei saa seda kasutada.
Krupoosse P-ga (pleuropneumoonia) patsientidel võib valuvaigistite manustamine esile kutsuda hüpotensiooni ja nende kasutamisest on parem hoiduda haiglaeelses staadiumis.
PARATSETAMOOL. Maksimaalne kontsentratsioon veres saavutatakse 0,5-2 tunni pärast pärast manustamist, toime kestus on 3-4 tundi.
Näidustused on kerge kuni mõõdukas valu, temperatuur üle 38 C.
Maksa- ja neeruhaiguste, kroonilise alkoholimürgistuse korral tuleb ravimit kasutada ettevaatusega.
Vastunäidustused on ülitundlikkusreaktsioonid ravimi suhtes ajaloos.
Kõrvaltoimed (areneb harva): nahalööve, tsütopeenia, maksakahjustus (harvemini - neerukahjustus) üleannustamise korral, eriti alkoholi võtmise ajal. Pikaajalisel kasutamisel võib tekkida äge pankreatiit.
Kombineeritud kasutamisel prokineetikaga ja pikaajalisel kombineeritud kasutamisel kaudsete antikoagulantidega on võimalik prokineetiliste ja antikoagulantide toimet tugevdada.
Annused: täiskasvanutele määratakse suu kaudu 0,5-1,0 g iga tund, maksimaalne ööpäevane annus on 4 g.
ASPIRIN (atsetüülsalitsüülhape). Maksimaalne kontsentratsioon veres saavutatakse 2 tundi pärast allaneelamist. Toime kestus 4 tundi.
Näidustused: kerge kuni mõõdukas valu, temperatuur üle 38 C
Astma, anamneesis allergiliste reaktsioonide, maksa- ja neeruhaiguste, dehüdratsiooni, raseduse ajal ja eakatel patsientidel tuleb ravimit kasutada ettevaatusega.
Alla 12-aastastel lastel, imetavatel emadel, peptilise haavandi, hemofiilia, ülitundlikkuse korral aspiriini ja teiste MSPVA-de suhtes, raske neeru- ja maksapuudulikkuse korral ning raseduse 3. trimestril on aspiriini kasutamine vastunäidustatud.
Kõrvaltoimete hulka kuuluvad seedetrakti düspepsia, bronhospasm, nahareaktsioonid. Pikaajalisel kasutamisel on võimalik haavandiline toime, veritsusaja pikenemine, trombotsütopeenia ja ülitundlikkusreaktsioonid.
Kombineerituna teiste MSPVA-de ja glükokortikosteroididega suureneb kõrvaltoimete tekkerisk, antikoagulantidega - verejooksu riski suurenemine. Kombineeritud kasutamine tsütostaatikumide ja epilepsiavastaste ravimitega suurendab nende ravimite toksilisust.
Annused: täiskasvanud - 0,25 - 1,0 g iga tund, maksimaalne annus 4 g / päevas.
Lüsiinmonoatsetüülsalitsülaat on parenteraalseks manustamiseks mõeldud aspiriini derivaat. Ületab selle arengu kiiruse ja valuvaigistava toime tugevuse poolest. Ühekordne annus 2 g, maksimaalne - kuni 10 g päevas. Kõrvaltoimed - sarnased aspiriini toimega.
IBUPROFEEN Maksimaalne kontsentratsioon veres tekib 1-2 tundi pärast allaneelamist, valuvaigistav ja palavikku alandav toime kestab kuni 8 tundi. Ibuprofeen on ette nähtud kerge kuni mõõduka valu korral, temperatuur üle 38 C
Vastunäidustused on ülitundlikkus mittesteroidsete põletikuvastaste ravimite suhtes, raske neeru- ja maksapuudulikkus, peptiline haavand, raseduse kolmas trimester.
Kõrvaltoimed: seedetrakti düspepsia, ülitundlikkusreaktsioonid, bronhospasm; tsütopeeniad, autoimmuunsed sündroomid, manustamiskuuriga, haavandiline toime, neeru- ja maksapuudulikkuse ägenemine, peavalu, pearinglus, kuulmiskahjustus, orientatsioon, valgustundlikkus, harva papillaarnekroos, aseptiline meningiit.
Kasutamine koos teiste MSPVA-de ja glükokortikosteroididega suurendab kõrvaltoimete riski. Fluorokinoloonidega kombineerimisel on võimalik krambisündroomi tekkimine. Diureetikumide, AKE inhibiitorite, beetablokaatoritega kombineerimisel väheneb nende ravimite terapeutiline toime ja suureneb kõrvaltoimete oht. Tsütostaatikumide, epilepsiavastaste ravimite, liitiumipreparaatidega kombineerimisel suureneb nende toime; kombineerituna antikoagulantidega suureneb hemorraagiliste tüsistuste oht; kombineerituna südameglükosiididega võivad MSPVA-d suurendada nende plasmakontsentratsiooni.
DIKLOFENAK. Maksimaalne kontsentratsioon veres areneb 0,5-2 tunni pärast. pärast allaneelamist ja minuti jooksul. pärast i / m manustamist.
Näidustused - vt ülalt
Vastunäidustused: vt eespool, samuti krooniliste soolehaiguste ägenemine, porfüüria.
Koostoimed: tüüpilised MSPVA-de rühma ravimitele (vt eespool).
Annused: mg / päevas kahe kuni kolme annusena, intramuskulaarselt 75 mg sügavale tuharalihasesse.
Õigeaegne antibiootikumravi mõjutab P kulgu ja selle tulemust otsustavalt. Kui patsient viiakse haiglasse, valitakse antibiootikum, võttes arvesse ülaltoodud kliinilisi tunnuseid.
PNEUMOONIA ANTIBIOOTIK RAVI.
Kõige levinumad patogeenid
Esimese rea antibiootikumid
Mitteraske kulg alla 60-aastastel tüsistusteta anamneesiga patsientidel
P 60-aastastel ja vanematel ja/või kaasuvate haigustega patsientidel
2. põlvkonna tsefalosporiinid
P raske kulg
3. põlvkonna tsefalosporiinid
P immuunpuudulikkusega patsientidel
kolmanda põlvkonna antipseudomonaalsed tsefalosporiinid
(antipseudomonaalsed penitsilliinid) + aminoglükosiidid,
3. põlvkonna tsefalosporiinid
amoksitsilliin - klavulanaat + aminoglükosiid,
5.3 Kopsuemboolia
Kopsuemboolia (PE) on sündroom, mis on põhjustatud kopsuarteri või selle harude embooliast trombist ja mida iseloomustavad rasked kardiorespiratoorsed häired ning väikeste okste ummistumise korral tekivad kopsu hemorraagilise infarkti sümptomid.
ETIOLOOGIA JA PATOGENEES.
Kopsuarteri harude emboliseerimise kõige levinum põhjus ja allikas on verehüübed alajäsemete süvaveenidest flebotromboosi korral (umbes 90% juhtudest), palju harvem - paremast südamest südamepuudulikkuse ja ülevenitamise korral. parem vatsake. Eelsoodumusteks on pikaajaline liikumatus, vaagnapiirkonna või alakõhu operatsioon, trauma, rasvumine, suukaudsed kontratseptiivid, rasedus, pahaloomulised kasvajad, müokardiinfarkt, dilatatiivne kardiomüopaatia, kongestiivne südamepuudulikkus, kodade virvendusarütmia, sepsis, insult, seljaaju vigastus, erütreemia, nefrootiline sündroom.
KLIINILINE PILT, KLASSIFIKATSIOON JA DIAGNOSTIKAKRITEERIUMID.
PE-le puuduvad patognoomilised kliinilised tunnused, anamneesiandmete, objektiivse uuringu tulemuste ja elektrokardiograafiliste sümptomite kombinatsiooni põhjal võib kahtlustada diagnoosimist haiglaeelses staadiumis.
PELi KLIINILINE JA ELEKTROKARDIOGRAAFILINE PILT.
Äkiline tekkimine koos õhupuuduse (72% juhtudest) ja ägeda valu rinnus (86%), sageli - äge veresoonte puudulikkus koos kahvatusega, tsüanoos, tahhükardia (87%), vererõhu langus kuni kollapsi ja teadvusekaotuse areng (12%) . Kopsuinfarkti tekkega 10-50% juhtudest ilmneb hemoptüüs röga vereribade kujul. Uurimisel saab määrata pulmonaalse hüpertensiooni ja ägeda kopsusüdame nähud - emakakaela veenide turse ja pulsatsioon, südame piiride laienemine paremale, pulsatsioon epigastriumis, mida süvendab sissehingamine, II tooni aktsent ja hargnemine kopsuarteril, maksa suurenemine. Võib-olla kuiv vilistav hingamine kopsudes.
EKG märgid (esinevad 25% juhtudest).
Parema aatriumi ülekoormuse tunnused (P-pulmonale - kõrge terav P-laine II, III, aVF) ja parema vatsakese (McJean-White'i sündroom - sügav S-laine pliis I, sügav Q-laine ja negatiivne T-laine pliis III koos ST-segmendi võimaliku tõusuga; His-kimbu parema jala mittetäielik blokaad),
Seega, hoolimata selgete diagnostiliste kriteeriumide puudumisest, saab PE diagnoosida haiglaeelses staadiumis, tuginedes anamneesi, uuringuandmete ja EKG põhjalikule igakülgsele hindamisele. Diagnoosi lõplik kontroll tehakse haiglas. Mõnikord avastatakse röntgenuuringul diafragma kõrgel seisev kuppel, diskoidne atelektaas, ühe kopsujuure rohkus või "hakitud" juur, kopsumustri ammendumine kopsu isheemilise tsooni kohal, perifeerne kolmnurk põletiku või pleuraefusiooni vari, kuid enamikul patsientidest radiograafilisi muutusi ei esine. Diagnoosi kinnitab kopsuperfusioonistsintigraafia, mis võimaldab tuvastada iseloomulikke kolmnurkseid alanenud kopsuperfusiooni piirkondi (valikmeetod), samuti kopsu radiopaque angiograafia (angiopulmonograafia), mis paljastab vähenenud verevoolu tsoonid.
Kliiniliselt eristatakse ägedat, alaägedat ja korduvat PE (tabel 13.).
TELA VOOLU VÕIMALUSED.
Iseloomulikud kliinilised tunnused
Äkiline tekkimine, valu rinnus, õhupuudus, vererõhu langus, ägeda cor pulmonale nähud
Progresseeruv hingamis- ja parema vatsakese puudulikkus, infarkti kopsupõletiku nähud, hemoptüüs
Korduvad õhupuuduse episoodid, minestus, kopsupõletiku nähud
Kliinilise pildi analüüsimisel peaks LUTS-i arst saama vastused järgmistele küsimustele.
1) Kas esineb õhupuudust, kui jah, siis kuidas see tekkis (ägedalt või järk-järgult).
PE-ga tekib õhupuudus ägedalt, ortopnea ei ole tüüpiline.
2) Kas teil on valu rinnus?
Võib meenutada stenokardiat, lokaliseeritud rinnaku taga, võib ägeneda hingamine ja köha.
3) Kas esines motiveerimata minestusi.
PE-ga kaasneb või avaldub minestus umbes 13% juhtudest.
4) Kas esineb hemoptüüsi.
Ilmub kopsuinfarkti tekkega.
5) Kas jalgadel on turseid (pöörake tähelepanu nende asümmeetriale).
Jalgade süvaveenide tromboos on tavaline PE allikas.
6) Kas on hiljuti olnud operatsioone, vigastusi, kas on südamehaigusi koos kongestiivse südamepuudulikkusega, rütmihäireid, kas ta võtab suukaudseid rasestumisvastaseid vahendeid, kas ta on rase, kas teda jälgib onkoloog.
Kui patsiendil tekivad ägedad kardiorespiratoorsed häired, peab arst arvestama PE-t soodustavate tegurite olemasolu (nt paroksüsmaalne kodade virvendusarütmia).
PASTEEDI TÖÖTLUSE ALGORITM
Peamised PE-ravi suunad haiglaeelses staadiumis hõlmavad valusündroomi leevendamist, kopsuarterite tromboosi ja korduvate PE episoodide ennetamist, mikrotsirkulatsiooni parandamist (antikoagulantravi), parema vatsakese puudulikkuse korrigeerimist, arteriaalset hüpotensiooni, hüpoksiat (hapnik). ravi), bronhospasmi leevendamine.
Tugeva valu korral ja kopsuvereringe koormamiseks ja õhupuuduse vähendamiseks kasutatakse narkootilisi analgeetikume (näiteks 1 ml morfiini 1% lahust intravenoosselt fraktsionaalselt). See võimaldab mitte ainult valusündroomi tõhusalt peatada, vaid ka vähendada PE-le iseloomulikku õhupuudust. Morfiini kasutamise kõrvaltoimete ja vastunäidustuste kohta vt lõik "Müokardiinfarkt".
Infarkti kopsupõletiku tekkega, kui valu rinnus on seotud hingamise, köhimise, kehaasendiga, on soovitatavam kasutada mitte-narkootilisi analgeetikume (näiteks 2 ml 50% analgini lahuse intravenoosne manustamine).
Kopsuinfarktiga patsientide ellujäämine sõltub otseselt antikoagulantide varajase kasutamise võimalusest. Soovitatav on kasutada otseseid antikoagulante - hepariini in / in jet annuses 00 RÜ. Hepariin ei lüüsi trombi, vaid peatab tromboosi protsessi ja takistab trombi kasvu emboolist distaalses ja proksimaalses piirkonnas. Trombotsüütide serotoniini ja histamiini vasokonstriktiivset ja bronhopaatilist toimet nõrgendades vähendab hepariin kopsuarterioolide ja bronhioolide spasme, mõjutades soodsalt flebotromboosi kulgu, hepariin aitab vältida kopsuemboolia kordumist. Kõrvaltoimete ja hepariini kasutamise vastunäidustuste kohta vt lõik “Müokardiinfarkt”.
Kui haiguse kulgu komplitseerib parema vatsakese puudulikkus, hüpotensioon või šokk, on näidustatud dopamiini- või dobutamiiniravi (vt lõik "Šokk"). Mikrotsirkulatsiooni parandamiseks kasutatakse lisaks intravenoosselt reopolüglütsiinml kiirusega kuni 1 ml minutis. Reopoliglükiin mitte ainult ei suurenda BCC-d ja tõstab vererõhku, vaid omab ka agregatsioonivastast toimet. Kui selle ravi taustal šokk püsib, lähevad nad üle 400 ml reopolüglütsiiniga lahjendatud dopamiini aminamimg-ravile, samal ajal kui 1 ml saadud lahust sisaldab 500 μg dopamiini ja üks tilk 25 μg. Algne manustamiskiirus on vererõhu kontrolli all 5 μg / kg min, suurendades annust järk-järgult kuni 15 μg / kg min. 2 ml 0,2% noradrenaliini lahust lahjendatakse 250 ml isotoonilises naatriumkloriidi lahuses ja manustatakse algkiirusega tilgad minutis (hemodünaamika stabiliseerumisel vähendatakse kiirust tilkadeks minutis).
PE-ga on näidustatud pikaajaline hapnikravi. Bronhospasmi ja stabiilse vererõhu (SBP mitte alla 100 mm Hg) tekkega on näidustatud 10 ml aminofülliini 2,4% lahuse intravenoosne aeglane (juga või tilk) manustamine. Eufilliin vähendab rõhku kopsuarteris, omab trombotsüütide agregatsiooni vastast toimet ja omab bronhe laiendavat toimet.
LEVIKUD RAVIVEAD.
PE-ga patsientide kopsuinfarkti korral ei ole hemostaatiliste ainete kasutamine sobilik, kuna hemoptüüs ilmneb tromboosi või trombemboolia taustal.
Samuti ei ole otstarbekas määrata südameglükosiide ägeda parema vatsakese puudulikkuse korral, kuna need ravimid ei mõjuta eraldiseisvalt paremat südant ega vähenda parema vatsakese järelkoormust. Digitaliseerimine on aga täielikult õigustatud patsientidel, kellel on tahhüsüstoolne kodade virvendusarütmia, mis on sageli trombemboolia põhjus.
NÄIDUSTUSED haiglaraviks.
PE kahtluse korral on haiglaravi kohustuslik.
5.4 KOPSU- JA PLEURA MÄDASED HAIGUSED.
Äge abstsess, kopsu gangreen on kopsu parenhüümi mädane-nekrootiline liitmine (gangreeniga on nekroos ulatuslikum, ilma selgete piirideta, kipub levima; kliiniliselt väljendub haigus patsiendi väga raskes üldseisundis).
ETIOLOOGIA JA PATOGENEES.
Destruktiivsete muutuste peamised põhjused kopsudes on: ägeda P tüsistus (sageli gripijärgne) - 63-95% juhtudest; aspiratsioon (nakkusetekitaja sattumine suuõõnest kopsu - kaariesed hambad, periodontaalne haigus, krooniline tonsilliit). Viimastel aastatel on kindlaks tehtud, et 50-60% juhtudest aspireeritakse ainult anaeroobset mikrofloorat (Fusobact. nucleatum, Fusobact. necrophorum, Bacter. fragilis, Bacter. melaninogenus jt).
Lisaks on levinumad patogeenid: hemolüütiline staphylococcus aureus ja gramnegatiivne mikrofloora.
Muude ägeda abstsessi ja kopsu gangreeni tekke põhjuste hulgas on vaja välja tuua hematogeenne-emboolia (0,8–9,0% juhtudest), traumajärgne tegur, bronhide obstruktsioon (kasvaja, võõrkeha).
Tuleb rõhutada, et ägedad abstsessid ja kopsugangreen arenevad kõige sagedamini krooniliste haiguste tõttu nõrgenenud patsientidel, alkoholisõltuvusega inimestel; raskete süsteemsete haigustega KOK-i taustal.
ägedad abstsessid ja kopsugangreen on mitmekesised ja sõltuvad kopsukoe nekrootiliste piirkondade suurusest, tüsistunud või tüsistusteta kulgemisest, patsiendi vanusest, kaasuvatest haigustest, organismi individuaalsetest iseärasustest jne. Kopsuabstsessi korral haiguse algsel (esimesel) perioodil (enne abstsessi avanemist bronhis) määrab patsiendi seisundi raskuse mädane joove, mis on tingitud mäda ja nekrootiliste masside võimatust evakueerimisest hävitamisest. õõnsused loomulikul teel läbi äravoolu bronhide. Patsiendid kurdavad kõrget palavikku, külmavärinaid, valu rindkere vastavas pooles, vähese rögaga köha. Füüsilisel läbivaatusel on "haige" poolel hingamine nõrgenenud, löökpillide heli lüheneb. Kopsukoe suure kahjustuse korral on kuulda krepiteerivat räigutamist. Röntgeni andmed näitavad kopsu põletikulist infiltratsiooni ilma selgete piirideta.
Haiguse esimene periood kestab keskmiselt 7-10 päeva.
Haiguse teisel perioodil (pärast abstsessi avanemist bronhis) on patognoomiliseks sümptomiks mädase, sageli ebameeldiva lõhnaga röga rohke eritumine, "suu täis". Kui samal ajal on bronhide veresoonte arrosioon, märgitakse kopsuverejooks. Samal ajal langeb temperatuur, väheneb joove, paraneb heaolu. Füüsilise läbivaatuse käigus on võimalik tuvastada õõnsus kopsus löökpillidega, auskultatsiooniga - bronhide hingamine amfoorse varjundiga. Iseloomulik on röntgenisemiootika - ümar õõnsus, mida ümbritseb infiltratsioonivõll, mille luumenis on horisontaalne vedelikutase.
Röga (makroskoopiliselt) on kolm kihti: mäda, hägune vedelik, vahune kiht.
Kopsu gangreeni iseloomustab ulatuslikum kopsu parenhüümi nekroos (kui abstsessiga), ilma selgete piirideta, mis hõlmab mitut segmenti, sagara või kogu kopsu. Haigus kulgeb kiiresti, millega kaasneb kirglik palavik, raske joobeseisund, valu rinnus kahjustuse küljel, õhupuudus. Röga on määrdunudhall või pruun (sagedamini) värvuselt ebameeldiva lõhnaga, määratakse eemalt, sageli kopsukoe sekvestritega. Mõnikord komplitseerib haigust kopsuverejooks (hemoptüüs), mis võib lõppeda surmaga. Kahjustuse koha kohal määratakse löökpillide heli lühenemine ja järsult nõrgenenud (või bronhiaalne) hingamine. Vere- ja rögaanalüüsis ägedale abstsessile iseloomulikud, kuid rohkem väljendunud muutused. Kopsude röntgenograafia näitab massiivset infiltratsiooni ilma selgete piirideta, hõivates ühe laba või kogu kopsu. Kui on tekkinud lagunemisõõnsus ja see suhtleb bronhi valendikuga, siis radioloogiliselt määratakse see ebakorrapärase kujuga valgustusena (üksik või mitmekordne), võib-olla koos vabade või parietaalsete sekvestrite olemasoluga.
Tuleb rõhutada, et kopsu äge abstsess ja gangreen on täis mitmete raskete, mõnikord surmaga lõppevate tüsistuste tekkimist: arrosiivne verejooks (eriti kui protsess lokaliseerub juuretsoonides), püopneumotooraks (koos subpleuraalsete abstsessidega), sepsis , perikardiit, vastaskopsu kahjustus.
Äge mädane pleuriit
Äge mädane pleuriit - pleura põletik, mida iseloomustab mädase eksudaadi moodustumine.
Äge mädane pleuriit (pleura empüeem) võib olla primaarne (pärast rindkere läbitungivat haava, kopsuoperatsioone, diagnostilist torakoskoopiat, kunstliku pneumotooraksi pealekandmisega) või sekundaarne (kopsu mädaste-põletikuliste haiguste tüsistustega ja kopsude avanemisega). subpleuraalselt paiknevad abstsessid). Viimasel juhul siseneb koos mädaga ka õhk pleuraõõnde (püopneumotooraks). Pleuraõõne sisu bakterite spekter 62,5% patsientidest näitab 2-5 erineva liigi patogeenide (staphylococcus aureus, proteus, Escherichia coli ja Pseudomonas aeruginosa) seost. Bakterioloogilised uuringud näitasid 28% juhtudest erinevat tüüpi mitteklostriidilisi anaeroobe (bakteroidid, fusobakterid, mädane streptokokk jne).
rinnakelme ägedat sekundaarset empüeemi iseloomustab asjaolu, et põletikuline protsess kopsust (kopsupõletik, abstsess, koobas, mädane tsüst) läheb pleurasse, tavaliselt samal küljel. Esinevad teravad valud rinnaku vastavas pooles, temperatuuri tõus 38,5-39 C-ni, hingamispuudulikkuse nähud (põhjustatud kopsu kokkusurumisest mäda poolt ja mädased-destruktiivsed muutused kopsukoes endas), köha koos mädanikuga. röga. Objektiivsel uurimisel ilmnevad joobeseisundi sümptomid, rindkere ühe poole hingamisliigutuste piiramine, löökpillide tuim ja hingamise järsk nõrgenemine (või seda ei tehta üldse, mis juhtub sagedamini). Röntgenuuring näitab empüeemi küljelt tumenemist, mediastiinumi nihkumist vastupidises suunas. Püopneumotooraksiga määratakse horisontaaltase ja selle kohal olev gaas. Sõltuvalt pleuraõõnes oleva mädase vedeliku kogusest ja vastavalt kopsu kokkuvarisemise astmest eristatakse piiratud, vahesumma ja kogu püopneumotooraks.
Spontaanne mittespetsiifiline pneumotooraks
Spontaanne pneumotooraks (SP) on õhu kogunemine pleuraõõnde, mis areneb reeglina ilma eelnevate sümptomiteta (täieliku tervise juures). Õhk siseneb subpleuraalselt paiknevate õhubullide defekti(de) kaudu. Enamik teadlasi usub, et pullide teket seostatakse kopsu parenhüümi kaasasündinud alaväärsusega. Viimasel ajal on teatatud haiguse perekondliku vormi – päriliku spontaanse pneumotooraksi (pärilik emfüseem) – juhtudest. Eeldatakse, et selle põhjuseks on alfa-1 antitrüpsiini puudulikkus, mis pärineb autosoomselt retsessiivselt. Parem kops on sagedamini kahjustatud, kahepoolset (tavaliselt vahelduvat) pneumotooraksi täheldatakse 17,7% juhtudest.
spontaanne pneumotooraks on üsna tüüpiline: teravate valude ilmnemine rindkere vastavas pooles (sageli ilma nähtava põhjuseta), õhupuudus (selle raskusaste sõltub kopsu kokkuvarisemise astmest). Valu kiirgub õla, kaela, epigastimaalsesse piirkonda, rinnaku taha (eriti vasakpoolse pneumotooraksi korral), sageli simuleerides stenokardiat või müokardiinfarkti. Füüsilisel läbivaatusel tuvastatakse õhupuudus, tümpaniidi löökpillidel kahjustuse küljel, hingamise nõrgenemine (või puudumine) auskultatsioonil. Diagnoosi täpsustavad röntgenuuringu andmed: kahjustatud poolel täheldatakse erineva raskusastmega pneumotooraksi ja kops on kokku kukkunud. Suure pneumotooraksi korral võib tekkida mediastiinumi nihkumine vastupidises suunas. Kopsude põhjalik uurimine on vajalik pneumotooraksi võimaliku põhjuse väljaselgitamiseks - bulloosne emfüseem, tuberkuloosne õõnsus, abstsess (nende haiguste korral on pneumotooraks nende tüsistus). Mõnikord saab röntgenülesvõtetel tuvastada esimese segmendi suuri subpleuraalselt paiknevaid bulla.
RAVIMEETMETE PÕHIMÕTTED.
Sekkumine haiglaeelses staadiumis taandatakse sümptomaatiliseks raviks.
1) Valusündroom - enne tugeva pleuravaluga patsiendi haiglasse transportimist võib manustada mittenarkootilisi valuvaigisteid - ketarolaki, tramadooli. Pneumotooraksiga võib valusündroomi intensiivsus nõuda narkootiliste analgeetikumide manustamist. Sel juhul tuleks eelistada 2% promedooli lahust. Tuleb meeles pidada, et võimsamad ravimid, morfiin ja fentanüül, mõjuvad hingamiskeskust pärssivalt ja võivad hüpoksiat süvendada.
2) Arteriaalne hüpotensioon – patsientide transportimine haiglasse, et vältida ortostaatilise kollapsi tekkimist, tuleb läbi viia lamavas asendis. Madala vererõhuga (SBP< 100) целесообразно во время транспортировки проводить в/в инфузию раствора полиглюкина.
3) Hingamispuudulikkus - areneb koos kopsukoe massilise kahjustusega. Hüpoksia astme vähendamiseks transpordi ajal hingatakse niisutatud hapnikku ninakanüülide või maski kaudu.
4) Hingamispuudulikkuse suurenemine pneumotooraksi korral võib olla seotud selle arengu klapimehhanismiga. Sellisel juhul nõuab pinge pneumotooraks erakorralist dekompressiooni, mis viiakse läbi ühe või mitme suure läbimõõduga süstlanõela sisestamisega pleuraõõnde. Selle manipuleerimise läbiviimine nõuab esialgset anesteesiat, lisades 1 ml 2% promedooli lahust.
NÄIDUSTUSED haiglaraviks.
Mädased kopsuhaigused, samuti pneumotooraksi arengu juhtumid nõuavad rindkere kirurgia osakonna patsientide erakorralist hospitaliseerimist.
1. Beeta-2 adrenomimeetikumid
1.1 Lühitoimelised beeta-2 adrenomimeetikumid:
Salbutamool 90./44/6
(Ventolin 00238/16.01.95, Ventolin Lihtne hingamine, Ventolini udukogu P8242-011022. 06.04.99 Ventodisk 007978/25.11.96. Salben 95/178/11) Fenoterol/011.9101.9. (Brikanil 00427/26.01.93) Heksoprenaliin (Ipradol 002557/14.07.92)
1.2 Beeta-2 pika toimeajaga agonistid:
Klenbuterool (Spiropent 007200/28.05.96) Formoterool (Foradil 003315/10.09.93, Oxys 011262/21.07.99) Salmeterool (Serevent 006227/28.06.96) 94/294/9)
2. Metüülksantiinid
2.1 Aminofülliin (Euphyllin 72/631/8. 72/334/32; Aminofülliin 002301/10.12.91; 002365/27.01.92)
teofülliin
Ipratroopiumbromiid (Atrovent 00943/09/22/93; 007175/04/04/96; 007655/07/22/96)
4. Kombineeritud ravimid:
beeta-2 adrenomimeetikum + ipratroopiumbromiid
fenoterool + ipratropuimbromiid (Berodual 01104/04.05.95)
beeta-2 adrenomimeetikum + kromoglütsiinhape
fenoterool + kromoglütsiinhape (Ditek 008030/25.02.97) salbutamool + kromoglütsiinhape (Intal plus 006261/11.07.95)
1. Beeta-2 adrenomimeetikum
1.1. Lühitoimeline beeta-2 agonist
Salbutamool
(Ventolin, Ventolini udukogu, Vetodiski, Ventolin Kerge hingamine, Salben) Farmakoloogiline toime
Salbutamool on bronhides, müomeetriumis ja veresoontes lokaliseeritud beeta-2-adrenergiliste retseptorite selektiivne agonist.Terapeutilistes annustes, toimides bronhide silelihaste beeta-2-adrenergilistel retseptoritel, on sellel tugev bronhodilataator ja see on vähene või puudub üldse. toime beeta-1-adrenergilistele retseptoritele.müokard
Sissehingamise teel imendub see kopsukudedesse, ilma kopsudes metaboliseerumata, siseneb vereringesse. Ravim metaboliseerub "esimese läbimise" ajal läbi maksa ja seejärel eritub peamiselt uriiniga muutumatul kujul või fenoolsulfaadi kujul.
Bronhodilateeriv toime ilmneb 4-5 minuti pärast, maksimaalne toime on 40-60 minutit, poolväärtusaeg 3-4 tundi, toime kestus 4-5 tundi. Koostis ja vabastamise vorm
Salbutamooli ravimvormid on saadaval mitmesuguste ravimvormidena ja erinevate hingamisteede manustamisseadmetega.
Doseeriv aerosoolinhalaator Ventolin sisaldab 100 mikrogrammi salbutamooli (salbutamoolsulfaadina) annuse kohta
Doseeritud inhalaator Ventolin Easy Breathing aktiveeritakse hingamise teel, mis hõlbustab sissehingamist, ei vaja sünkroniseerimist, sisaldab 100 mcg salbutamooli (salbutamoolsulfaati) annuse kohta
Ventoliini udukogu(plastampullid) 2,5 ml, mis sisaldavad 2,5 mg salbutamooli füsioloogilises lahuses (salbutamoolsulfaadi kujul) inhaleerimiseks läbi nebulisaatori. Ravimi koostis ei sisalda säilitusaineid ega värvaineid
Ventodisk - inhalatsioonipulber, 200 mcg salbutamoolsulfaati ühes annuses, komplektis ketasinhalaatoriga "Ventolin-Diskhaler"
Salben- kuiv inhalatsioonipulber, 200 mcg, manustatuna individuaalse tsüklohalerinhalaatori abil
Annustamisrežiim
Doseeritud aerosool Ventolin, Ventolin Easy hingamine, pulber Ventodisk, Salben kantakse peale 100-200 mcg (1 või 2 inhalatsiooni), 3-4 korda päevas.
Ventolin Nebula't tuleb kasutada spetsialistide järelevalve all, kasutades spetsiaalset inhalaatorit (nebulisaatorit). Ventolin Nebula on ette nähtud kasutamiseks lahjendamata kujul ainult inhalatsiooniks 2)
Kõrvalmõjud
Salbutamool võib põhjustada kerget skeletilihaste värinat, mis on tavaliselt kõige tugevam kätes, aeg-ajalt ärritust ja suurenenud motoorset aktiivsust. Mõnel juhul on 16 patsiendil peavalu, perifeerne vasodilatatsioon ja kerge kompenseeriv südame löögisageduse tõus. Patsientidel, kellel on eelsoodumus arütmiate tekkeks, on võimalikud südame rütmihäired. Inhaleeritavad ravimid võivad põhjustada suuõõne ja neelu limaskesta ärritust.
- Salbutamooli ja teiste beeta-2-agonistide suurte annuste kasutamine võib põhjustada hüpokaleemiat, seetõttu tuleb üleannustamise kahtluse korral jälgida kaaliumisisaldust vereseerumis.
Sarnaselt teiste beeta-adrenergiliste agonistidega võib salbutamool põhjustada pöörduvaid metaboolseid muutusi, nt veresuhkru kontsentratsiooni tõusu.Suhkurtõvega patsientidel võib tekkida dekompensatsioon ja mõnel juhul ka ketoatsidoos.
Fenoteroolvesinikbromiid (Berotek) Farmakoloogiline toime
Fenoterool on lühitoimeline beeta-2-adrenergiline stimulant.Kõrge bronhodilataatoriefekt on seotud selektiivsusega beeta-2-adrenergiliste retseptorite suhtes, samuti adenülaattsüklaasi aktiveerimisega, akumuleeruv cAMP lõdvestab bronhide silelihaseid; põhjustab nuumrakkude membraanide ja basofiilide stabiliseerumist (vähendab bioloogiliselt aktiivsete ainete vabanemist), parandab mukotsiliaarset kliirensit; omab tokolüütilist toimet Koostis ja vabastamise vorm
Berotek N doseeritud inhalaator (CFC-vaba propellendiga) —ühes annuses 100 mikrogrammi fenoteroolvesinikbromiidi
Beroteki lahus nebulisaatorraviks- 1 ml lahust sisaldab 1,0 mg fenoteroolvesinikbromiidi
Annustamisrežiim
a) äge bronhiaalastma atakk
Enamikul juhtudel piisab sümptomite leevendamiseks ühest inhalatsiooniannusest, kuid kui hingamine 5 minuti jooksul ei leevendu, võite inhalatsiooni korrata.
Kui pärast kahte sissehingamist efekt puudub ja on vaja täiendavaid sissehingamisi, peate viivitamatult pöörduma arsti poole lähimasse haiglasse.
b) füüsilise pingutuse astma ennetamine
1-2 inhalatsiooniannust korraga, kuni 8 annust päevas
c) Bronhiaalastma ja muud seisundid, millega kaasneb hingamisteede pöörduv ahenemine
1-2 inhalatsiooniannust annuse kohta, kui on vaja korduvaid inhalatsioone, siis mitte rohkem kui 8 inhalatsiooni päevas
Lastele mõeldud Berotek N doseeritud aerosooli võib välja kirjutada ainult arsti soovitusel ja täiskasvanute järelevalve all.
Inhalatsioonilahus määratakse läbi nebulisaatori range meditsiinilise järelevalve all (Beroteki annused nebulisaatori jaoks on toodud lisas 2)
Kõrvalmõju
Üleannustamise tagajärjel võivad tekkida näkku voolava vere aistingud, sõrmede värisemine, iiveldus, ärevus, südamepekslemine, peapööritus, süstoolse vererõhu tõus, diastoolse vererõhu langus, agitatsioon ja võimalikud ekstrasüstolid.
Terbutaliin (Brikaniil) Farmakoloogiline toime
Terbutaliin on lühitoimeline selektiivne beeta-2 agonist. Bronhodilateeriv toime on tingitud beeta-2-adrenergiliste retseptorite stimuleerimisest;
silelihasrakkude toonuse langus ja bronhide lihaste laienemine.
Koostis ja vabanemisvorm Annustamine aerosoolinhalaator Brikanil -ühes annuses 250 mcg terbutaliinsulfaati Bricanil tabletid- 1 tablett sisaldab: terbutaliinsulfaati - 2,5 mg
Annustamisrežiim
Sissehingamine doseeritud inhalaatoriga, 1-2 hingetõmmet (0,25) iga 6 tunni järel. Suukaudne annus 2,5 mg 3-4 korda päevas.
Heksoprenaliin (Ipradol) Farmakoloogiline toime
Ipradol on lühitoimeline selektiivne beeta-2 agonist – katehhoolamiin, mis on kokku pandud kahest heksametüleensillaga ühendatud norepinefriini molekulist. Kõigile nendele molekulidele on ühine selektiivne beeta-2 retseptori afiinsus.
Koostis ja vabastamise vorm:
Aerosoolinhalaator Ipradol- 1 annus 200 mcg heksoprenaliinsulfaati
Tabletid- 1 tb - 500 mcg heksoprenaliinsulfaati.
Annustamisrežiim
Ipradol inhalatsioon on ette nähtud üle 3-aastastele lastele 1 hingetõmbega, intervalliga vähemalt 30 minutit.
Ipradol tableti kujul on ette nähtud lastele, kellel on kerge kuni mõõdukas astma ja kerge õhupuuduse hood annuses
3-6 kuud 0,125 mg (1/4tb) 1-2 korda päevas
7-12 kuud 0,125 mg (1/4 tb) 1 kord päevas
1-3 aastat 0,125-0,25 mg (1/4-1/2 TB) 1-3 korda päevas
4-6 aastased 0,25 mg(1/2 tb) 1-3 korda päevas
7-10 aastat 0,5 mg (1 tb) 1 kord päevas Kõrvalmõju
Väikelastel esinevate kõrvaltoimete hulgas on harva suurenenud erutuvus, ärrituvus, unehäired ja unerütmi muutus.
1.2. Pika toimeajaga beeta-2 agonistid
Salmeterool (Serevent, Salmeter) Farmakoloogiline toime
Pikaajalise toimega beeta-2-adrenergiliste retseptorite selektiivne agonist. Toime algab 5-10 minutit pärast sissehingamist pikaajalise bronhide laienemisega kuni 12 tundi. Salmeterool hüdroksüleeritakse maksas kiiresti, suurem osa manustatud annusest eritub 72 tunni jooksul.
Vabastamise vorm
Serevent Rotadisk- fooliumist ümmarguste villide (rotadiskide) kujul, millel on 4 lahtrit, mille ümbermõõt on paigutatud pulber. Üks rakk sisaldab 50 mikrogrammi salmeteroolksinafoaati ja täiteainena laktoosi. Serevent Rotadiski kasutatakse spetsiaalse inhalatsiooniseadmega - "Serevent Diskhaler". Kogu ravimi annus siseneb hingamisteedesse isegi väga väikese sissehingamise kiirusega.
Doseeriv aerosoolinhalaator Serevent sisaldab 25 mikrogrammi salmeteroolksinafoaati annuse kohta.
Annustamisrežiim
See on ette nähtud üle 3-aastastele lastele 25-50 mcg (1-2 hingetõmmet) 2 korda päevas.
Sereventi regulaarne (2 korda päevas) kasutamine on näidustatud juhtudel, kui patsiendil on vaja kasutada lühitoimelist inhaleeritavat bronhospasmolüütikumi rohkem kui 1 kord päevas või kombinatsioonis inhaleeritavate kortikosteroididega. Kõrvalmõju
Võib-olla paradoksaalse bronhospasmi, peavalu, tahhükardia, treemori areng;
võimalik hüpokaleemia.
Pikaajalise toimega salbutamool (Volmaks, Saltos) Farmakoloogiline toime
Beeta-2-adrenergilise agonisti pikaajaline toime tuleneb osmootselt kontrollitud mehhanismist, mille käigus vabaneb ravimaine järk-järgult tabletisüdamikust 9-12 tunni jooksul.
Vabastamise vorm
Volmax- 4 mg ja 8 mg salbutamoolsulfaadi tabletid.
Saltos- 7,23 mg salbutamoolsulfaadi tabletid.
Annustamisrežiim
Lapsed vanuses 3–12 aastat: 4 mg 2 korda päevas Tabletid tuleb alla neelata tervelt koos veega, ilma hammustamise või närimiseta. Üle 12-aastased - vajadusel võib annust suurendada 8 mg-ni 2 korda päevas.
Formoterool (Foradil, 0xis) Farmakoloogiline toime
Selektiivne beeta-2-agonist. Bronhospasmolüütiline toime algab pärast sissehingamist 1-3 minuti pärast, terapeutiline toime püsib 12 tundi. Toimeaine ja selle metaboliidid erituvad organismist täielikult. Suukaudse ja inhaleeritava formoterooli farmakokineetilised omadused on suures osas sarnased.
Koostis ja vabastamise vorm- 1 annus sisaldab: formoteroolfumaraati - 4,5-9 mcg. Foradil - inhalatsioonipulber kapslites - 1 kapsel sisaldab: formoteroolfumaraati - 12 mcg
Annustamisrežiim 5-aastastele ja vanematele lastele määratakse 1-2 korda päevas.
Klenbuterool (Spiropent) Farmakoloogiline toime
Spiropent selektiivne beeta-2 agonist. Sellel on suukaudsel manustamisel pikk bioloogiline poolväärtusaeg ning kiire ja täielik imendumine. See avaldab mõju pärast võtmist 10-12 tunni jooksul.
Koostis ja vabastamise vorm
Tabletid - 1 TB sisaldab 0,02 mg klenbuteroolvesinikkloriidi
Siirup - 5 ml 0,005 mg klenbuteroolvesinikkloriidi
Annustamisrežiim
Tabletid on ette nähtud üle 12-aastastele lastele ja täiskasvanutele, 1 TB (0,02 mg 2 korda päevas. Pikaajalise ravi korral võib annust vähendada 0,02 mg-ni päevas).
Alla 12-aastastele lastele on spiropendi annus 0,0012 mg/kg kehakaalu kohta.
Spiropent siirupis on ette nähtud lastele:
6-12 aastat 15 ml (0,015 mg) 2 korda päevas.
4-6 aastat 10 ml (0,01 mg) 2 korda päevas.
2-4 aastat 5 ml (0,005 mg) 3 korda päevas.
alla 2-aastased 5 ml (0,005 mg) 2 korda päevas.
Kõrvalmõju
Spiropent võib põhjustada sõrmede värinat, harva erutust, tahhükardiat, ekstrasüstole.
2.Metüülksantiinid
2.1 Eufillin, aminofiliin Farmakoloogiline toime
Metüülksantiinidel on väljendunud bronhodilataator, need parandavad diafragma kontraktsiooni, suurendavad mukotsiliaarset kliirensit, vähendavad kopsuveresoonkonna resistentsust, neil on positiivne inotroopne ja mõõdukas diureetiline toime. Teofülliinid pärsivad allergia vahendajate vabanemist nuumrakkudest, stimuleerivad kesknärvisüsteemi, hingamiskeskust ja suurendavad adrenaliini vabanemist neerupealiste poolt. Ravimite toime on tingitud fosfodiesteraasi inhibeerimisest ja selle tulemusena tsüklilise adenosiinmonofosfaadi akumuleerumise suurenemisest kudedes. Kliiniline toime sõltub ravimi kontsentratsioonist vereseerumis. Suukaudsel manustamisel imendub teofülliin kiiresti ja täielikult, kuid biosaadavus sõltub ravimi ravimvormist. Teofülliini peamine eliminatsioonitee on selle biotransformatsioon maksas, 10% muutumatul kujul eritub uriiniga.
Vabastamise vorm
Eufilliini lahus- intravenoosseks manustamiseks - 10 ml 2,4% ampullis
Eufillini tabletid– 1 tablett sisaldab – 150 mg
Annustamisrežiim
Intravenoosse manustamise küllastusannus on 4,5-5 mg/kg 20-30 minuti jooksul. Seejärel võib aminofülliini manustada pideva infusioonina annuses 0,6-0,8 mg / kg / tunnis või fraktsionaalselt sobivates annustes iga 4-5 tunni järel, kontrollides teofülliini kontsentratsiooni veres.
Suukaudne päevane annus on keskmiselt 7-10 mg/kg. Kõrvalmõju
Ärevus, unehäired, peavalu, treemor, iiveldus, oksendamine, kõhulahtisus, südamepekslemine, rütmihäired.
2.2 Pikatoimeline teofülliin
Teofülliini vabanemine toimeainet püsivalt vabastavatest ravimvormidest toimub nii, et kontsentratsioon püsib terapeutilistes piirides (8-15 mg / l) peaaegu kõik päevad sujuva maksimumiga öösel ja varahommikul.
Väljalaske vorm Teopak- tabletid - 1 tablett - 100, 200, 300 mg veevaba teofülliini Retafil- tabletid -1 tablett - 200, 300 mg veevaba teofülliini Theotard- kapslid - 1 kapsel - 200, 350, 500 mg veevaba teofülliini Euphylong- kapslid - 1 kapsel - 250, 375 mg veevaba teofülliini. Ventax- kapslid, mis sisaldavad 100, 200, 300 mg veevaba teofülliini veevaba teofülliini Sporofülliin-retard- 100, 250 mg veevaba teofülliini tabletid
Annustamisrežiim
Päevane annus 6-8-aastastele lastele on 200-400 mg 1-2 annusena, 8-12-aastastele 400-600 mg, üle 12-aastastele 600-800 mg
Kõrvalmõju
Südamepekslemine, arütmia, rahutus, agiteeritus, treemor, unehäired, peavalu, iiveldus, oksendamine, kõhulahtisus
3. M-kolinergiliste retseptorite blokaatorid
Ipratroopiumbromiid (ATROVENT) Farmakoloogiline toime
Toimeaine on ipratroopiumbromiid, neurotransmitteri atsetüülkoliini Atrovent konkureeriv antagonist, mis blokeerib trahheobronhiaalpuu silelihaste retseptoreid ja pärsib refleksi bronhokonstriktsiooni, takistab erinevate teguritega kokkupuutel vagusnärvi tundlike kiudude atsetüülkoliini poolt vahendatud stimulatsiooni. on nii ennetava kui ka bronhodilateeriva toimega, põhjustab bronhide näärmete sekretsiooni vähenemist
Ravimi toime ilmneb 25-50 minutit pärast sissehingamist, saavutab maksimumi 1 tunni lõpuks ja kestab 6-8 tundi.
Koostis ja vabastamise vorm
Mõõdetud aerosoolinhalaator, 1 annus - 20 mikrogrammi ipratroopiumbromiidi
Inhalatsioonilahus 1 ml (20 tilka)- 250 mikrogrammi ipratroopiumbromiidi Annustamisrežiim
Aerosooli doseerimine- 1-2 inhalatsiooni 3-4 korda päevas
Inhalatsioonilahus läbi nebulisaatori (2. liide) Kõrvalmõju
Süsteemsed toimed on teadmata, mõnel juhul võib silma sattumisel ilmneda suukuivus, kerged pöörduvad akommodatsioonihäired.
4. Kombineeritud ravimid
Beeta-2 adrenomimeetikum + ipratroopiumbromiid (BERODUAL) Farmakoloogiline toime
Berodual on kombineeritud bronhodilataator, mis sisaldab fenoterooli (beeta-2-agonist) ja ipratroopiumbromiidi, M-kolinergiliste retseptorite blokaatorit. Ipratroopiumbromiid blokeerib kolinergilised retseptorid, beeta-2-agonist põhjustab silelihasrakkude beeta-retseptorite stimuleerimist ja kiiret bronhodilatatsiooni Erineva toimemehhanismiga ainete kombinatsioon võimendab bronhodilataatorit ja pikendab selle kestust Koostis ja vabastamise vorm
Doseeriv aerosoolinhalaator Berodual- 1 annus sisaldab 50 mikrogrammi fenoterooli ja 20 mikrogrammi ipratroopiumbromiidi
Inhalatsioonilahus Berodual– 20 ml viaalis nebulisaatorravi jaoks. 1 ml (20 tilka) sisaldab 500 mcg fenoterooli ja 250 mcg ipratroopiumbromiidi Annustamisrežiim
Annustamisaerosool Berodual on ette nähtud üle 3-aastastele lastele, 1-2 annust 3 korda päevas (kuni 8 annust päevas).
Beroduali lahus nebulisaatori jaoks (lisa 2)
Kõrvalmõju
Kõrvaltoimed on ebaolulised Suhtelise või absoluutse üleannustamise korral on võimalik sõrmede värisemine, südamepekslemine, mis on seotud fenoterooli sisaldusega preparaadis. Mõnel juhul on ipratroopiumbromiidi esinemisega seotud suukuivus, kerged ja pöörduvad akommodatsioonihäired. ettevalmistus
Beeta-2 adrenomimeetikum + kromoglütsiinhape (Ditek) Farmakoloogiline toime
Kombineeritud ravim bronhodilataatori ja allergiavastase toimega. Hoiab ära ja kõrvaldab bronhospasmi, parandab ripsepiteeli funktsiooni, takistades nuumrakkude degranulatsiooni ja bioloogiliselt aktiivsete ainete vabanemist neist.
Koostis ja vabastamise vorm
Doseeritud inhalaator - 1 inhaleeritav annus sisaldab fenoteroolvesinikbromiidi - 50 mcg ja dinaatriumkromoglükaati - 1 mg
Annustamisrežiim 4-6-aastased lapsed: 1 annus 4 korda päevas. Üle 6-aastastele lastele 2 inhalatsiooniannust 4 korda päevas
Kõrvalmõju Võimalik sõrmede värisemine, südamepekslemine, rahutus
Beeta-2 adrenomimeetikum + kromoglütsiinhape (Intal plus) Farmakoloogiline toime
Naatriumkromoglükaat hoiab ära bronhospasmi, takistades nuumrakkude degranulatsiooni ja nendest bioloogiliselt aktiivsete ainete vabanemist. Salbutamool on beeta-adrenergiline agonist, millel on domineeriv toime beeta-2 retseptoritele, omab bronhe laiendavat toimet.
Koostis ja vabastamise vorm
Annustamine aerosoolinhalaator - 1 annus sisaldab naatriumkromoglükaati - 1 mg, salbutamooli - 100 mi- Annustamisrežiim
Lapsed vanuses 6 aastat 1-2 inhalatsiooni 4 korda päevas. Raskematel juhtudel või kokkupuutel allergeeniga on võimalik annust suurendada 6-8 inhalatsioonini päevas.
Kõrvalmõju
Võimalik kurguvalu, köha, bronhospasm, peavalu, mööduvad lihaskrambid, väga harva angioödeem, arteriaalne hüpotensioon, kollaps.
(Külastatud 221 korda, täna 1 külastust)
Beeta agonistid
Beeta-agonistid(sün. beeta-agonistid, beeta-agonistid, β-agonistid, β-agonistid). Bioloogilised või sünteetilised ained, mis põhjustavad β-adrenergiliste retseptorite stimulatsiooni ja avaldavad olulist mõju organismi põhifunktsioonidele. Sõltuvalt võimest seonduda β-retseptorite erinevate alatüüpidega, eraldatakse β1- ja β2-agonistid.
β-adrenergiliste retseptorite füsioloogiline roll
Kardioselektiivsete β1-blokaatorite hulka kuuluvad talinolool (Cordanum), atsebutolool (Sektral) ja tseliprolool.
Beeta-agonistide kasutamine meditsiinis
Mitteselektiivsed β1-, β2-agonistid isoprenaliini ja ortsiprenaliini kasutatakse lühiajaliselt atrioventrikulaarse juhtivuse parandamiseks ja rütmi suurendamiseks bradükardia korral
β1-agonistid: dopamiini ja dobutamiini kasutatakse südame kontraktsioonide jõu stimuleerimiseks müokardiinfarkti, müokardiidi või muude põhjuste põhjustatud ägeda südamepuudulikkuse korral.
lühitoimelised β2-agonistid nt fenoterooli, salbutamooli ja terbutaliini kasutatakse mõõdetud annustega aerosoolidena astmahoo leevendamiseks bronhiaalastma, kroonilise obstruktiivse kopsuhaiguse (KOK) ja teiste bronhoobstruktiivsete sündroomide korral. Intravenoosset fenoterooli ja terbutaliini kasutatakse sünnitustegevuse vähendamiseks ja raseduse katkemise ohuks.
pika toimeajaga β2-agonistid salmeterooli kasutatakse profülaktikaks ja formoterooli nii bronhospasmide ennetamiseks kui ka leevendamiseks bronhiaalastma ja KOK-i korral mõõdetud aerosoolide kujul. Sageli kombineeritakse neid astma ja KOK-i raviks samas aerosoolis inhaleeritavate glükokortikosteroididega.
Beeta-agonistide kõrvaltoimed
Inhaleeritavate beeta-agonistide kasutamisel esineb kõige sagedamini tahhükardiat ja treemorit. Mõnikord - hüperglükeemia, kesknärvisüsteemi erutus, vererõhu langus. Parenteraalsel kasutamisel on kõik need nähtused rohkem väljendunud.
Üleannustamine
Seda iseloomustab vererõhu langus, rütmihäired, väljutusfraktsiooni vähenemine, segasus jne.
Ravi - beetablokaatorite, antiarütmiliste ravimite jne kasutamine.
β2-agonistide kasutamine tervetel inimestel suurendab ajutiselt vastupanuvõimet füüsilisele aktiivsusele, kuna need "hoivad" bronhid laienenud olekus ja aitavad kaasa varakult "teise tuule avanemisele". Sageli kasutasid seda professionaalsed sportlased, eriti jalgratturid. Tuleb märkida, et lühiajaliselt suurendavad β2-agonistid koormustaluvust. Kuid nende kontrollimatu kasutamine, nagu iga doping, võib põhjustada tervisele korvamatut kahju. β2-adrenomimeetikumidest tekib sõltuvus (selleks, et bronhid "lahti hoida", tuleb annust pidevalt suurendada). Annuse suurendamine põhjustab arütmiaid ja südameseiskuse ohtu.




