Peensoole bakterite hingamistest. Bakteriaalse ülekasvu sündroom (SIBR) peensooles. Patsiendi juhtimise põhiaspektid
bakteriaalse ülekasvu sündroom- sümptomite kompleks, mis tekib siis, kui mikroorganismide kontsentratsioon peensooles ületab 10 5 rakku / ml aspireeritud sisus.
Bakterite liigse kasvu sündroomi peamised ilmingud on: iiveldus, korin kõhus, kõhulahtisus, malabsorptsiooni sündroom, kehakaalu langus. Sündroomi diagnoosimiseks viiakse läbi peensoole sisu aspiratsioon külvi jaoks; tehakse hingamistestid. Liigse bakteriaalse sündroomiga patsientide ravi viiakse läbi antibakteriaalsete ravimitega.
- Bakteriaalse ülekasvu sündroomi epidemioloogia
Bakteriaalse kasvu sündroomi tekkerisk on vastsündinutel, väikelastel ja eakatel (eriti alatoitumusega inimestel).
USA-s areneb ligikaudu 20–43% diabeediga patsientidest bakteriaalne ülekasvu sündroom.
Bakterite ülekasvu sündroom põhjustab 50% vastsündinute kroonilisest kõhulahtisusest.
- Bakteriaalse ülekasvu sündroomi etioloogia
Bakteriaalse ülekasvu sündroomi riskitegurid on järgmised:
- Anatoomilised muutused peensooles, mis aeglustavad sisu liikumist läbi seedetrakti. Need muutused ilmnevad järgmiste haigustega patsientidel:
- soolestiku kitsendused,
- soole lümfoomid,
- Ileotsekaalklapi puudumine ja pärast resektsiooni jäänud peensoole pikkus on lastel alla 0,6 m ja täiskasvanutel alla 1,5 m:
- Seedetrakti peristaltika häired:
- diabeetiline neuropaatia,
- amüloidoos,
- sklerodermia,
- Hüpotüreoidism.
- Vesinikkloriidhappe hüposekretsioon (peamine etioloogiline tegur bakteriaalse ülekasvu sündroomi tekkes eakatel patsientidel).
- Immuunsüsteemi häired:
- Immunosupressantide võtmine,
- IgA puudulikkus,
- Hüpogammaglobulineemia.
- Prootonpumba inhibiitorite, näiteks omeprasooli, ranitidiini kasutamine (vesinikkloriidhappe sekretsiooni pärssimise tõttu).
- Anatoomilised muutused peensooles, mis aeglustavad sisu liikumist läbi seedetrakti. Need muutused ilmnevad järgmiste haigustega patsientidel:
- Bakteriaalse ülekasvu sündroomi kliinik
- Bakteriaalse ülekasvu sündroomi peamised kliinilised ilmingud
Bakterite ülekasvu sündroomi peamised ilmingud on:
- Iiveldus.
- Valu ja korin kõhus.
- Kõhupuhitus.
- Kõhulahtisus, steatorröa.
- Enamikul juhtudel väheneb kehakaal.
- Bakteriaalse ülekasvu sündroomiga lastel esineb kasvupeetust.
- Mõnel juhul võib bakterite ülekasvu sündroom olla asümptomaatiline. Samal ajal on patsientidel ainult kehakaalu langus.
- Bakterite ülekasvu sündroomi tüsistused
Pikaajaline ülemäärase bakterite kasvu sündroom põhjustab alatoitumist, vitamiinide (eriti vitamiin B 12) ja mikroelementide (eriti raua) puudust.
Kui tekib B12-vitamiini vaegus, tekib makrotsüütiline aneemia; hüpoferreemia ilmnemisega - mikrotsüütiline aneemia.
- Bakteriaalse ülekasvu sündroomi peamised kliinilised ilmingud
- Bakterite ülekasvu sündroomi diagnoosimine
- Diagnostilised meetodid
- Mitteinvasiivsed diagnostikameetodid
- Diagnostiline algoritm
Bakterite ülekasvu sündroomi diagnoosimise kuldstandardiks on peensoole sisu kultiveerimine ja bakterite suurenenud kontsentratsiooni tuvastamine selles (üle 10 5 raku / ml).
Hingamistestid on diagnostiliselt informatiivsed ja tehnilisest küljest lihtsamini teostatavad. Soovitatav on teha kolm testi: vesinik, ksüloos ja sapphape, kuid ksüloos on kõige spetsiifilisem.
Bakteriaalse ülekasvu sündroomiga täiskasvanud patsientide uriinianalüüsides on võimalik määrata 4-hüdroksüfenüülatsetoonhappe taset. Tuleb meeles pidada, et 2% juhtudest on võimalik saada valepositiivseid tulemusi.
- Diagnostilised meetodid
- Bakterite ülekasvu sündroomi ravi
Bakteriaalse ülekasvu sündroomiga patsientide ravi viiakse tavaliselt läbi rifaksimiiniga (Alpha Normix) annuses 1200 mg päevas. See annus tagab 60% dekontaminatsiooni määra.
Bakteriaalse ülekasvu sündroomi raviks on ette nähtud ka järgmised ravimid:
- tetratsükliin (tetratsükliinvesinikkloriid) - suu kaudu täiskasvanutele, 500 mg 4 korda päevas; alla 8-aastased lapsed ei ole soovitatavad.
- gentamütsiin sees 50 mg / kg / päevas 4-6r / päevas (mitte rohkem kui 360 mg / päevas).
- amoksitsilliin / klavulaanhape (Augmentin) - täiskasvanutele sees.250-500 mg 2 korda päevas; lapsed - 40 mg / kg / päevas 2r / päevas.
- klindamütsiin (Dalacin, Clindamycin) - täiskasvanutele sees, 300 mg 3 korda päevas; IV 600-2700 mg/päevas 2 korda päevas; lapsed - sees 30 mg / kg / päevas 2r / päevas; IV annuses 40 mg/kg/päevas 2-4 korda päevas.
- Amoksitsilliin/klavulaanhape on ette nähtud suhkurtõvega patsientidele.
- Eakatele patsientidele soovitatakse klindamütsiini ja metronidasooli.
- Gentamütsiin parandab oluliselt alla üheaastaste laste seisundit, kellel on bakteriaalne ülekasvu sündroom.
- Pärast antibiootikumravi lõppu tuleb patsienti jälgida mitu kuud.
- On vaja ravida haigust, mis viis bakteriaalse ülekasvu sündroomi ilmnemiseni.
- Bakterite ülekasvu sündroomi ennustamine ja ennetamine
Bakterite ülekasvu sündroomi ennetamine taandub selle arenguni viinud haiguse ennetamisele.
Kui põhjust, mis põhjustas bakteriaalse ülekasvu sündroomi, ei kõrvaldata, võib see korduda.
Paratamatult kaasneb EPI-ga seedimise ja toitainete omastamise halvenemine, mis võib viia malabsorptsiooni tekkeni. Arvatakse, et piisav ravi ensüümpreparaatidega peaks kompenseerima endogeensete ensüümide vaeguse ja taastama normaalse seedimise. Praktikas pole aga kaugeltki alati võimalik EPI-ga lihtsalt toime tulla. Selle peamine põhjus on reeglina seotud ensüümi ainete ebapiisava annuse või ebaefektiivse ravimi valikuga. EPI püsival kulgemisel ja ensüümravi esmapilgul madalal efektiivsusel on teine, väga tõsine põhjus. Seda seostatakse peensoole bakteriaalse ülekasvu sündroomi (SIBO) tekkega, mida ingliskeelses kirjanduses nimetatakse "bakteriaalseks ülekasvuks". SIBO on paljudele arstidele vähe tuntud ja seda ei võeta ravitaktikas arvesse. Seetõttu oli selle artikli eesmärk tutvustada sisearste ja gastroenterolooge kaasaegsete lähenemisviisidega SIBO korrigeerimiseks CP-s. Seedetrakti normaalne mikrofloora
Kaasaegsetest positsioonidest vaadeldes peetakse inimese normaalset mikrofloorat (normofloora, mikrobioota) paljude mikrobiotsenooside kogumina, mis hõivavad arvukalt ökoloogilisi nišše (biotoope) kõigi väliskeskkonnale avatud kehaõõnsuste nahal ja limaskestadel. Bakterite koguarv täiskasvanul on 1015 rakku, mis on üle 10 korra suurem kui makroorganismi enda rakkude arv. Praegu kehtiv normatiivdokument "Venemaa düsbakterioosi tööstuse standard" pakub normaalse taimestiku järgmist määratlust: see on "üksikute organite ja süsteemide erinevate mikroobide populatsioonide kvalitatiivne ja kvantitatiivne suhe, mis säilitab makroorganismi biokeemilise, metaboolse ja immunoloogilise tasakaalu. inimeste tervise säilitamiseks vajalik." Sellest määratlusest järeldub, et iga biotoobi normofloora täidab arvukalt funktsioone mitte ainult selle toimimise, vaid ka kogu keha homöostaasi säilitamiseks.
Seedetrakti iga biotoobi (GIT) mikrofloora liigiline ja kvantitatiivne koostis on nii peremeesorganismi kui ka mikrobiota enda arvukate kaitsefaktorite mõju tõttu üsna konstantne:
geneetiline eelsoodumus
Happeline maokeskkond
Seedetrakti normaalne motoorne evakueerimisfunktsioon
Seedetrakti anatoomilised sulgurlihased
Pidev intraluminaalse pH tase erinevates biotoopides
Limaskestade immuunsüsteemi seisund
Limaskestade poolt toodetud bakteritsiidsed ained (lüsosüüm, laktoferriin jne)
Limaskesta makrofaagide fagotsüütiline aktiivsus
Sekretoorne IgA
Bakteriaalsed kolitsiinid ja mikrotsiinid (mikroobse päritoluga endogeensed peptiidantibiootikumid)
Ainult inimese seedetraktis on üle 400 bakteriliigi - 17 erineva perekonna esindajad. Inimese seedetraktis elavad bakterid ebaühtlaselt.
Nagu tabelist näha, on mikroobse saastumise suurim tihedus käärsooles ligikaudu 400 erineva liigiga. Käärsoole mikroobirakkude kogubiomass on ligikaudu 1,5 kg, mis vastab 1011–1012 CFU/g sisu kohta ja moodustab umbes 1/3 väljaheite kuivkaalust. Just jämesool kannab nii suure saastatuse tõttu teiste biotoopidega võrreldes suurimat funktsionaalset koormust. Bakterite sisaldus ülasooles varieerub kitsas vahemikus 103–104 CFU/ml soolesisu kohta.
Bakteroidid, eubakterid, bifidobakterid, peptostreptokokid, ruminokokid, klostriidid ja laktobatsillid moodustavad suurema osa bakteritest peensoole jämedas ja alumises osas ning bakteroidid, laktobatsillid ja kokid peensoole ülemistes osades (Table peensoole). Vaatamata suhteliselt väikesele mikroorganismide arvule proksimaalses peensooles, on nende funktsioonid väga olulised selle biotoobi elutegevuseks, eelkõige luminaalse pH ja limaskesta immuunstaatuse säilitamiseks. Seedetrakti normaalne mikrofloora tervikuna täidab metaboolseid, kaitsvaid, antimutageenseid ja kantserogeenseid funktsioone. Metaboolsed ja kantserogeensed funktsioonid langevad peamiselt käärsoole floorale ning kõigi biotoopide mikrofloora osaleb antitoksiliste, kaitse- ja immuunfunktsioonide elluviimises, kolonisatsiooniresistentsuse ja mikroobide antagonismi säilitamises patogeenide ja oportunistlike patogeenide suhtes. See kehtib ka peensoole ülemiste osade kohta. Kolonisatsiooniresistentsuse all mõistetakse mehhanismide kogumit, mis tagab mikroobipopulatsioonide liigi püsivuse ja kvantitatiivse koostise konkreetses biotoobis, takistades oportunistliku ja patogeense taimestiku paljunemist ning selle ümberpaigutamist mitteiseloomulikesse biotoopidesse ja organismi sisekeskkonda. Sellise mikrofloora translokatsiooni ilming võib olla SIBO peensooles koos viimase mikroobse saastumise suurenemisega rohkem kui 104 CFU/ml soolesisu kohta.
Ülemäärase bakterite kasvu sündroom (ülemäärase saastumise sündroom - bakterite ülekasv)
Nagu eespool mainitud, kõigub soolestiku ülaosa bakterite normaalne sisaldus kitsas vahemikus 103-104 CFU / ml soolesisalduse kohta ja see väärtus on omamoodi konstant peensoole jaoks. Ka mikrobiota liigiline koosseis on üsna püsiv: bakteroidid, laktobatsillid, kokid.
Võttes kokku olemasolevad definitsioonid, saame meie vaatenurgast anda SIBO sündroomi järgmise definitsiooni: bakteriaalne ülekasvu sündroom on peensoole proksimaalsete osade saastumine üle 104 m.k. (CFU) / ml soole sisu oportunistliku mikrofloora tõttu, mis pärineb seedetrakti ülaosast (või ülemistest hingamisteedest) või käärsoole mikrobiota oportunistlike esindajate retrograadse translokatsiooni tõttu.
Tuleb rõhutada, et SIBO mõiste viitab rahvusvahelises kirjanduses ainult peensoole taimestiku ülekasvule, kuid mitte jämesoole.
SIBO-le viivad mitu peamist mehhanismi. Esimene mehhanism on tingitud mis tahes päritolu hüpo- või akloorhüdriast. Kaitsva happebarjääri vähenemine võimaldab suuõõne ja ülemiste hingamisteede mikroobidel koloniseerida makku ja seejärel peensoole. See protsess võib põhineda erinevatel põhjustel, kuid enamasti toimub see peensoole mikroobse saastumise tee pärast maovähendusoperatsiooni või maovähendusoperatsiooni, maosekretsiooni inhibiitorite pikaajalisel kasutamisel, autoimmuunse gastriidi korral, autoimmuunhaigustega nagu pernicious aneemia ja sklerodermia. .
Teine SIBO arengu mehhanism on tingitud nn "soolestiku kliirensi" rikkumisest, st. peensoole võime rikkumine kõrvaldada sinna sattunud patogeenid või oportunistlikud mikroorganismid. Kliirensi halvenemine ilmneb peensoole mikrobiota püsivust säilitavate kaitsemehhanismide aktiivsuse vähenemisega: motoorse aktiivsuse pärssimine, bakteritsiidsete ainete ja sekretoorse IgA sünteesi vähenemine, makrofaagide fagotsüütilise funktsiooni vähenemine. peensoole limaskest jne.
Kolmas mehhanism on seotud mikrofloora retrograadse translokatsiooniga jämesoolest peensoolde, mis on tingitud ileotsekaalklapi puudulikkusest põletiku või jämesoole motoorsete häirete korral. Peaaegu iga gastroenteroloogiline haigus võib põhjustada SIBO arengut.
SIBO hindamise meetodid
SIBO diagnoosimine on väga raske, kuna peensoole sisu proovide võtmise meetodid on liiga töömahukad. Selleks on välja töötatud lihtne ja mugav meetod vesiniku kontsentratsiooni määramiseks väljahingatavas õhus pärast süsivesikute koormust glükoosi või laktoosiga (vesinikhingamise test). SIBO juuresolekul on vesiniku tase väljahingatavas õhus kõrge, kuna peensooles tekivad mikroobsed metaboliidid. Sama meetodiga saab jälgida ravi tulemusi erinevate ravimitega, mis pärsivad peensoole liigse floora kasvu. Meetod on odav, seda on lihtne teostada, kuid kahjuks ei kasutata seda Venemaal laialdaselt.
Krooniline pankreatiit ja SIBO
Vastavalt J.E. Dominguez-Munoz, SIBO esineb 40% CP-ga patsientidest ja see on üks levinumaid põhjuseid, mis põhjustab ensüümasendusravi ebapiisava efektiivsuse.
Seega on HP-ga kaasas:
Seedimise ja imendumise protsesside rikkumine
Bakterite ülekasvu areng peensooles
Seedetrakti motoorse funktsiooni rikkumine
Esmane õõnes seedimise rikkumine CP-s keeruliste mehhanismide koostoime kaudu süveneb membraanide seedimise rikkumisega ja kõik osalevad mehhanismid töötavad nõiaringi põhimõttel.
Bakterite ülekasvu sündroomi ravi
Tuleb meeles pidada, et SIBO ei ole iseseisev patoloogia, vaid ainult sekundaarne sündroom, mis kaasneb paljude patoloogiliste seisunditega. Kui reeglina ei esine käärsoole mikrobiota rikkumiste puhul selgelt määratletud kliinilisi sümptomeid, siis SIBO korral tekivad tavaliselt kõhupuhitus, väljaheitehäired ja mõnikord ka tõsine kõhulahtisus. Samas ei ole kõik need sümptomid spetsiifilised ning neid ei ole võimalik üheselt SIBO-ga seostada. Selle artikli kontekstis võivad kõhupuhitus, kõhulahtisus, stetorröa olla võrdselt nii EPI kui ka SIBO tagajärg.
Igal juhul on mikroobsed häired nii jäme- kui peensooles alati teisejärgulised, mistõttu on nende korrigeerimiseks vaja ennekõike kõrvaldada neid põhjustavad negatiivsed tegurid (näiteks meditsiinilised või keskkonnamõjud) või ravida. põhihaigus. Oluline on rõhutada, et SIBO korrigeerimine ei ole eesmärk omaette ja see viiakse läbi:
Kui selle põhjust ei ole võimalik kõrvaldada
Püsiva agressiivse teguri (näiteks keemiaravi) toimel
Täiendava meetmena neid häireid põhjustanud põhihaiguse ravi ebapiisava efektiivsusega.
Nende sätete ideaalne näide on EPI taustal arenev SIBO. Ideaaljuhul taastub seedimine, kui määratakse piisav annus ensüümipreparaate ja SIBO täiendav korrigeerimine pole vajalik. SIBO on aga üks levinumaid põhjuseid, mis põhjustab ensüümasendusravi ebapiisava efektiivsuse. Ühes uuringus hinnati Creon-ravi mõju SIBO-le (vesinikhingamise testi järgi) 15 patsiendil, kellel oli CP-s EPI. Need patsiendid 2 kuu jooksul. läbiviidud ravi Creoniga 100-150 tuhat RÜ päevas. Enamikul (65% - 10 patsienti) korduva vesiniku testi järgi SIBO elimineeriti, 53% (8 patsienti) kõhupuhitus kadus, 73% (11 patsienti) oli enesetunne paranenud, kuid düspeptiline. sümptomid püsisid.
Eespool öeldu põhjal peaks EPI-ga koos SIBO-ga või ilma pankreasehaiguste esmavaliku raviks piisavate annuste manustamine efektiivsete ensüümi ainete (Creon 25 000–40 000 RÜ iga toidukorra ajal) manustamine. Selle ebapiisava efektiivsusega on näidustatud ravimite määramine peensoole mikroobide kasvu kõrvaldamiseks. Mikroobsete häirete terapeutiline taktika sõltub nende raskusastmest, kliiniliste ilmingute olemasolust ja bakterite ümberpaigutusest teistesse biotoopidesse. Mõnel juhul on SIBO juuresolekul vaja läbi viia "soolestiku selektiivne mikroobne puhastamine". See kontseptsioon hõlmab soolestiku sanitaarhooldust (saastusest puhastamist) ravimitega, mis pärsivad selektiivselt võõrfloora kasvu ega mõjuta normofloorat. Desinfitseerimiseks kasutatakse mitut ainete rühma:
Antibakteriaalsed ravimid
Mittepatogeensed seened
Spoore moodustavad preparaadid, mis põhinevad mööduva taimestiku esindajatel
mikroobsed metaboliidid.
Antibiootikumid
Optimaalne antibakteriaalne ravim peensoole puhastamiseks ja SIBO eemaldamiseks peab vastama järgmistele nõuetele:
Imenduvad soolestikust minimaalselt
Looge sooleõõnes kõrge kontsentratsioon
Selektiivsus (peaks pärssima võõrfloorat ega mõjuta normofloorat
Sellel on lai antimikroobse toime spekter, sealhulgas aeroobid ja anaeroobid
Omage minimaalselt kõrvaltoimeid ja olge ohutu
On tõestatud kliiniline efektiivsus
Üks uusimaid Venemaal ja kõigist kolmest vaatenurgast kõige huvitavam ravim on rifamütsiini derivaat - ravim rifaksimiin (Alfa-normix). See ei ole imenduv<1%) при приеме внутрь антибиотик, достигающий высоких концентраций в слизистой оболочке ЖКТ.
Ravim ei toimi väljaspool seedekulglat, s.t. on lokaalselt toimiv soole antiseptik. Rifaksimiin on hästi talutav, sellel on minimaalselt kõrvaltoimeid ja see ei põhjusta bakterite resistentsust. Ravimil on lai spekter antibakteriaalset toimet grampositiivsete (Enterococcus spp, M. tuberculosis, Streptococcus pyogenes, Streptococcus faecalis, Streptococcus pneumoniae, Staphylococcus epidermidis, Staphylococcus aureus) ja gramnegatiivsete (Salgerich, Salgeellas colipp) vastu. Yersinia enterocolica, Proteus spp, Vibrio cholerae) aeroobsed bakterid ja grampositiivsed (Clostridium perfrigens, Clostridium difficile, Peptococcus spp, Peptostreptococcus spp) ja gramnegatiivsed (Bacteroides spp, Bacterolicobes. See toimespekter määrab ravimi terapeutilise potentsiaali. Seega rahuldab rifaksimiin kõik ideaalse antibakteriaalse ravimi põhinõuded. Seda on edukalt kasutatud ägedate sooleinfektsioonide korral, käärsoole puhastamiseks düsbakterioosiga, SIBO korrigeerimiseks, antibiootikumidega seotud soolekahjustuste ja hepaatilise entsefalopaatia korral. Vesiniku hingamistestiga tõestatud SIBO korral kasutatakse rifaksimiini 400 mg 3 korda päevas 7 päeva jooksul. Samal ajal väheneb väljahingatava vesiniku tase juba kolmandaks ravipäevaks 3–5 korda, mis viitab peensoole kiirele sanitaarsusele.
Pikka aega on SIBO raviks erinevate patoloogiate korral kasutatud erinevaid antibiootikume (tetratsükliinid, linkomütsiin, ampitsilliin jt), mis ei ole selektiivsed, ei mõjuta anaeroobset floorat, imenduvad kiiresti seedetraktist ja millel on laia valikut kõrvaltoimeid (sh antibiootikume).kaasnev kõhulahtisus) ja pärsivad normaalset taimestikku. Rifaksimiini efektiivsuse demonstreerimiseks viidi läbi topeltpime uuring, mis kinnitas rifaksimiini prioriteetsust tetratsükliini ees SIBO-s. Selles uuringus hinnati SIBO-d kahes patsientide rühmas vesiniku hingamistesti abil ning määrati vesiniku eritumise tipp väljahingatavas õhus ning vesiniku kogukontsentratsioon pärast glükoosikoormust enne ja 3 päeva pärast antibiootikumikuuri lõppu. Näidati, et vesiniku võrdse algtaseme korral oli selle tipp pärast glükoosi laadimist, samuti kogukontsentratsioon väljahingatavas õhus pärast ravi, oluliselt madalam rifaksimiiniga ravitud patsientidel võrreldes kloortetratsükliiniga ravitud rühmaga.
Teiste tõhusate antibakteriaalsete ainete hulka kuuluvad oksükinolooni derivaadid, väheimenduvad nitrofuraani derivaadid (nifuroksasiid) ja nitroimidasoolid (metronidasool, tinidasool). Kuigi viimane rühm imendub jämesoolest, on selle kasutamine siiski tõhus, peamiselt anaeroobsete mikroorganismidega saastumise korral. SIBO dekontaminatsioonikuuri kestus on 12–14 päeva.
Mittepatogeensed seened
Antibakteriaalsete ravimite talumatuse korral on võimalik ja efektiivne määrata ravimeid, mis põhinevad perekonna S. boulardii mittepatogeensetel pärmseentel. Samas ei inhibeeri S. boulardii kohustuslike mikroorganismide kasvu sooleõõnes ja on resistentne soolhappe toimele. Igapäevase tarbimise korral leidub neid seedetrakti kõikides osades, sealhulgas peensooles. Need pärmseened on inimese jaoks mööduv taimestik, mistõttu 2–5 päeva pärast ravimi võtmise lõppu eemaldatakse need organismist täielikult ilma kõrvaltoimeteta. Ravim ei imendu seedetrakti luumenist ja on lokaalselt toimiv soole antiseptik. S. boulardii antimikroobne toime määrati kindlaks in vitro ja in vivo sooleinfektsioonide patogeenide (Cl. difficile, Salmonella, Shigella, Yersinnia), algloomade (Giardia ja mitmed) oportunistlike mikroorganismide (patogeensed kokid, seened, Klebsiela jne) vastu. .), mis võib viia SIBO arenguni.
Eoseid moodustavaid mittepatogeenseid antibakteriaalseid aineid saab SIBO-s kasutada ka talumatuse korral alternatiivina antibiootikumidele. Sellesse rühma kuuluvad ravimid, mis põhinevad heinabacillil Bacillus subtilis ja sarnasel mikroorganismil B. cereus. Eosmikroorganismid on inimese jaoks mööduv taimestik, seetõttu eemaldatakse need pärast tarbimise lõpetamist kiiresti soolestikust. Nende ravimite toimemehhanism on tingitud happeliste metaboliitide moodustumisest eluprotsessis ja pH langusest kogu soolestikus, pärssides seeläbi oportunistliku floora kasvu. Lisaks sünteesivad need ravimid mitmeid seedeensüüme, kompenseerides osaliselt soolestiku enda ensüümi aktiivsuse vähenemist, kui seda kahjustavad bakterid ja nende toksiinid. SIBO ravikuur on 10–14 päeva. Pikem kursus on ebasoovitav, sest. B. cereus on võimeline tootma enterotoksiine, mis põhjustavad kõhulahtisust.
Mikroobsed metaboliidid
Täiendav aine, mis taastab valdavalt peensoole mikrofloora, on mikroobne metaboliit hilak forte. Peamised bioloogiliselt aktiivsed komponendid, millest hilak forte koosneb, on lühikese ahelaga rasvhapped (SCFA) ja piimhape, mis on saadud normaalse soole mikrofloora sahharolüütilistest ja proteolüütilistest esindajatest. Bioloogiliselt aktiivsete ainete kontsentratsioon ühes ravimi tilgas vastab 1010 bakteri vastavate metaboliitide toimele. Hilak forte toimemehhanismi mikrobiota koostise ja funktsioonide normaliseerimisel ning soolestiku aktiivsuse taastamisel vahendavad selle koostiskomponendid. Preparaadis sisalduvad SCFA-d annavad limaskestadele lisaenergiat, soodustavad sooleseina kahjustatud epiteelirakkude taastumist ja parandavad limaskesta trofismi. Happeliste metaboliitide (SCFA, piimhape) mõju tagab intraluminaalse pH reguleerimise, mis põhjustab patogeenide ja oportunistlike patogeenide kasvu pärssimist kogu soolestikus.
Seega tuleks CP SIBO-ga ravimise taktika üles ehitada järgmiselt:
Piisav ensüümravi (Creon 75 000 RÜ või rohkem päevas)
Peensoole saastest puhastamine: antibiootikumravi (rifaksimiin)
Mikroobsed metaboliidid
Käärsoole mikrobiotsenoosi normaliseerimine pro- ja prebiootikumidega (vajadusel)
Motoorsete häirete kõrvaldamine - kaksteistsõrmiksoole hüpertensioon, kiirendatud tõukejõud (vajadusel).
Soolestiku bakteriaalse ülekasvu sündroom (SIBO) on patoloogiline seisund, mis on põhjustatud peensoole koloniseerimisest fekaalse mikroflooraga. SIBO-ga kaasneb kõhulahtisus ning rasvade ja vitamiinide malabsorptsioon.
See on soolestiku patoloogiliste häirete tagajärg ja selle põhjuseks on seedimata toidujääkide sattumine jämesoolde, mis aitab kaasa täiendavate mäda- ja pärmibakterite kolooniate tekkele, mis häirivad seedetrakti. Escherichia coli mürgised ained, mis satuvad vereringesse, põhjustavad mürgistust, mis põhjustab seedekulglas põletikulisi muutusi.
Epidemioloogia
SIBO põhjused
Kui laps sünnib, on tema sooled steriilsed. Järgmiste nädalate jooksul koloniseerivad seedetrakti streptokokid, laktobatsillid ja enterokokid. Lisaks väheneb järsult kolibakterite arv peensooles ja jämesooles paljunedes muutuvad need normiks.
SIBO patoloogilises seisundis tekib tsekoileaalne refluks, mis põhjustab gaasi moodustumise suurenemist ja peen- ja jämesoole peristaltika täiendavat stimuleerimist.
Riskitegurid
Põhjused, mis põhjustavad soolestikus liigse bakterite kasvu sündroomi ilmnemist, on järgmised: peensoole morfoloogilised või hävitavad tunnused, mis aitavad kaasa toidu osalisele pärssimisele läbi seedesüsteemi. Selle põhjuseks on patoloogilised seisundid: pikaajaline stress, erineva etioloogiaga enteropaatiad, püsivad põletikulised soolehaigused, kolangiit jms.
Peensoole mikrofloora tasakaalu patoloogilisi muutusi põhjustavate tegurite hulka kuuluvad:
- ileotsekaalse klapi toimimise rikkumine;
- kirurgilised sekkumised - pimeda silmuse moodustamine, koletsüstektoomia, peensoole resektsioon jne;
- seedesüsteemi haigused, mis põhinevad soolemotoorika häiretel (krooniline kõhukinnisus, gastrostaas, duodenostaas);
- kõhuõõne seedimise ja imendumise patoloogilistest muutustest põhjustatud seisundid (malabsorptsioon ja seedimine);
- sekretoorse puudulikkusega seotud patoloogilised muutused kõhunäärmes;
- sapiteede patoloogilised seisundid;
- pidev toitumise tasakaalustamatus, soolepõletik, divertiikulid, lühikese soole sündroom;
- immunosupressiivsed patoloogiad AIDSi ja keemiaravi korral, antibiootikumid;
- soolestiku ja ümbritsevate lümfisõlmede kasvajad
- Crohni tõbi.
- tsöliaakia
- hüpogammaglobulineemia
Patogenees
SIBO patogenees koosneb järgmistest elementidest:
- Lipiidide, valkude, polüsahhariidide, vitamiinide halb imendumine põhjustab enterotsüütide funktsioonide pärssimist ja bakteriaalseid muutusi toitainekeskkonnas toksilise ja mitteimenduva seisundini.
- Anaeroobne taimestik põhjustab sapphapete patoloogilisi muutusi ja jätab need seedimisprotsessist välja. Muutunud happed ja süsivesikute killud provotseerivad lahtist väljaheidet.
- Anaeroobsed mikroorganismid absorbeerivad vitamiini B12, mis põhjustab makrotsüütilise aneemia teket.
SIBO sümptomid
SIBO sümptomid on järgmised: iiveldushood, suurenenud gaasi moodustumise nähtused, kõhulahtisus, malabsorptsiooni sündroom, püsiv kaalulangus. SIBO aitab diagnoosida selliseid spetsiifilisi uuringuid nagu: peensoole sisu aspiratsioon kultiveerimiseks ja hingamistestid.
Sümptomid on jagatud kahte rühma:
- Kõhuõõne põhjustatud patoloogilistest protsessidest kõhuõõnes, üsna sagedane puhitus ja korin kõhus, mõnikord iiveldus, mis tekib mõni aeg pärast söömist. Tooli ebastabiilsus.
- On levinud, mis põhinevad rasvlahustuvate vitamiinide, tsüanokobalamiini ja foolhappe, raua puudusel, mis põhjustab töövõime langust, väsimust, impotentsust, letargiat, peapööritust ja kehakaalu langust. Vitamiinipuuduse seisundit iseloomustab naha kuivus, hägune nägemine õhtuhämaruses; suurenenud ärevus, meeleolu kõikumine, närvilisus.
Tüsistused ja tagajärjed
SIBO diagnoos
Anamneesi hoolikas kogumine tagab täpse diagnoosi. Patsiendilt küsitakse üksikasjalikult seedetrakti funktsionaalsete haiguste esinemist, millega kaasneb erineva intensiivsusega valu kõhus, kõhupuhitus, kõhulahtisus.
Diagnoos – SIBO eeldab laboratoorsete testide ja erinevate uurimismeetodite (mitteinvasiivne, invasiivne) kasutamist.
Patoloogilise mikrofloora tüübi määramiseks on kohustuslik külvata peensoole aspiratsioonimassid. Tüüpiline diagnostiline test on hingamistest.
SIBO-ga koprogrammis jäävad seedimata toidujäägid, määratakse liigse koguse rasva moodustumine. Läbi viidi peensoole seinte intestinoskoopia ja biopsia.
Bakterite ülekasvu sündroomi hingamistest
Glükoosi test. See põhineb patsiendi poolt väljahingatavas õhus oleva vesiniku tuvastamisel spetsiaalse seadme abil. See viiakse läbi tühja kõhuga. Patsient hingab sügavalt sisse, hoiab hinge kinni 10-15 sekundit. Seejärel hingake aeglaselt välja testimisseadmesse. Laborant kirjutab aparaadi näidud üles. Seejärel joob patsient lahust, millele on lisatud glükoosi. 30-minutilise intervalliga teeb spetsialist kolm korda mõõtmisi väljahingamisel. Vesiniku taseme märgatav tõus näitab probleeme peensooles.
ksüloosi test(ksüloos on süsivesik, mis imendub ainult peensooles). Selle testiga tuvastatakse muutunud CO2, mille teket seostatakse SIBO poolt põhjustatud patsiendi keha metaboolsete reaktsioonide häirega.
Analüüsid
Bakterite ülekasvu sündroomi diagnoosimisel on soovitatav teha laboratoorsed uuringud: täielik vereanalüüs - aneemia määramine (madal hemoglobiin, patoloogiliselt muutunud punased verelibled, madal värvusindeks), põletiku olemasolu (leukotsütoos, kõrgenenud ESR);
Biokeemiline vereanalüüs (kõrgenenud ALT, AST, C-reaktiivse valgu positiivne tulemus).
Uriinianalüüs (suure koguse lima, bakterite olemasolu).
Väljaheidete koproloogiline uuring (avastada seedimata toidujäägid, väljaheidete suurenenud happesus ja kõrge rasvasisaldus)
Bakterioloogiline kultuur (patoloogiliste mikroorganismide kolooniate kiire kasvu tuvastamine).
Instrumentaalne diagnostika
Intestinoskoopia on endoskoopiline meetod. Patsiendi peensoolde sisestatakse selle sisu aspireerimiseks optilise seadmega juht, millele järgneb aspiraadi nakatamine toitainekeskkonnale.
Peensoole biopsia on peensoole koe instrumentaalne püüdmine mikroskoopilise uurimise eesmärgil. Bakterite liigse kasvu sümptomite kompleksis määratakse peensoole patoloogiliselt muutunud atroofilised villid.
Selle põhjustanud SIBO peamise põhjuse (divertikulaar, peensoole vööt jne) tuvastamiseks tehakse röntgenülesvõte.
Diferentsiaaldiagnoos
SIBO tuleks eristada tsöliaakiast ja eksokriinsest pankrease puudulikkusest. Patoloogilised muutused on väga sarnased: nendele haigustele on iseloomulik osaline villi atroofia, krüpti hüperplaasia, lümfotsüütide kogunemine epiteeli enda kihti. Diferentsiaaldiagnoosi selgitamine nõuab spetsiifilisi uuringuid.
SIBO ravi
Ravi peaks olema keerulise etiopatogeneetilise iseloomuga. On vaja kõrvaldada patoloogia, mis põhjustas SIBO esinemise.
Patsiente ravitakse antibakteriaalsete ravimitega, vitamiinidega, pro- ja prebiootikumidega, absorbentidega.
Antibiootikumi valimise otsus põhineb peensoole aspiraadi bakterioloogilise analüüsi tulemustel ja patoloogilise floora ravimite tundlikkuse analüüsidel. SIBO-ga patsientide ravi viiakse läbi laia toimespektriga antibiootikumidega rifaksimiinööpäevases annuses 1200 mg.
Täiskasvanud kasutavad aktiivselt tetratsükliini antibiootikume, näiteks tetratsükliinvesinikkloriid- 0,5 g 4 rubla päevas. Vastunäidustatud alla 8-aastastele lastele. Kõrvaltoimed väljenduvad suurenenud intrakraniaalse rõhu, pearingluse, nõrkuse, allergiliste ilmingute, valgustundlikkuse kujul.
Amoksitsilliin. Täiskasvanud - sees 0,25-0,5 g 2 rubla / päevas; lapsed - 40 mg / kg / päevas 2r / päevas. Kõrvaltoimete võimalikud ilmingud - sügelus, naha punetus, Quincke ödeem, anafülaktiline šokk.
Bakteriaalse ülekasvu sündroomi edukaks raviks soolestikus on vaja luua ainulaadsed tingimused, millel on kasulik mõju normaalse mikrofloora taastamisele ja soole koloniseerimisele bifiduse ja laktobatsillidega. Neid omadusi omavaid ravimeid nimetatakse pre- ja probiootikumideks.
"Kolibakteriin". See sisaldab E. coli M-17 tüve eluskultuure, millel on antagonism patogeense ja oportunistliku mikrofloora suhtes. Tavaliselt võtke 6 kuni 10 annust ühe või kahe annusena (võtke ravim 40 minutit enne sööki) kuu jooksul.
"Bificol". See ühendab samaaegselt kultiveeritud bakterid E.coli M-17 ja bifidobakterid. Päevane määr on 6 kuni 10 annust.
vitamiinid
Patsientidele, kellel on probleeme kaalulangusega või teatud vitamiinide ja mineraalainete puudusega, määratakse vitamiinipreparaadid, mis sisaldavad vitamiini B12, askorbiinhapet, rasvlahustuvaid vitamiine, kaltsiumi ja magneesiumi (Undevit, Supradin, Multi-tabs immuno plus, Vitrum, Revit ) .
Füsioteraapia ravi
SIBO füsioterapeutilise ravina võetakse suu kaudu sooja mineraalvesinikkarbonaadi-kloriidi ja naatrium-kaltsiumi vett. Need pärsivad intensiivset motoorikat ja vähendavad seeläbi roojamise sagedust. Seedetraktis taastab ja korrigeerib mineraalvesi erinevat tüüpi ainevahetust. Soovitatav võib olla vastuvõtt - Borjomi, Narzan, Slavjanovskaja jne.
Alternatiivne ravi
kohupiima vadak. See on valmistatud keefirist, mis pannakse kuuma vette, kus see läbib kohupiimaks ja vadakuks eraldumise. Seerum kurnatakse hoolikalt ja seda kasutatakse düsbakterioosi efektiivseks raviks.
Keefiri klistiir. Keefir (80 g) kuumutatakse ja manustatakse lapsele enne magamaminekut.
mustikatarretis SIBO raviks valmistage retsepti järgi: segage supilusikatäis mustikaid supilusikatäis tärklise ja väikese koguse veega. Lisa peenikese joana veel klaas vett ja aja pidevalt segades segu keema. Tarretist soovitatakse juua soojalt.
SIBO on määratletud kui bakterite liigne vohamine peensooles. Seda sündroomi on veel vähe uuritud haigus. Inglise keeles kõlab see nagu SIBO.
Algselt arvati, et SIBO (bakteriaalse ülekasvu sündroom) esineb vaid vähesel hulgal patsientidel, kuid nüüdseks on selge, et häire on sagedasem. Siiski kogevad bakteriaalse ülekasvu sündroomiga patsiendid mitmesuguseid sümptomeid: krooniline kõhulahtisus, kehakaalu langus ja imendumishäire, kuigi esinevad väikesed sümptomid.
Bakteriaalse ülekasvu sündroom: sümptomid ja ravi
SIBO-ga patsiendid võivad kannatada ka alatoitumise ja osteoporoosi all. Levinud eksiarvamus on olnud, et SIBO mõjutab ainult piiratud arvu patsiente, kellel on seedetrakti ülaosa anatoomilised kõrvalekalded või liikumishäired.
Tänu uutele diagnostilistele testidele on aga teatavaks saanud, et tegemist on sagedasema haigusega, sest üldised kõhulahtisuse ja kaalulanguse sümptomid võivad olla erinevate häirete põhjuseks.
Seetõttu on maoprobleemidega tegelemisel kõige esimene samm kindlaks teha, kas sümptomi põhjuseks on bakterite liigne vohamine maos.
Mis on SIBR?
See lühend tähistab bakterite ülekasvu peensooles.. Need. see tingimus on tingitud liiga palju mikroobe peensooles.
Kõik teavad, et terves seedetraktis on bakterid normaalsed. Kõik bakterid on erineva tüübi ja kontsentratsiooni poolest sõltuvalt nende asukohast seedesüsteemis.
Mõned bakterid, näiteks probiootikumid, on meie kehale väga kasulikud. Kuid muud tüüpi bakterid, mis on ühes kohas kasulikud, võivad olla teises kohas väga kahjulikud.
Nii et SIBO tekib siis, kui peensoolde siseneb liiga palju käärsoole baktereid.
SIBO on määratletud kui peensoole bakteripopulatsioon, mis ületab 105–106 mikroorganismi ml kohta.
Tavaliselt peaks peensoole ülaosas olema alla 103 mikroorganismi/ml ja enamik neist on gramnegatiivsed mikroorganismid.
Lisaks mikroorganismide absoluutarvule mängib vohamise tunnuste ja sümptomite ilmnemisel olulist rolli ka olemasoleva mikroobse floora tüüp.
Näiteks sapisoolasid lahustumatuteks ühenditeks metaboliseerivate bakterite ülekaal põhjustab malabsorptsiooni või kõhulahtisust.
Mikroorganismid, mis muudavad peamiselt süsivesikuid lühikese ahelaga rasvhapeteks ja gaasideks, põhjustavad puhitus ilma kõhulahtisuseta.
Gramnegatiivsed bakterid, näiteks Klebsiella liigid, toodavad toksiine, mis kahjustavad limaskesta ja häirivad imendumist.
SIBO ja peensool
SIBO-d põhjustavad bakterid asuvad tavaliselt jämesooles. Haruldasem olukord tekib siis, kui neid leidub mujal kehas peale peensoole, kuigi väikeses kontsentratsioonis.
Peensool on seedetrakti suurim osa. Selles piirkonnas imenduvad vereringesse toidusegud seedemahladega ning oluliste mineraalide ja vitamiinidega.
Peensooles peaks tavaliselt olema vähem baktereid kui jämesooles (umbes 103–104 1 ml vedeliku kohta võrreldes rohkem kui 109 1 ml vedeliku kohta).
Need soolestiku bakterid on vajalikud "halbade" bakteritega võitlemiseks, terve immuunfunktsiooni säilitamiseks, toitainete imendumise parandamiseks ja K-vitamiini tootmise soodustamiseks.
On hästi teada, et sellised probleemid nagu SIBO tekivad siis, kui bakterid jäme- ja peensooles segunevad või lähevad tasakaalust välja. Kuid miks see juhtub, on keerulisem küsimus.
On teada, et SIBO areneb, kui normaalsed homöostaatilised mehhanismid, mis kontrollivad soolestiku bakterite populatsioone, on häiritud. Kaks protsessi, mis kõige sagedamini soodustavad bakterite kasvu, on maohappe sekretsiooni vähenemine ja peensoole düsmotiilsus.
Mis põhjustab SIBO?
Vaatamata selle levimusele ei ole bakteriaalse ülekasvu sündroomi põhjused veel hästi teada.
Uuringud näitavad, et seda sündroomi esineb paljudel inimestel, kuid sümptomid on inimestel väga erinevad.
SIBO algab teadaolevalt mitmel põhjusel, alates üldisest vananemisest kuni peensoole defektide, diabeedi ja pankreatiidini. Regulaarsel antibiootikumide kasutamisel on häiritud ka seedebakterite tasakaal, mis põhjustab selle seisundi.
Sellele aitavad kaasa ka mõned soolestiku füüsilised takistused, nagu kirurgilised armid või Crohni tõbi.
Selle arengu kõige olulisem tegur on aga lihtsate suhkrute, rafineeritud süsivesikute, pärmi või alkoholiga täidetud toitude regulaarne tarbimine.
Kas tasub karta?
Kui see on korralikult tasakaalus, aitavad käärsooles olevad bakterid toitu seedida ja organism omastab olulisi toitaineid. Kui aga bakterid tungivad peensoole ja võtavad selle üle, võib see põhjustada toitainete halva imendumise ja isegi mao limaskesta kahjustusi.
SIBO puhul läbib toit peensoole ning liigsed bakterid häirivad tervet seedimist ja imendumist. Bakterid tarbivad tegelikult teatud toite ja toitaineid, mille tagajärjeks on ebameeldivad sümptomid, sealhulgas valu.
Kas on põhjust muretsemiseks, kui SIBO kahtlustatakse? Mida kauem te ilma ravita elate, seda hullem on mõju.
Bakterite liigne kasv võib põhjustada toitainete malabsorptsiooni, mis põhjustab seedehäireid, nagu gaas, puhitus ja isegi lekkiva soole sündroom.
Raud, kaltsium ja teised vitamiinid on vajalikud igale organismile. Vitamiini malabsorptsioon põhjustab alatoitumist, üldist nõrkust, vaimset stressi ja isegi pikaajalisi närvikahjustusi.
Kuna SIBO võib kahjustada soole limaskesta, liiguvad mõnikord väikesed toiduosakesed vereringesse ja teistesse kehaosadesse, vallandades seeläbi organismis immuunvastuse, mis viib ka toiduallergiate tekkeni.
Paljud inimesed, kuuldes sageli bakteritest, kardavad koheselt teistelt patsientidelt nakatuda. Kuid õnneks pole see nakkav haigus. Ja see, et see on nii levinud, on tõenäoliselt tingitud asjaolust, et inimesed elavad sarnast elustiili ja vähesed inimesed söövad õigesti.
Kas on muid terviseprobleeme?
On tõendeid selle kohta, et SIBO-d seostatakse mitmesuguste muude haigusseisunditega, sealhulgas ärritunud soole sündroomi, põletikulise soolehaiguse, rosaatsea ja teistega.
Teadmata põhjustel on see hüpotüreoidismi, mittealkohoolse rasvmaksahaiguse ja tsirroosiga inimestel tavaline sümptom.
Pole juhus, et selle peamised sümptomid on lekkiva soole sündroomi puhul samad. Tegelikult on samu sümptomeid leitud enam kui 80% lekkiva soole sündroomiga patsientidest, mistõttu mõned teadlased oletavad, et see on viimase häire algpõhjus.
Veel pole teada, kui suur osa elanikkonnast kannatab bakterite ülekasvu all, kuid mõnedes uuringutes viitavad teadlased tõsiasjale, et nende arv ulatub lausa 20%-ni.
Seda haigust ei tohiks alahinnata, sest inimesed pöörduvad selliste sümptomitega harva arsti poole.
Kui SIBO-d ei ravita õigeaegselt, võib see aja jooksul põhjustada muid tüsistusi.
Bakterite kasv peensooles võib põhjustada alatoitlust, mis takistab paljude toitainete, valkude, süsivesikute ja rasvade õiget imendumist. Hiljem tekib raua, B12-vitamiini, kaltsiumi ja isegi rasvlahustuvate vitamiinide puudus: A-, D-, E- ja K-vitamiin.
Toitainete puudus põhjustab üldist nõrkust, väsimust, segasust ja kesknärvisüsteemi kahjustusi.
B12-vitamiini puudus on kõige levinum. Sellele on vastuvõtlikumad taimetoitlased ja veganid, samuti inimesed, kelle maohappe tootmine on ebapiisav või kes võtavad maohapet alla suruvaid ravimeid.
SIBO märgid
Peamised sümptomid hõlmavad järgmist:
-
Sage kõhuvalu;
Väsimus;
krambid;
Äkiline toidutalumatus (gluteen, laktoos või fruktoos);
Lekkiv soolestik;
-
kroonilised haigused (diabeet, autoimmuunhaigused);
Nahalööbed (rosaatsea, akne, ekseem, lööve);
Depressioon;
-
Alatoitumus ja seletamatu kaalulangus (väga äärmuslikel juhtudel).
Krooniline gaasilisus;
puhitus (eriti paar tundi pärast söömist);
Vitamiini või mineraalide puuduse nähud;
kõhukinnisus või kõhulahtisus;
Peamised riskitegurid
Bakterite kasvu peensooles soodustavad paljud seisundid. Nende hulka kuuluvad üldine vananemine, krooniline pankreatiit, diabeet, divertikuloos, peensoole struktuursed defektid, haavad, fistulid, soole lümfoom ja sklerodermia.
Maohape pärsib allaneelatud bakterite kasvu, piirates seeläbi bakterite arvu peensoole ülaosas. Maohappe tootmise vähenemine on SIBO oluline riskitegur ja võib tekkida pärast Helicobacter pylori koloniseerimist või vananemise tagajärjel.
Teatud ravimite kasutamine(immunosupressandid, prootonpumba inhibiitorid), immuunsüsteemi häired, hiljutine operatsioon ja tsöliaakia, Samuti seotud suurenenud riskiga SIBO tekkeks.
Tsöliaakia on eriti ohtlik, kuna see häirib soolemotoorikat, mis põhjustab peensoole ebaõiget toimimist.
Teine SIBO põhjus on pimeda silmuse sündroom.. See juhtub siis, kui peensool tegelikult moodustab silmuse, sundides toitu osast seedetraktist mööda minema. Toit liigub aeglasemalt, mistõttu see muutub bakterite kasvulavaks.
Ainevahetushäired, sealhulgas 2. tüüpi diabeet, põhjustavad samuti teatud seedetrakti häireid või soodustavad nende tekkimist.
Keha vananemine- eriline riskitegur SIBO tekkeks. Vananedes seedetrakt aeglustub.
Riskirühma kuuluvad ka need, kes kannatavad rosaatsea, akne ja ekseemi all. Nagu näete, on bakterite ülekasv õhukeses seotud paljude tingimustega.
Kuidas SIBO diagnoosida?
Selle seisundi keerukuse tõttu ei sobi ükski test selle diagnoosimiseks kindlasti. Peensool raskendab juurdepääsu, seega on standardsed väljaheiteproovid käärsoole, kuid mitte peensoole tervise parim näitaja.
Standardne test SIBO määramiseks on vesiniku hingamistest. See mõõdab seedesüsteemis bakterite poolt toodetud vesiniku ja metaani kogust.
Kui teil on SIBO, võib neid gaase teatud kontsentratsioonides tuvastada väljahingatavas õhus paar tundi pärast tavalise suhkrulahuse joomist.
Sarnane test laktuloosi kasutamisega. Bakterid võivad laktuloosi seedida ja kui nad seda teevad, tekivad gaasid. Kui laktuloosi hingamistest näitab gaasi, on teil tõenäoliselt bakterite ülekasv.
Hingamistestid pole kaugeltki täiuslikud, sest need võimaldavad tõlgendamist. Kõigil arstidel on erinev kogemus, nad saavad diagnoosida tulemusi positiivseteks või negatiivseteks, sest SIBO sümptomid langevad sageli erinevate haiguste spektritesse.
Sel põhjusel on tavaliselt kõige parem teha mitu testi korraga, et saada selgem pilt sisemisest bakterite tasemest.
Kuidas SIBO-ga toime tulla?
Kui olete leidnud peensooles bakterite liigset kasvu, siis ärge sattuge paanikasse. Võimalik on taastada bakterite tasakaal ja leevendada sümptomeid.
1) Pidage kinni dieedist
Üks peamisi tegureid, mis provotseerib bakterite kasvu, on alatoitumus, täidetud kergesti seeditava toiduga. Nende hulka kuuluvad lihtsad suhkrud, rafineeritud süsivesikud ja kõik alkoholitüübid.
Dieedi esimene punkt on loobuda toiduainetest, mis neid baktereid toidavad. Dieedi eesmärk on toita teid, kuid jätta bakterid nälga, tavaliselt piirates süsivesikuid ja täites kõhtu lahustumatute kiudainetega.
Toidud, mida vältida:
-
Värsked puuviljad;
tuunikala ja lõhe;
Veise- ja lambaliha;
-
kõvad toorjuustud;
Mandli- või kookospiim;
Värsked marjad (mustikad, maasikad, sõstrad);
Pähkliõlid.
Fruktoos – mõned puuviljamahlad, mesi, töödeldud terad, küpsetised, maisi- ja vahtrasiirupid, töödeldud suhkrud.
Laktoos – tavalised piimatooted ja töödeldud toidud piima ja laktoosilisanditega, näiteks piimapulber.
Fruktaanid - spargel, sibul, artišokk, nisupuder, küüslauk, spargelkapsas, lehtkapsas.
Galaktaanid – kaunviljad, kapsas, rooskapsas, sojaoad.
Polüoolid (väga suurte molekulidega süsivesikud) - sorbitool, isomalt, laktitool, maltitool. Neid leidub närimiskummides, kõvades kommides ja mõnedes ravimites.
Toidud, mida saate süüa:
Köögiviljad (rohelised, kurgid, porgandid, squash, tomatid);
Kõrge kiudainesisalduse tõttu ei lähe värsked puuviljad maos käärima. enne seedimise algust.
Ärge üle sööge, sest liigne toit piirab happe tootmist maos ning loob seetõttu peensooles sobiva keskkonna bakterite paljunemiseks.
Samuti on mõistlik süüa väiksemaid eineid sagedamini kogu päeva jooksul kui kolm suurt einet. See aitab seedesüsteemil iga toidukorda tõhusamalt töödelda. Pärast seda kahenädalast toidukorda muutub toitumine veidi, et kogu seedetraktis bakterid uuesti tasakaalu viia ja toksiinide vereringesse sattumise vältimiseks.
Vältida tuleks kõiki teravilju, töödeldud suhkruid, kõrge tärklisesisaldusega toite, töödeldud toite ja mittemahepõllumajanduslikke liha-piimatooteid.
Järk-järgult tutvustage probiootikumirikkaid toite, kuid mitte poejogurtit, vaid omatehtud, kultiveeritud juurvilju, nattot, kombuchat ja fermenteeritud toite, näiteks hapukapsast.
2) Toidulisandid
SIBO põhjustab sageli toitainete puudujääke sest soolebakterid seedivad suure osa teie toidust.
Tarbi iga päev multivitamiini vitamiinide B12, D, K, tsingi ja rauaga kuni riik on taas kontrolli all.
Kõrge vitamiinitase aitab ka võidelda või vähendada SIBO väljakujunemise võimalusi.
3) antibiootikumid
Antibiootikumid on sageli SIBO põhjuseks, kuid need aitavad taastada ka normaalset bakterite taset. Antibiootikumid tapavad soovimatud bakterid, vähendades seeläbi nende arvu peensooles.
Antibiootikumid tapavad aga baktereid valimatult, seega väheneb ka kasulike bakterite arv, mille tulemuseks on kõrge kordumise määr.
4) Probiootikumid
Arstid määravad sageli probiootikume koos antibiootikumidega ja koos dieediga. kordumise määra vähendamiseks.
5) Taimsed ravimid
Paljud taimed omavad looduslikke antibakteriaalseid omadusi, nagu näiteks mugirohu ekstrakt, argaaniaõli, India lodjapuu juureekstrakt ja melissiõli. Need aitavad vähendada väikeste bakterite kasvu.
Mõned eeterlikud õlid võivad samuti parandada SIBO sümptomeid ja isegi haigusseisundi püsivalt likvideerida.
Piparmündi eeterlik õli vähendab seedetrakti valulikke sümptomeid, nagu kõhukinnisus ja kõhulahtisus, samuti nelgiõli, estragoni ja viiruki eeterlik õli.
Üks parimaid viise kogu oma seedesüsteemi parandamiseks on tervisliku eluviisi järgimine. Stressi kontroll, regulaarne treening ja meditatsioon võivad vähendada SIBO riski.avaldatud.
P.S. Ja pidage meeles, et lihtsalt oma tarbimist muutes muudame koos maailma! © econet
Tsiteerimiseks: Belousova E.A. Peensoole liigse bakteriaalse kasvu sündroom kroonilise pankreatiidi korral // eKr. 2009. nr 5. S. 317
Sissejuhatus Kroonilist pankreatiiti (CP) peetakse raskete sümptomite kompleksiga haiguseks, mille hulgas domineerivad valu ja ekskretoorne pankrease puudulikkus (EPI). Nende sündroomide tekkepõhjusteks on erineva raskusastmega pankrease kanalite krooniline obstruktsioon, mis takistab pankrease mahla voolu kaksteistsõrmiksoole. Paratamatult kaasneb EPI-ga seedimise ja toitainete omastamise halvenemine, mis võib viia malabsorptsiooni tekkeni. Arvatakse, et piisav ravi ensüümpreparaatidega peaks kompenseerima endogeensete ensüümide vaeguse ja taastama normaalse seedimise. Praktikas pole aga kaugeltki alati võimalik EPI-ga lihtsalt toime tulla. Selle peamine põhjus on reeglina seotud ensüümi ainete ebapiisava annuse või ebaefektiivse ravimi valikuga. EPI püsival kulgemisel ja ensüümravi esmapilgul madalal efektiivsusel on teine, väga tõsine põhjus. Seda seostatakse peensoole bakteriaalse ülekasvu sündroomi (SIBO) tekkega, mida ingliskeelses kirjanduses nimetatakse "bakteriaalseks ülekasvuks". SIBO on paljudele arstidele vähe tuntud ja seda ei võeta ravitaktikas arvesse. Seetõttu oli selle artikli eesmärk tutvustada sisearste ja gastroenterolooge kaasaegsete lähenemisviisidega SIBO korrigeerimiseks CP-s.
Kroonilist pankreatiiti (CP) peetakse raskete sümptomite kompleksiga haiguseks, mille hulgas domineerivad valu ja ekskretoorne pankrease puudulikkus (EPI). Nende sündroomide tekkepõhjusteks on erineva raskusastmega pankrease kanalite krooniline obstruktsioon, mis takistab pankrease mahla voolu kaksteistsõrmiksoole. Paratamatult kaasneb EPI-ga seedimise ja toitainete omastamise halvenemine, mis võib viia malabsorptsiooni tekkeni. Arvatakse, et piisav ravi ensüümpreparaatidega peaks kompenseerima endogeensete ensüümide vaeguse ja taastama normaalse seedimise. Praktikas pole aga kaugeltki alati võimalik EPI-ga lihtsalt toime tulla. Selle peamine põhjus on reeglina seotud ensüümi ainete ebapiisava annuse või ebaefektiivse ravimi valikuga. EPI püsival kulgemisel ja ensüümravi esmapilgul madalal efektiivsusel on teine, väga tõsine põhjus. Seda seostatakse peensoole bakteriaalse ülekasvu sündroomi (SIBO) tekkega, mida ingliskeelses kirjanduses nimetatakse "bakteriaalseks ülekasvuks". SIBO on paljudele arstidele vähe tuntud ja seda ei võeta ravitaktikas arvesse. Seetõttu oli selle artikli eesmärk tutvustada sisearste ja gastroenterolooge kaasaegsete lähenemisviisidega SIBO korrigeerimiseks CP-s.
Normaalne mikrofloora
seedetrakti
Kaasaegsetest positsioonidest vaadeldes peetakse inimese normaalset mikrofloorat (normofloora, mikrobioota) paljude mikrobiotsenooside kogumina, mis hõivavad arvukalt ökoloogilisi nišše (biotoope) kõigi väliskeskkonnale avatud kehaõõnsuste nahal ja limaskestadel. Bakterite koguarv täiskasvanul on 1015 rakku, mis on üle 10 korra suurem kui makroorganismi enda rakkude arv. Praegu kehtiv normatiivdokument "Venemaa düsbakterioosi tööstuse standard" pakub normofloora järgmist määratlust: see on "üksikute organite ja süsteemide erinevate mikroobide populatsioonide kvalitatiivne ja kvantitatiivne suhe, mis toetab makroorganismi biokeemilist, metaboolset ja immunoloogilist tasakaalu". inimeste tervise säilitamiseks. Sellest määratlusest järeldub, et iga biotoobi normofloora täidab arvukalt funktsioone mitte ainult selle toimimise, vaid ka kogu keha homöostaasi säilitamiseks.
Seedetrakti iga biotoobi (GIT) mikrofloora liigiline ja kvantitatiivne koostis on nii peremeesorganismi kui ka mikrobiota enda arvukate kaitsefaktorite mõju tõttu üsna konstantne:
. geneetiline eelsoodumus
. Happeline maokeskkond
. Seedetrakti normaalne motoorne evakueerimisfunktsioon
. Seedetrakti anatoomilised sulgurlihased
. Pidev intraluminaalse pH tase erinevates biotoopides
. Limaskestade immuunsüsteemi seisund
. Limaskestade poolt toodetud bakteritsiidsed ained (lüsosüüm, laktoferriin jne)
. Limaskesta makrofaagide fagotsüütiline aktiivsus
. Sekretoorne IgA
. Bakteriaalsed kolitsiinid ja mikrotsiinid (mikroobse päritoluga endogeensed peptiidantibiootikumid)
Ainuüksi inimese seedetraktis elab üle 400 bakteriliigi – 17 erineva perekonna esindajad. Inimese seedetrakt on ebaühtlaselt asustatud bakteritega, erinevate biotoopide mikrofloora koostis on toodud tabelis 1.
Nagu tabelist näha, on mikroobse saastumise suurim tihedus käärsooles ligikaudu 400 erineva liigiga. Käärsoole mikroobirakkude kogubiomass on ligikaudu 1,5 kg, mis vastab 1011-1012 CFU/g sisu kohta ja on ligikaudu 1/3 väljaheidete kuivkaalust. Just jämesool kannab nii suure saastatuse tõttu teiste biotoopidega võrreldes suurimat funktsionaalset koormust. Bakterite sisaldus soole ülaosas varieerub kitsas vahemikus 103-104 CFU/ml soolesisu kohta. Bakterite põhimass peensoole jäme- ja alumises osas on bakteroidid, eubakterid, bifidobakterid, peptostreptokokid, ruminokokid, klostriidid ja laktobatsillid ning peensoole ülemistes osades - bakterioidid, laktobatsillid ja kokid (Table).
Vaatamata suhteliselt väikesele mikroorganismide arvule proksimaalses peensooles, on nende funktsioonid väga olulised selle biotoobi elutegevuseks, eelkõige luminaalse pH ja limaskesta immuunstaatuse säilitamiseks. Seedetrakti normaalne mikrofloora tervikuna täidab metaboolseid, kaitsvaid, antimutageenseid ja kantserogeenseid funktsioone. Metaboolsed ja kantserogeensed funktsioonid langevad peamiselt käärsoole floorale ning kõigi biotoopide mikrofloora osaleb antitoksiliste, kaitse- ja immuunfunktsioonide elluviimises, kolonisatsiooniresistentsuse ja mikroobide antagonismi säilitamises patogeenide ja oportunistlike patogeenide suhtes. See kehtib ka peensoole ülemiste osade kohta.
Kolonisatsiooniresistentsuse all mõistetakse mehhanismide kogumit, mis tagavad teatud biotoobis mikroobipopulatsioonide liigilise püsivuse ja kvantitatiivse koostise, takistades oportunistliku ja patogeense taimestiku paljunemist ning selle translokatsiooni mitteiseloomulikesse biotoopidesse ja organismi sisekeskkonda. Sellise mikrofloora translokatsiooni ilming võib olla SIBO peensooles, kusjuures viimase mikroobne saastumine suureneb rohkem kui 104 CFU / ml soolesisu kohta.
Bakterite ülekasvu sündroom
saastumine - bakterite ülekasv)
Nagu eespool mainitud, kõigub soolestiku ülaosa bakterite normaalne sisaldus kitsas vahemikus 103-104 CFU / ml soolesisalduse kohta ja see väärtus on omamoodi konstant peensoole jaoks. Ka mikrobiota liigiline koosseis on üsna püsiv: bakteroidid, laktobatsillid, kokid.
Võttes kokku olemasolevad määratlused, saame meie vaatenurgast anda SIBO sündroomi järgmise definitsiooni: bakteriaalne ülekasvu sündroom on peensoole proksimaalsete osade külvamine üle 104 mc. (CFU) / ml soole sisu oportunistliku mikrofloora tõttu, mis pärineb seedetrakti ülaosast (või ülemistest hingamisteedest) või käärsoole mikrobiota oportunistlike esindajate retrograadse translokatsiooni tõttu.
Tuleb rõhutada, et SIBO mõiste viitab rahvusvahelises kirjanduses ainult peensoole taimestiku ülekasvule, kuid mitte jämesoole.
SIBO-le viivad mitu peamist mehhanismi. Esimene mehhanism on tingitud mis tahes päritolu hüpo- või akloorhüdriast. Kaitsva happebarjääri vähenemine võimaldab suuõõne ja ülemiste hingamisteede mikroobidel koloniseerida makku ja seejärel peensoole. See protsess võib põhineda erinevatel põhjustel, kuid enamasti toimub see peensoole mikroobse saastumise tee pärast maovähendusoperatsiooni või maovähendusoperatsiooni, maosekretsiooni inhibiitorite pikaajalisel kasutamisel, autoimmuunse gastriidi korral, autoimmuunhaigustega nagu pernicious aneemia ja sklerodermia. .
Teine SIBO arengu mehhanism on tingitud nn "soolestiku kliirensi" rikkumisest, st. peensoole võime rikkumine kõrvaldada sinna sattunud patogeensed või oportunistlikud mikroorganismid. Kliirensi halvenemine ilmneb peensoole mikrobiota püsivust säilitavate kaitsemehhanismide aktiivsuse vähenemisega: motoorse aktiivsuse pärssimine, bakteritsiidsete ainete ja sekretoorse IgA sünteesi vähenemine, makrofaagide fagotsüütilise funktsiooni vähenemine. peensoole limaskest jne.
Kolmas mehhanism on seotud mikrofloora retrograadse translokatsiooniga käärsoolest peensoolde, mis on tingitud ileotsekaalklapi puudulikkusest käärsoole põletiku või motoorsete häirete ajal. Peaaegu iga gastroenteroloogiline haigus võib põhjustada SIBO arengut (tabel 2).
SIBO hindamise meetodid
SIBO diagnoosimine on väga raske, kuna peensoole sisu proovide võtmise meetodid on liiga töömahukad. Selleks on välja töötatud lihtne ja mugav meetod vesiniku kontsentratsiooni määramiseks väljahingatavas õhus pärast süsivesikute koormust glükoosi või laktoosiga (vesinikhingamise test). SIBO juuresolekul on vesiniku tase väljahingatavas õhus kõrge, kuna peensooles tekivad mikroobsed metaboliidid. Sama meetodiga saab jälgida ravi tulemusi erinevate ravimitega, mis pärsivad peensoole liigse floora kasvu. Meetod on odav, seda on lihtne teostada, kuid kahjuks ei kasutata seda Venemaal laialdaselt.
Krooniline pankreatiit ja SIBO
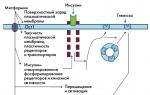
Vastavalt J.E. Dominguez-Munoz, SIBO esineb 40% CP-ga patsientidest ja see on üks levinumaid põhjuseid, mis põhjustab ensüümasendusravi ebapiisava efektiivsuse. Joonisel 1 on üksikasjalikult esitatud arvukad mehhanismid, mis põhjustavad seedimise ja SIBO halvenemist CP-s.
Seega on HP-ga kaasas:
. seedimise ja imendumise protsesside rikkumine
. bakterite ülekasv peensooles
. seedetrakti motoorse funktsiooni rikkumine
Esmane õõnes seedimise rikkumine CP-s keeruliste mehhanismide koostoime kaudu süveneb membraanide seedimise rikkumisega ja kõik osalevad mehhanismid töötavad nõiaringi põhimõttel.
Ülekaalulise sündroomi ravi
bakterite kasvu
Tuleb meeles pidada, et SIBO ei ole iseseisev patoloogia, vaid ainult sekundaarne sündroom, mis kaasneb paljude patoloogiliste seisunditega. Kui reeglina ei esine käärsoole mikrobiota rikkumiste puhul selgelt määratletud kliinilisi sümptomeid, siis SIBO korral tekivad tavaliselt kõhupuhitus, väljaheitehäired ja mõnikord ka tõsine kõhulahtisus. Samas ei ole kõik need sümptomid spetsiifilised ning neid ei ole võimalik üheselt SIBO-ga seostada. Selle artikli kontekstis võivad kõhupuhitus, kõhulahtisus, stetorröa olla võrdselt nii EPI kui ka SIBO tagajärg.
Mikroobsed häired nii jäme- kui peensooles on igal juhul alati teisejärgulised, mistõttu on nende korrigeerimiseks vaja ennekõike kõrvaldada neid põhjustavad negatiivsed tegurid (näiteks meditsiinilised või keskkonnamõjud) või ravida põhihaigust. Oluline on rõhutada, et SIBO korrigeerimine ei ole eesmärk omaette ja see viiakse läbi:
. kui selle põhjust ei ole võimalik kõrvaldada
. pideva agressiivse teguri toimel (näiteks keemiaravi)
. lisameetmena, kui neid häireid põhjustanud põhihaiguse ravi ei ole piisavalt tõhus.
Nende sätete ideaalne näide on EPI taustal arenev SIBO. Ideaaljuhul taastub seedimine, kui määratakse piisav annus ensüümipreparaate ja SIBO täiendav korrigeerimine pole vajalik. SIBO on aga üks levinumaid põhjuseid, mis põhjustab ensüümasendusravi ebapiisava efektiivsuse. Ühes uuringus hinnati Creon-ravi mõju SIBO-le (vesinikhingamise testi järgi) 15 patsiendil, kellel oli CP-s EPI. Need patsiendid 2 kuu jooksul. läbiviidud ravi Creoniga 100-150 tuhat RÜ päevas. Enamikul (65% - 10 patsienti) korduva vesiniku testi järgi SIBO elimineeriti, 53% (8 patsienti) kõhupuhitus kadus, 73% (11 patsienti) oli enesetunne paranenud, kuid düspeptiline. sümptomid püsisid.
Eelneva põhjal peaks EPI-ga koos SIBO-ga või ilma pankreasehaiguste esmavaliku raviks piisavate annuste manustamine efektiivsete ensüümi ainete (Creon 25000-40000 RÜ iga toidukorra ajal) manustamine. Selle ebapiisava efektiivsusega on näidustatud ravimite määramine peensoole mikroobide kasvu kõrvaldamiseks.
Mikroobsete häirete terapeutiline taktika sõltub nende raskusastmest, kliiniliste ilmingute olemasolust ja bakterite ümberpaigutusest teistesse biotoopidesse. Mõnel juhul on SIBO juuresolekul vaja läbi viia "soolestiku selektiivne mikroobne puhastamine". See kontseptsioon hõlmab soolestiku puhastamist (saastusest puhastamist) ravimitega, mis pärsivad selektiivselt võõrfloora kasvu ega mõjuta normofloorat. Desinfitseerimiseks kasutatakse mitut ainete rühma:
. antibakteriaalsed ravimid
. mittepatogeensed seened
. eoseid moodustavad preparaadid, mis põhinevad mööduva taimestiku esindajatel
. mikroobsed metaboliidid.
Antibiootikumid
Optimaalne antibakteriaalne ravim peensoole puhastamiseks ja SIBO eemaldamiseks peab vastama järgmistele nõuetele:
. neil on soolestikust minimaalne imendumine
. luua sooleõõnes kõrge kontsentratsioon
. neil on selektiivsus (peaks pärssima võõrfloorat ega mõjuta normofloorat
. neil on lai antimikroobse toime spekter, sealhulgas aeroobid ja anaeroobid
. neil on minimaalselt kõrvaltoimeid ja see on ohutu
. on tõestanud kliinilist efektiivsust
Üks uusimaid Venemaal ja kõigist kolmest vaatenurgast kõige huvitavam ravim on rifamütsiini derivaat - ravim rifaksimiin (Alfa-normix). See ei ole imenduv<1%) при приеме внутрь антибиотик, достигающий высоких концентраций в слизистой оболочке ЖКТ. Препарат не действует вне ЖКТ, т.е. является местнодействующим кишечным антисептиком. Рифа-кси-мин хорошо переносится, имеет минимум побочных эф-фек-тов и не вызывает бактериальной резистентности. Препарат имеет широкий спектр антибактериального действия против грамположительных (Enterococcus spp, M. tuberculosis, Streptococcus pyogenes, Streptococcus faecalis, Streptococcus pneumoniae, Staphylococcus epidermidis, Staphylococcus aureus) и грамотрицательных (Escheri-chia coli, Shigella spp, Salmonella spp, Yersinia enterocolica, Proteus spp, Vibrio cholerae) аэробных бактерий и грампо-ло-жительных (Clostridium perfrigens, Clostridium difficile, Peptococcus spp, Peptostreptococcus spp) и грамот-ри-цательных (Bacteroides spp, Bacteroides fragilis, Helico-bacter pylori) анаэробов . Такой спектр действия определяет те-ра-певтические возможности препарата. Таким образом, ри-фак-симин удовлетворяет всем основ-ным требованиям, предъявляемым к идеальному антибактериальному препарату. Он с успехом используется при острых кишечных инфекциях, для санации толстой кишки при «дисбактериозе», для коррекции СИБР, при антибиотико-ассо-ции-ро-ванных поражениях кишечника и при печеночной энцефалопатии. При СИБР, доказанном с помощью водородного дыхательного теста, рифаксимин применяется по 400 мг 3 раза в сутки в течение 7 дней. При этом уровень выдыхаемого водорода снижается в 3-5 раз уже к третьему дню лечения, что свидетельствует о быстрой санации тонкой кишки .
Pikka aega on SIBO raviks erinevate patoloogiate korral kasutatud erinevaid antibiootikume (tetratsükliinid, linkomütsiin, ampitsilliin jt), mis ei ole selektiivsed, ei mõjuta anaeroobset floorat, imenduvad kiiresti seedetraktist ja millel on laia valikut kõrvaltoimeid (sealhulgas antibiootikumid). -seotud kõhulahtisus) ja pärsivad normaalset taimestikku. Rifaksimiini efektiivsuse demonstreerimiseks viidi läbi topeltpime uuring, mis kinnitas rifaksimiini prioriteetsust tetratsükliini ees SIBO-s. Selles uuringus hinnati SIBO-d kahes patsientide rühmas vesiniku hingamistesti abil ning määrati vesiniku eritumise tipp väljahingatavas õhus ning vesiniku kogukontsentratsioon pärast glükoosikoormust enne ja 3 päeva pärast antibiootikumikuuri lõppu. Näidati, et vesiniku võrdse algtaseme korral oli selle tipp pärast glükoosi laadimist, samuti kogukontsentratsioon väljahingatavas õhus pärast ravi, oluliselt madalam rifaksimiiniga ravitud patsientidel võrreldes kloortetratsükliiniga ravitud rühmaga.
Teiste tõhusate antibakteriaalsete ainete hulka kuuluvad oksükinolooni derivaadid, väheimenduvad nitrofuraani derivaadid (nifuroksasiid) ja nitroimidasoolid (metronidasool, tinidasool). Kuigi viimane rühm imendub jämesoolest, on selle kasutamine siiski tõhus, peamiselt anaeroobsete mikroorganismidega saastumise korral. SIBO dekontaminatsioonikuuri kestus on 12-14 päeva.
Mittepatogeensed seened
Antibakteriaalsete ravimite talumatuse korral on võimalik ja efektiivne määrata ravimeid, mis põhinevad perekonna S. boulardii mittepatogeensetel pärmseentel. Samas ei inhibeeri S. boulardii kohustuslike mikroorganismide kasvu sooleõõnes ja on resistentne soolhappe toimele. Igapäevase tarbimise korral leidub neid seedetrakti kõikides osades, sealhulgas peensooles. Need pärmseened on inimese jaoks mööduv taimestik, mistõttu 2-5 päeva pärast ravimi võtmise lõppu elimineeritakse need organismist täielikult ilma kõrvaltoimeteta. Ravim ei imendu seedetrakti luumenist ja on lokaalselt toimiv soole antiseptik. S. boulardii antimikroobne toime määrati kindlaks in vitro ja in vivo sooleinfektsioonide patogeenide (Cl. difficile, Salmonella, Shigella, Yersinnia), algloomade (Giardia ja mitmed) oportunistlike mikroorganismide (patogeensed kokid, seened, Klebsiela jne) vastu. .), mis võib viia SIBO arenguni.
Eoseid moodustavaid mittepatogeenseid antibakteriaalseid aineid saab SIBO-s kasutada ka talumatuse korral alternatiivina antibiootikumidele. Sellesse rühma kuuluvad ravimid, mis põhinevad heinabacillil Bacillus subtilis ja sarnasel mikroorganismil B. cereus. Eosmikroorganismid on inimese jaoks mööduv taimestik, seetõttu eemaldatakse need pärast tarbimise lõpetamist kiiresti soolestikust. Nende ravimite toimemehhanism on tingitud happeliste metaboliitide moodustumisest eluprotsessis ja pH langusest kogu soolestikus, mille tõttu pärsitakse oportunistliku floora kasvu. Lisaks sünteesivad need ained mitmeid seedeensüüme, kompenseerides osaliselt soolestiku enda ensümaatilise aktiivsuse vähenemist, kui seda kahjustavad bakterid ja nende toksiinid. SIBO ravikuur on 10-14 päeva. Pikem kursus on ebasoovitav, sest. B. cereus on võimeline tootma enterotoksiine, mis põhjustavad kõhulahtisust.
Mikroobsed metaboliidid
Täiendav aine, mis taastab valdavalt peensoole mikrofloora, on mikroobne metaboliit hilak forte. Peamised bioloogiliselt aktiivsed komponendid, millest hilak forte koosneb, on lühikese ahelaga rasvhapped (SCFA) ja piimhape, mis on saadud normaalse soole mikrofloora sahharolüütilistest ja proteolüütilistest esindajatest. Bioloogiliselt aktiivsete ainete kontsentratsioon ühes ravimi tilgas vastab 1010 bakteri vastavate metaboliitide toimele. Hilak forte toimemehhanismi mikrobiota koostise ja funktsioonide normaliseerimisel ning soolestiku aktiivsuse taastamisel vahendavad selle koostiskomponendid. Preparaadis sisalduvad SCFA-d annavad limaskestadele lisaenergiat, soodustavad kahjustatud sooleseina epiteelirakkude taastumist ja parandavad limaskesta trofismi. Happeliste metaboliitide (SCFA, piimhape) mõju tagab intraluminaalse pH reguleerimise, mis põhjustab patogeenide ja oportunistlike patogeenide kasvu pärssimist kogu soolestikus.
Seega tuleks CP SIBO-ga ravimise taktika üles ehitada järgmiselt:
. piisav ensüümravi (Creon 75 000 RÜ või rohkem päevas)
. peensoole saastest puhastamine: antibiootikumravi (rifaksimiin)
. mikroobsed metaboliidid
. käärsoole mikrobiotsenoosi normaliseerimine pro- ja prebiootikumidega (vajadusel)
. motoorsete häirete kõrvaldamine - kaksteistsõrmiksoole hüpertensioon, kiirendatud tõukejõud (vajadusel).


Kirjandus
1. Ardatskaja M.D., Minushkin O.N., Ikonnikov N.S. "Soolestiku düsbakterioos": kontseptsioon, diagnostilised lähenemisviisid ja korrigeerimisviisid. Väljaheidete biokeemilise uuringu võimalused ja eelised. - Juhend arstidele. - M., 2004.
2. Belousova E.A. Peensoole bakterite liigse kasvu sündroom soole düsbakterioosi üldkontseptsiooni valguses. Pilk probleemile. //Farmateka, 2009, nr 2 lk.
3. Bondarenko V.M. Oportunistlike soolebakterite roll inimese mitme organi patoloogias. M.: Triada, 2007.
4. Bondarenko V.M., Gratševa N.M., Matsulevitš T.V. Soole düsbakterioos täiskasvanutel.- M. KMK Scientific Press.-2003.-224 lk.
5. Shenderov B.A. Meditsiiniline mikroobne ökoloogia ja funktsionaalne toitumine. 3 köites. Moskva: Grant, 1998.
6. Korovina N.A., Zakharova I.N., Kostadinova V.N. Prebiootikumid ja probiootikumid soolestiku mikrobiotsenoosi häirete korral lastel. Juhend arstidele. Medpraktika - M., 2004.
7. Doronin A.F., Shenderov B.A. Funktsionaalne toit. - M.: Grant, 2002. - 296 lk.
8. Soolestiku mikrofloora. Seedetrakti füsioloogia ja patoloogia. Ed. J-C. Rambaud, J.P. Agas jt. JL Eurontext. Pariis. 2006.
9. Parfenov A.I. Enteroloogia. - M.: Triada, 2002.
10. Lähenemine krooniliste seedetrakti häiretega patsientidele. Ed. E. Corazziari. MESSAGGI. 2000.
11. Dominguez-Munoz J.E. Pankrease ensüümravi pankrease eksokriinse puudulikkuse korral. Curr. Gastroenterol Rep. 2007, 9(2): 116-122.
12. Pap A. et al. Creon-ravi mõju SIBO-le RVF-ga patsientidel. Kokkuvõtted 35. Euroopa Pankreaseklubi koosolekust. Pankreatoloogia, 2003; 3:240.
13. Rifaksimiin: halvasti imenduv antibiootikum. Ed. C. scarpingato. Karger.2005.
14. Di Stefano M., Сorazza G.R. Peensoole bakterite vohamise ja sellega seotud sümptomite ravi rifaksimiiniga. In: Rifaksimiin: halvasti imenduv antibiootikum. Ed. C. scarpingato. Karger. 2005.
15. Di Stefano M., Malservisi S., Veneto G., Сorazza G.R. Rifaksimiin versus kloortetratsükliin peensoole bakterite ülekasvu lühiajalises ravis. Aliment Pharmacol Ther 2000; 14:551-556.
16. Belousova E.A. Saccharomyces boulardii (Enterol) gastroenteroloogilises praktikas (kirjanduse ülevaade). //Farmateka, 2006, nr 12. lk.68-72.
17. Belousova E.A., Nikitina N.V., Mishurovskaya T.S., Zlatkina A.R. Mikroobsetel metaboliitidel põhinevate ravimite võimalused soolestiku mikrobiota taastamiseks //Consilium, 2005, nr 1, lk. 9-13.