Бактериофаги: современные аспекты применения, перспективы на будущее. Применение фагов в медицине и микробиологии
|
Валентин Викторович Власов — академик РАН, доктор химических наук, профессор, директор Института химической биологии и фундаментальной медицины СО РАН (Новосибирск). Лауреат Государственной премии РФ (1999). Автор и соавтор более 300 научных работ и 20 патентов. |
|
Вера Витальевна Морозова — кандидат биологических наук, старший научный сотрудник лаборатории молекулярной микробиологии Института химической биологии и фундаментальной медицины СО РАН (Новосибирск). Автор более 30 научных работ и 6 патентов. |
|
Игорь Викторович Бабкин — кандидат биологических наук, ведущий научный сотрудник лаборатории молекулярной микробиологии Института химической биологии и фундаментальной медицины СО РАН (Новосибирск). Автор и соавтор 58 научных работ и 2 патентов. |
|
Нина Викторовна Тикунова — доктор биологических наук, заведующая лабораторией молекулярной микробиологии Института химической биологии и фундаментальной медицины СО РАН (Новосибирск). Автор и соавтор 120 научных работ и 21 патента. |
В середине прошлого века биологическая наука сделала революционный шаг вперед, установив молекулярные основы функционирования живых систем. Огромную роль в успешных исследованиях, которые привели к определению химической природы наследственных молекул, расшифровке генетического кода и созданию технологий манипуляций генами, сыграли бактериофаги, открытые еще в начале прошлого столетия. На сегодняшний день эти бактериальные вирусы освоили много полезных для человека «профессий»: их используют не только как безопасные антибактериальные препараты, но и как дезинфектанты и даже в качестве основы для создания электронных наноустройств.
Когда в 1930-х гг. группа ученых занялась проблемами функционирования живых систем, то в поиске простейших моделей они обратили внимание на бактериофаги - вирусы бактерий. Ведь среди биологических объектов нет ничего проще, чем бактериофаги, к тому же их можно легко и быстро выращивать и анализировать, а вирусные генетические программы невелики.
Фаг - это минимального размера природная структура , содержащая плотно упакованную генетическую программу (ДНК или РНК), в которой нет ничего лишнего. Эта программа заключена в белковую оболочку, снабженную минимальным набором устройств для ее доставки внутрь бактериальной клетки. Бактериофаги не могут размножаться сами по себе, и в этом смысле их нельзя считать полноценными живыми объектами. Их гены начинают работать только в бактерии, используя имеющиеся в бактериальной клетке биосинтетические системы и запасы молекул, необходимых для синтеза. Однако генетические программы этих вирусов принципиально не отличаются от программ более сложных организмов, поэтому эксперименты с бактериофагами позволили установить основополагающие принципы устройства и работы генома.
В дальнейшем эти знания и разработанные в ходе исследований методы стали фундаментом для развития биологической и медицинской науки, а также широкого спектра биотехнологических приложений.
Борцы с патогенами
Первые попытки использовать бактериофаги для лечения инфекционных заболеваний были предприняты практически сразу после их открытия, однако недостаток знаний и несовершенные биотехнологии того времени не позволили достичь полного успеха. Тем не менее дальнейшая клиническая практика показала принципиальную возможность успешного применения бактериофагов при инфекционных заболеваниях желудочно-кишечного тракта, мочеполовой системы, при острых гнойно-септических состояниях больных, для лечения хирургических инфекций и т. д.
По сравнению с антибиотиками бактериофаги имеют ряд преимуществ : они не вызывают побочных эффектов, к тому же строго специфичны для определенных видов бактерий, поэтому при их использовании не нарушается нормальный микробиом человека. Однако такая высокая избирательность создает и проблемы: чтобы успешно лечить пациента, нужно точно знать инфекционный агент и подбирать бактериофаг индивидуально.
Фаги можно использовать и профилактически. Так, Московский научно-исследовательский институт эпидемиологии и микробиологии им. Г. Н. Габричевского разработал профилактический продукт «ФУДФАГ» на основе коктейля из бактериофагов, снижающий риск заражения острыми кишечными инфекциями. Клинические исследования показали, что недельный прием препарата позволяет избавиться от гемолизирующей кишечной палочки и других патогенных и условно-патогенных бактерий, вызывающих дисбактериоз кишечника.
Бактериофагами лечат инфекционные болезни не только людей, но и домашних и сельскохозяйственных животных: мастит у коров, колибактериоз и эшерихиоз у телят и свиней, сальмонеллез у кур... Особенно удобно применять фаговые препараты в случае аквакультуры - для лечения промышленно выращиваемых рыб и креветок, так как в воде они долго сохраняются. Бактериофаги помогают защитить и растения , хотя применение фаговых технологий в этом случае затруднено из-за воздействия природных факторов, таких как солнечный свет и дождь, губительных для вирусов.
Фаги могут сыграть большую роль в поддержании микробиологической безопасности продуктов питания, так как применение антибиотиков и химических агентов в пищевой отрасли не решает эту проблему, одновременно снижая уровень экологической чистоты продукции. О серьезности самой проблемы говорят статистические данные: например, в США и России ежегодно регистрируется до 40 тыс. заболевших сальмонеллезом, из которых 1% умирает. Распространение этой инфекции в значительной степени связано с выращиванием, переработкой и потреблением различных видов птицы, и попытки применить для борьбы с ней бактериофаги дали многообещающие результаты.
Так, американская компания Intralytix производит фаговые препараты для борьбы с листериозом, сальмонеллезом и бактериальным загрязнением кишечной палочкой. Они разрешены к применению как добавки, предотвращающие размножение бактерий на продуктах питания - их распыляют на продукты из мяса и домашней птицы, а также на овощи и фрукты. Эксперименты показали, что коктейль из бактериофагов может быть успешно применен и при транспортировке и реализации живой прудовой рыбы для снижения бактериального загрязнения не только воды, но и самой рыбы.
Очевидным применением бактериофагов является дезинфекция , то есть уничтожение бактерий в тех местах, где их не должно быть: в больницах, на пищевых производствах и т. п. Для этой цели британская компания Fixed-Phage разработала метод фиксации фаговых препаратов на поверхностях, обеспечивающий сохранение биологической активности фагов до трех лет.
Бактериофаги - «дрозофилы» молекулярной биологии
В 1946 г. на 11-м симпозиуме в знаменитой американской лаборатории в Колд Спринг Харборе, была провозглашена теория «один ген - один фермент». Бактериолог А. Херши и «бывший» физик, молекулярный биолог М. Дельбрюк доложили об обмене генетическими признаками между различными фагами при одновременном заражении ими клеток кишечной палочки. Это открытие, сделанное в то время, когда физический носитель гена еще не был известен, свидетельствовало, что явление «рекомбинации» - перемешивания генетических признаков, свойственно не только высшим организмам, но и вирусам. Обнаружение этого феномена в дальнейшем дало возможность детально исследовать молекулярные механизмы репликации. Позднее эксперименты с бактериофагами позволили установить принципы устройства и работы генетических программ.
В 1952 г. А. Херши и М. Чейз экспериментально доказали, что наследственная информация бактериофага Т2 закодирована не в белках, как считали многие ученые, а в молекулах ДНК (Hershey & Chase, 1952). Исследователи проследили за процессом воспроизводства в двух группах бактериофагов, одна из которых несла меченные радиоактивной меткой белки, а другая - молекулы ДНК. После инфицирования бактерий такими фагами оказалось, что в зараженную клетку передается только вирусная ДНК, что и послужило доказательством ее роли в хранении и передаче наследственной информации.
В том же году американские генетики Д. Ледерберг и Н. Циндлер в эксперименте с участием двух штаммов сальмонелл и бактериофага Р22 установили, что бактериофаг способен в процессе размножения включать в себя фрагменты ДНК бактерии-хозяина и передавать их другим бактериям при заражении (Zinder & Lederberg, 1952). Это явление переноса генов от бактерии-донора к реципиенту было названо «трансдукцией». Результаты эксперимента стали очередным подтверждением роли ДНК в передаче наследственной информации.
В 1969 г. А. Херши, М. Дельбрюк и их коллега С. Луриа стали Нобелевскими лауреатами «за открытия, касающиеся механизма репликации и генетической структуры вирусов».
В 1972 г. Р. Берд с коллегами при изучении процесса репликации (копировании клеточной информации) ДНК кишечной палочки использовали бактериофаги в качестве зондов, способных встраиваться в геном бактериальной клетки, и обнаружили, что процесс репликации идет в двух направлениях вдоль хромосомы (Стент, 1974).
Семь дней творения
Современные методы синтетической биологии позволяют не только вносить различные модификации в фаговые геномы, но и создавать полностью искусственные активные фаги. Технологически это несложно, нужно только синтезировать фаговый геном и ввести его в бактериальную клетку, а там он уже сам запустит все процессы, необходимые для синтеза белков и сборки новых фаговых частиц. В современных лабораториях на эту работу уйдет всего несколько дней.
Генетические модификации применяют, чтобы изменить специфичность фагов и повысить эффективность их терапевтического действия. Для этого наиболее агрессивные фаги снабжают узнающими структурами, связывающими их с целевыми бактериями. Также в вирусные геномы дополнительно встраивают гены, кодирующие токсические для бактерий белки, нарушающие метаболизм, - такие фаги более смертоносны для бактерий.
Бактерии имеют несколько механизмов защиты от антибиотиков и бактериофагов , один из которых - разрушение вирусных геномов ферментами рестрикции , действующими на определенные нуклеотидные последовательности. Для увеличения терапевтической активности фагов можно за счет вырожденности генетического кода так «переформатировать» последовательности их генов, чтобы минимизировать число нуклеотидных последовательностей, «чувствительных» к ферментам, одновременно сохранив их кодирующие свойства.
Универсальный способ защиты бактерий от всех внешних воздействий - так называемые биофильмы , пленки из ДНК, полисахаридов и белков, которые бактерии создают совместными усилиями и куда не проникают ни антибиотики, ни терапевтические белки. Такие биопленки - головная боль врачей, так как они способствуют разрушению зубной эмали, образуются на поверхности имплантов, катетеров, искусственных суставов, а также в дыхательных путях, на поверхности кожи и т. п. Для борьбы с биофильмами были сконструированы особые бактериофаги, содержащие ген, кодирующий специальный литический фермент, разрушающий бактериальные полимеры.
Ферменты «от бактериофага»
Большое число ферментов, сегодня широко использующихся в молекулярной биологии и генетической инженерии, были открыты в результате исследований бактериофагов.
Одним из таких примеров являются ферменты рестриктазы - группа бактериальных нуклеаз, расщепляющих ДНК. Еще в начале 1950-х гг. было обнаружено, что бактериофаги, выделенные из клеток одного штамма бактерий, зачастую плохо размножаются в близкородственном штамме. Обнаружение этого феномена означало, что у бактерий есть система подавления размножения вирусов (Luria & Human, 1952). В результате была открыта ферментативная система рестрикции-модификации, с помощью которой бактерии разрушали попавшую в клетку чужеродную ДНК. Выделение рестриктаз (эндонуклеаз рестрикции) дало в руки молекулярных биологов бесценный инструмент, позволивший манипулировать ДНК: встраивать одни последовательности в другие или вырезать необходимые фрагменты цепи, что в итоге привело к разработке технологии создания рекомбинантной ДНК.
Еще один широко используемый в молекулярной биологии фермент - ДНК-лигаза бактериофага Т4, которая «сшивает» «липкие» и «тупые» концы двуцепочечных молекул ДНК и РНК. А недавно появились генно-модифицированные варианты этого фермента с большей активностью.
От бактериофагов ведут свое происхождение и большинство используемых в лабораторной практике РНК-лигаз, которые «сшивают» одноцепочечные молекулы РНК и ДНК. В природе они в основном служат для починки сломанных молекул РНК. Исследователи наиболее часто используют РНК-лигазу бактериофага Т4, с помощью которой можно «пришить» одноцепочечные полинуклеотиды к РНК-молекулам, чтобы пометить их. Такой прием применяется для анализа структуры РНК, поиска мест связывания РНК с белками, олигонуклеотидного синтеза и т. д. Недавно среди рутинно используемых ферментов появились термостабильные РНК-лигазы, выделенные из бактериофагов rm378 и TS2126 (Nordberg Karlsson, et al., 2010; Hjorleifsdottir, 2014).
Из бактериофагов получены и некоторые из еще одной группы чрезвычайно важных ферментов - полимераз. Например, очень «точная» ДНК-полимераза бактериофага Т7, которая нашла применение в различных областях молекулярной биологии, таких как сайт-направленный мутагенез, но в основном ее используют для определения первичной структуры ДНК.
Химически модифицированная ДНК-полимераза фага Т7 была предложена как идеальный инструмент для секвенирования ДНК еще в 1987 г. (Tabor & Richardson, 1987). Модификация этой полимеразы увеличила эффективность ее работы в несколько раз: скорость полимеризации ДНК при этом достигает более 300 нуклеотидов в секунду, поэтому ее можно использовать для амплификации больших фрагментов ДНК. Этот фермент стал предшественником секвеназы - генно-инженерного фермента, оптимизированного для секвенирования ДНК в реакции Сэнгера. Секвеназа отличается высокой эффективностью и способностью включать в последовательность ДНК нуклеотидные аналоги, используемые для улучшения результатов секвенирования.
Происхождение от бактериофагов ведут и используемые в молекулярной биологии основные РНК-полимеразы (ДНК-зависимые РНК-полимеразы) - ферменты, которые катализируют процесс транскрипции (считывание РНК-копий с матрицы ДНК). К ним относятся SP6-, T7- и Т3-РНК-полимеразы, названные в честь соответствующих бактериофагов SP6, Т7 и Т3. Все эти ферменты используются для синтеза «в пробирке» антисмысловых РНК-транскриптов, меченых РНК-зондов и т. д.
Первым полностью секвенированным ДНК-геномом стал геном фага φ174 длиной свыше 5 тыс. нуклеотидов (Sanger et al., 1977). Эту расшифровку осуществила группа английского биохимика Ф. Сэнгера, создателя известного одноименного метода секвенирования ДНК.
Полинуклеотидкиназы катализируют перенос фосфатной группы от молекулы АТФ к 5′-концу молекулы нуклеиновой кислоты, обмен 5′-фосфатных групп или фосфорилирование 3′-концов мононуклеотидов. В лабораторной практике наибольшее распространение получила полинуклеотидкиназа бактериофага Т4. Она обычно используется в экспериментах для мечения ДНК радиоактивным изотопом фосфора. Полинуклеотидкиназа также используется для поиска сайтов рестрикции, ДНК и РНК дактилоскопии, синтеза субстратов для ДНК или РНК-лигаз.
В молекулярно-биологических экспериментах также находят широкое применение такие ферменты бактериофагов, как полинуклеотидкиназа фага Т4, обычно используемая для мечения ДНК радиоактивным изотопом фосфора, ДНК и РНК дактилоскопии и др., а также ферменты, расщепляющие ДНК, которые используются для получения одноцепочечных ДНК-матриц для секвенирования и анализа нуклеотидного полиморфизма.
Методами синтетической биологии удалось разработать и бактериофаги, вооруженные самым изощренным оружием, которое бактерии используют против самих фагов. Речь идет о бактериальных системах CRISPR-Cas , представляющих собой комплекс фермента нуклеазы, расщепляющей ДНК, и РНК-последовательности, направляющей действие этого фермента на определенный фрагмент вирусного генома. В качестве «указателя» служит кусочек фаговой ДНК, который бактерия сохраняет «на память» в специальном гене. При обнаружении внутри бактерии аналогичного фрагмента этот белково-нуклеотидный комплекс разрушает его.
Разобравшись с механизмом работы систем CRISPR-Cas, исследователи попробовали снабдить подобным «оружием» и самих фагов, для чего в их геном ввели комплекс генов, кодирующий нуклеазу и адресующие последовательности РНК, комплементарные специфическим участкам генома бактерий. «Мишенью» могут выступать гены, ответственные за множественную лекарственную устойчивость. Эксперименты увенчались полным успехом - такие фаги с большой эффективностью поражали бактерии, на которые были «настроены».
Фаговые антибиотики
В терапевтических целях фаги необязательно использовать напрямую. За миллионы лет эволюции бактериофаги разработали арсенал специфических белков - инструментов для распознавания целевых микроорганизмов и манипуляций с биополимерами жертвы, на основе которых можно создавать противобактериальные препараты. Наиболее перспективными белками такого типа являются ферменты эндолизины, которые фаги используют для разрушения клеточной стенки при выходе из бактерии. Сами по себе эти вещества являются мощными антибактериальными средствами, нетоксичными для человека. Эффективность и направленность их действия можно повысить, изменив в них адресующие структуры - белки, специфически связывающиеся с определенными бактериями.
Большинство бактерий делятся по устройству клеточной стенки на грамположительные, мембрана которых покрыта очень толстым слоем пептидогликанов, и грамотрицательные, у которых слой пептидогликана расположен между двумя мембранами. Использование природных эндолизинов особенно эффективно в случае грамположительных бактерий (стафилококков, стрептококков и др.), поскольку пептидогликановый слой у них расположен снаружи. Грамотрицательные бактерии (синегнойная палочка, сальмонеллы, кишечная палочка и др.) являются менее доступной мишенью, поскольку ферменту, чтобы добраться до внутреннего пептидогликанового слоя, необходимо проникнуть сквозь внешнюю бактериальную мембрану.
Для преодоления этой проблемы были созданы так называемые артилизины - модифицированные варианты природных эндолизинов, содержащие поликатионные или амфипатические пептиды, которые дестабилизируют внешнюю мембрану и обеспечивают доставку эндолизина непосредственно к пептидогликановому слою. Артилизины обладают высокой бактерицидной активностью и уже показали свою эффективность при лечении отитов у собак (Briers et al., 2014).
Примером модифицированного эндолизина, избирательно действующего на определенные бактерии, является препарат P128 канадской компании GangaGen Inc . Он представляет собой биологически активный фрагмент эндолизина, соединенный с лизостафином - адресующей белковой молекулой, которая связывается с поверхностью клеток стафилококков. Полученный химерный белок обладает высокой активностью против разных штаммов стафилококка, в том числе обладающих множественной лекарственной устойчивостью.
«Счетчики» бактерий
Бактериофаги служат не только разносторонним терапевтическим и «дезинфицирующим» средством, но и удобным и точным аналитическим инструментом микробиолога. К примеру, благодаря своей высокой специфичности они являются природными аналитическими реагентами для выявления бактерий определенного вида и штамма.
В простейшем варианте такого исследования в чашку Петри с питательной средой, засеянную бактериальной культурой, добавляют по капле различные диагностические бактериофаги. Если бактерия окажется чувствительной к фагу, то на этом месте бактериального «газона» образуется «бляшка» - прозрачный участок с убитыми и лизированными бактериальными клетками.
Анализируя размножение фагов в присутствии целевых бактерий, можно количественно определить численность последних. Так как количество фаговых частиц в растворе возрастет пропорционально числу содержавшихся в нем бактериальных клеток, то для оценки численности бактерий достаточно определить титр бактериофага.
Специфичность и чувствительность такой аналитической реакции достаточно высока, а сами процедуры просты в исполнении и не требуют сложного оборудования. Важно, что диагностические системы, основанные на бактериофагах, сигнализируют о наличии именно живого патогена, тогда как другие методы, такие как ПЦР и иммуноаналитические, свидетельствуют лишь о наличии биополимеров, принадлежащих этой бактерии. Такого типа диагностические методы особенно удобны для использования в экологических исследованиях, а также в пищевой индустрии и сельском хозяйстве.
Сейчас для выявления и количественного определения разных штаммов микроорганизмов применяют специальные референсные виды фагов. Очень быстрые, работающие практически в режиме реального времени аналитические системы могут быть созданы на основе генетически модифицированных бактериофагов, которые при попадании в бактериальную клетку запускают в ней синтез репортерных флуоресцирующих (или способных к люминесценции) белков, таких как люцифераза . При добавлении к подобной среде необходимых субстратов в ней будет появляться люминесцентный сигнал, величина которого соответствует содержанию бактерий в образце. Такие «меченные светом» фаги были разработаны для детекции опасных патогенов - возбудителей чумы, сибирской язвы, туберкулеза, а также инфекций растений.
Вероятно, с помощью модифицированных фагов удастся решить и давнюю задачу глобальной важности - разработать дешевые и быстрые методы детекции возбудителей туберкулеза на ранней стадии заболевания. Задача эта очень сложна, поскольку микобактерии, вызывающие туберкулез, отличаются крайне медленным ростом при культивировании в лабораторных условиях. Поэтому диагностика заболевания традиционными методами может затягиваться на срок до нескольких недель.
Фаговая технология позволяет упростить эту задачу. Суть ее в том, что к образцам анализируемой крови добавляют бактериофаг D29, способный поражать широкий спектр микобактерий. Затем бактериофаги отделяют, и образец перемешивают с быстрорастущей непатогенной культурой микобактерий, также чувствительной к этому бактериофагу. Если в крови первоначально имелись микобактерии, которые были инфицированы фагами, то в новой культуре будет также наблюдаться наработка бактериофага. Таким образом можно выявить единичные клетки микобактерий, а сам процесс диагностики с 2–3 недель сокращается до 2–5 дней (Swift & Rees, 2016).
Фаговый дисплей
В наши дни бактериофаги широко применяются также в качестве простых систем для наработки белков с заданными свойствами. Речь идет о разработанной в 1980-х гг. крайне эффективной молекулярно-селекционной методике - фаговом дисплее . Этот термин был предложен американцем Дж. Смитом, который доказал, что на основе бактериофагов кишечной палочки можно создать жизнеспособный модифицированный вирус, несущий на своей поверхности чужеродный белок. Для этого в фаговый геном внедряется соответствующий ген, который сливается с геном, кодирующим один из поверхностных вирусных белков. Такие модифицированные бактериофаги можно выделить из смеси с фагами дикого типа благодаря способности «чужого» белка связываться со специфичными антителами (Smith, 1985).
Из экспериментов Смита последовало два важных вывода: во-первых, используя технологию рекомбинантных ДНК, можно создавать огромные по разнообразию популяции численностью 10 6 –10 14 фаговых частиц, каждая из которых несет на своей поверхности разные варианты белков. Такие популяции назвали комбинаторные фаговые библиотеки . Во-вторых, выделив из популяции конкретный фаг (например, обладающий способностью связываться с определенным белком или органической молекулой), можно этот фаг размножить в бактериальных клетках и получить неограниченное число потомков с заданными свойствами.

С помощью фагового дисплея сегодня производят белки, которые могут избирательно связываться с терапевтическими мишенями, например, экспонированные на поверхности фага М13, способные узнавать и взаимодействовать с опухолевыми клетками. Роль этих белков в фаговой частице заключается в «упаковке» нуклеиновой кислоты, поэтому они хорошо подходят для создания препаратов генотерапии, только в этом случае они формируют частицу уже с терапевтической нуклеиновой кислотой.
На сегодня можно выделить два основных направления применения фагового дисплея. Технология на основе пептидов используется для исследования рецепторов и картирования сайтов связывания антител, создания иммуногенов и нановакцин, а также картирования сайтов связывания субстратов у белков-ферментов. Технология на основе белков и белковых доменов - для отбора антител с заданными свойствами, изучения белок-лигандных взаимодействий, скрининга экспрессируемых фрагментов комплементарной ДНК и направленных модификаций белков.
С помощью фагового дисплея можно вносить узнающие группировки во все виды поверхностных вирусных белков, а также в основной белок, формирующий тело бактериофага. Вводя в поверхностные белки пептиды с заданными свойствами, можно получить целый спектр ценных биотехнологических продуктов. Например, если этот пептид будет имитировать белок опасного вируса или бактерии, узнаваемый иммунной системой, то такой модифицированный бактериофаг представляет собой вакцину, которую можно просто, быстро и безопасно наработать.
Если же концевой поверхностный белок бактериофага «адресовать» на раковые клетки, а к другому поверхностному белку присоединить репортерные группы (например, флуоресцирующие или магнитные), то получится средство для обнаружения опухолей. А если к частице присоединить еще и цитотоксический препарат (а современная биоорганическая химия позволяет легко это сделать), то получится лекарство, направленно действующее на раковые клетки.
Одним из важных применений метода фагового дисплея белков является создание фаговых библиотек рекомбинантных антител, где антигенсвязывающие фрагменты иммуноглобулинов расположены на поверхности фаговых частиц fd или М13. Особый интерес представляют библиотеки антител человека, поскольку такие антитела могут быть использованы в терапии без ограничения. В последние годы только на фармацевтическом рынке США продается около полутора десятка терапевтических антител, сконструированных с использованием этого метода.
«Промышленные» фаги
Методология фагового дисплея нашла себе и совершенно неожиданное применение. Ведь бактериофаги в первую очередь являются наноразмерными частицами определенной структуры, на поверхности которых располагаются белки, которые с помощью фагового дисплея можно «снабдить» свойствами специфически связываться с нужными молекулами. Такие наночастицы открывают широчайшие возможности для создания материалов с заданной архитектурой и «умных» молекулярных наноустройств, при этом технологии их производства будут экологически чистыми.
Так как вирус представляет собой достаточно жесткую конструкцию с определенным соотношением размерностей, это обстоятельство позволяет использовать его для получения пористых наноструктур с известной площадью поверхности и нужным распределением пор в структуре. Как известно, именно площадь поверхности катализатора является критическим параметром, определяющим его эффективность. А существующие на сегодня технологии формирования на поверхности бактериофагов тончайшего слоя металлов и их оксидов позволяют получать катализаторы с чрезвычайно развитой регулярной поверхностью заданной размерности. (Lee et al., 2012).
Исследователь из Массачусетского технологического института А. Бельхер использовала бактериофаг M13 как шаблон для роста наночастиц и нанопроводов родия и никеля на поверхности оксида церия. Полученные наночастицы катализатора способствуют конвертации этанола в водород, таким образом, этот катализатор может оказаться весьма полезным для модернизации существующих и создания новых водородных топливных ячеек. Катализатор, выращенный на шаблоне вируса, отличается от аналогичного по составу «обычного» катализатора более высокой стабильностью, он менее подвержен старению и дезактивации поверхности (Nam et al. , 2012).

Путем покрытия нитчатых фагов золотом и двуокисью индия были получены электрохромные материалы - пористые нанопленки, меняющие цвет при изменении электрического поля, способные реагировать на изменение электрического поля в полтора раза быстрее известных аналогов. Подобного рода материалы перспективны для создания энергосберегающих ультратонких экранных устройств (Nam et al., 2012).
В Массачусетском технологическом институте бактериофаги стали основой для производства очень мощных и чрезвычайно компактных электрических батарей. Для этого использовали живые, генетически модифицированные фаги М13, неопасные для человека и способные присоединять к поверхности ионы различных металлов. В результате самосборки этих вирусов были получены структуры заданной конфигурации, которые при покрытии металлом сформировали достаточно длинные нанопровода, ставшие основой анода и катода. При самоформировании материала анода использовался вирус, способный присоединять золото и оксид кобальта, для катода - способный присоединять фосфат железа и серебро. Последний фаг также обладал способностью за счет молекулярного опознания «подхватывать» концы углеродной нанотрубки, что необходимо для обеспечения эффективного переноса электронов.
На основе комплексов бактериофага М13, двуокиси титана и одностенных углеродных нанотрубок были также созданы материалы для солнечных батарей (Dang et al., 2011).
Последние годы ознаменовались широкими исследованиями бактериофагов, которые находят себе все новые применения не только в терапии, но и в био- и нанотехнологиях. Их очевидным практическим результатом должно стать возникновение нового мощного направления персонализированной медицины, а также создание целого спектра технологий в пищевой промышленности, ветеринарии, сельском хозяйстве и в производстве современных материалов. Мы ждем, что второе столетие исследований бактериофагов принесет не меньше открытий, чем первое.
Литература
1.
Бактериофаги: биология и применение / Ред.: Э. Каттер, А. Сулаквелидзе. М.: Научный мир. 2012.
2.
Стент Г., Кэлиндар Р. Молекулярная генетика. М.: Мир. 1974. 614 с.
3.
Тикунова Н. В., Морозова В. В. Фаговый дисплей на основе нитчатых бактериофагов: применение для отбора рекомбинантных антител // Acta Naturae
. 2009. № 3. C. 6–15.
4.
Mc Grath S., van Sinderen D. Bacteriophage: Genetics and Molecular Biology. Horizon Scientific Press, 2007.
№ 10-2013
Фотография, сделанная с помощью электронного микроскопа,
показывает процесс закрепления бактериофагов (колифагов T1) на поверхности бактерии E. coli
.
В конце ХХ века стало ясно, что бактерии безусловно доминируют в биосфере Земли, составляя более 90% ее биомассы. У каждого вида имеется множество специализированных типов вирусов. По предварительным оценкам, число видов бактериофагов составляет около 10 15 . Чтобы понять масштаб этой цифры, можно сказать, что если каждый человек на Земле будет каждый день открывать по одному новому бактериофагу, то на описание всех их понадобится 30 лет.
Таким образом, бактериофаги – самые малоизученные существа в нашей биосфере. Большинство известных сегодня бактериофагов принадлежит к отряду Caudovirales – хвостатые вирусы. Их частицы имеют размер от 50 до 200 нм. Хвост разной длины и формы обеспечивает присоединение вируса к поверхности бактерии-хозяина, головка (капсид) служит хранилищем для генома. Геномная ДНК кодирует структурные белки, формирующие «тело» бактериофага, и белки, которые обеспечивают размножение фага внутри клетки в процессе инфекции.
Можно сказать, что бактериофаг – это природный высокотехнологичный нанообъект. Например, хвосты фагов представляют собой «молекулярный шприц», который протыкает стенку бактерии и, сокращаясь, впрыскивает свою ДНК внутрь клетки. С этого момента начинается инфекционный цикл. Его дальнейшие этапы состоят из переключения механизмов жизнедеятельности бактерии на обслуживание бактериофага, размножение его генома, построение множества копий вирусных оболочек, упаковки в них ДНК вируса и, наконец, разрушение (лизис) хозяйской клетки.

Бактериофаг – это не живое существо, а молекулярный наномеханизм, созданный природой.
Хвост бактериофага – шприц, который протыкает стенку бактерии и впрыскивает вирусную ДНК,
которая хранится в головке (капсиде), внутрь клетки
.
Помимо постоянного эволюционного соревнования механизмов защиты у бактерий и нападения у вирусов, причиной сложившегося равновесия можно считать и то, что бактериофаги специализировались по своему инфекционному действию. Если имеется крупная колония бактерий, где своих жертв найдут и следующие поколения фагов, то уничтожение бактерий литическими (убивающими, дословно – растворяющими) фагами идет быстро и непрерывно.
Если потенциальных жертв маловато или внешние условия не слишком подходят для эффективного размножения фагов, то преимущество получают фаги с лизогенным циклом развития. В этом случае после внедрения внутрь бактерии ДНК фага не сразу запускает механизм инфекции, а до поры до времени существует внутри клетки в пассивном состоянии, зачастую внедряясь в бактериальный геном.
В таком состоянии профага вирус может существовать долго, проходя вместе с хромосомой бактерии циклы деления клетки. И лишь когда бактерия попадает в благоприятную для размножения среду, активируется литический цикл инфекции. При этом, когда ДНК фага освобождается из бактериальной хромосомы, часто захватываются и соседние участки бактериального генома, а их содержимое в дальнейшем может перенестись в следующую бактерию, которую заразит бактериофаг. Этот процесс (трансдукция генов) считается важнейшим средством переноса информации между прокариотами – организмами без клеточных ядер.

Как действует бактериофаг
Все эти молекулярные тонкости не были известны во втором десятилетии ХХ века, когда были открыты «невидимые инфекционные агенты, уничтожающие бактерий». Но и без электронного микроскопа, с помощью которого в конце 1940-х впервые удалось получить изображения бактериофагов, было понятно, что они способны уничтожать бактерии, в том числе и болезнетворные. Это свойство было незамедлительно востребовано медициной.
Первые попытки лечения фагами дизентерии, раневых инфекций, холеры, тифа и даже чумы были проведены достаточно аккуратно, и успех выглядел вполне убедительно. Но после начала массового выпуска и использования фаговых препаратов эйфория сменилась разочарованием. О том, что такое бактериофаги, как производить, очищать и применять их лекарственные формы, было известно еще очень мало. Достаточно сказать, что по результатам предпринятой в США в конце 1920-х годов проверки во многих промышленных фагопрепаратах собственно бактериофагов вообще не оказалось.
Проблема с антибиотиками
Вторую половину ХХ века в медицине можно назвать «эрой антибиотиков». Однако еще первооткрыватель пенициллина Александр Флеминг в своей нобелевской лекции предупреждал, что устойчивость микробов к пенициллину возникает довольно быстро. До поры до времени антибиотикоустойчивость компенсировалась разработкой новых типов противомикробных лекарств. Но с 1990-х годов стало ясно, что человечество проигрывает «гонку вооружений» против микробов.
Виновато прежде всего бесконтрольное применение антибиотиков не только в лечебных, но и в профилактических целях, причем не только в медицине, но и в сельском хозяйстве, пищевой промышленности и быту. В результате устойчивость к этим препаратам начала вырабатываться не только у болезнетворных бактерий, но и у самых обычных микроорганизмов, живущих в почве и воде, делая из них «условных патогенов».
Такие бактерии комфортно существуют в медицинских учреждениях, заселяя сантехнику, мебель, медицинскую аппаратуру, порой даже дезинфицирующие растворы. У людей с ослабленным иммунитетом, каких в больницах большинство, они вызывают тяжелейшие осложнения.
Неудивительно, что медицинское сообщество бьет тревогу. В прошедшем, 2012 году гендиректор ВОЗ Маргарет Чен выступила с заявлением, предсказывающим конец эры антибиотиков и беззащитность человечества перед инфекционными заболеваниями. Впрочем, практические возможности комбинаторной химии – основы фармакологической науки – далеко не исчерпаны. Другое дело, что разработка противомикробных средств – очень дорогой процесс, не приносящий таких прибылей, как многие другие лекарства. Так что страшилки о «супербактериях» – это скорее предостережение, побуждающее людей к поискам альтернативных решений.
Бактериофаги и иммунитет
Поскольку бактериофагов в природе несметное количество и они постоянно попадают в организм человека с водой, воздухом и пищей, то иммунитет их просто игнорирует. Существует даже гипотеза о симбиозе бактериофагов в кишечнике, регулирующем кишечную микрофлору. Добиться какой-то иммунной реакции можно лишь при длительном введении в организм больших доз фагов.
Но таким образом можно добиться аллергии на почти любые вещества. И наконец, очень важно, что бактериофаги недороги. Разработка и производство препарата, состоящего из точно подобранных бактериофагов с полностью расшифрованными геномами, культивированных по современным биотехнологическим стандартам на определенных штаммах бактерий в химически чистых средах и прошедших высокую очистку, на порядки дешевле, чем современных сложных антибиотиков.
Это позволяет быстро приспосабливать фаготерапевтические препараты к меняющимся наборам патогенных бактерий и применять бактериофаги в ветеринарии, где дорогие лекарства экономически не оправданы.
На медицинской службе
Вполне логичным выглядит возрождение интереса к использованию бактериофагов – естественных врагов бактерий – для лечения инфекций. Действительно, за десятилетия «эры антибиотиков» бактериофаги активно служили науке, но не медицине, а фундаментальной молекулярной биологии. Достаточно упомянуть расшифровку «триплетов» генетического кода и процесса рекомбинации ДНК. Сейчас о бактериофагах известно достаточно, чтобы обоснованно выбирать фаги, подходящие для терапевтических целей.
Достоинств у бактериофагов как потенциальных лекарств множество. Прежде всего – это их несметное количество. Хотя изменять генетический аппарат бактериофага тоже намного проще, чем у бактерии, и тем более – у высших организмов, в этом нет необходимости. Всегда можно подобрать что-то подходящее в природе. Речь идет скорее о селекции, закреплении востребованных свойств и размножении нужных бактериофагов.
Это можно сравнить с выведением пород собак – ездовых, сторожевых, охотничьих, гончих, бойцовых, декоративных… Все они при этом остаются собаками, но оптимизированы под определенный вид действий, нужных человеку. Во-вторых, бактериофаги строго специфичны, то есть они уничтожают только определенный вид микробов, не угнетая при этом нормальную микрофлору человека.
В-третьих, когда бактериофаг находит бактерию, которую должен уничтожить, он в процессе своего жизненного цикла начинает размножаться. Таким образом, не столь острым становится вопрос дозировки. В-четвертых, бактериофаги не вызывают побочных эффектов. Все случаи аллергических реакций при использовании терапевтических бактериофагов были вызваны либо примесями, от которых препарат был недостаточно очищен, либо токсинами, выделяющимися при массовой гибели бактерий. Последнее явление, «эффект Герксхаймера», нередко наблюдается и при применении антибиотиков.
Две стороны медали
К сожалению, недостатков у медицинских бактериофагов тоже немало. Самая главная проблема проистекает из достоинства – высокой специфичности фагов. Каждый бактериофаг инфицирует строго определенный тип бактерий, даже не таксономический вид, а ряд более узких разновидностей, штаммов. Условно говоря, как если бы сторожевая собака начинала лаять только на одетых в черные плащи громил двухметрового роста, а на лезущего в дом подростка в шортах никак не реагировала.
Поэтому для нынешних фаговых препаратов нередки случаи неэффективного применения. Препарат, сделанный против определенного набора штаммов и прекрасно лечащий стрептококковую ангину в Смоленске, может оказаться бессильным против по всем признакам такой же ангины в Кемерове. Болезнь та же, вызывается тем же микробом, а штаммы стрептококка в разных регионах оказываются различными.
Для максимально эффективного применения бактериофага необходима точная диагностика патогенного микроба, вплоть до штамма. Самый распространенный сейчас метод диагностики – культуральный посев – занимает много времени и требуемой точности не дает. Быстрые методы – типирование с помощью полимеразной цепной реакции или масс-спектрометрии – внедряются медленно из-за дороговизны аппаратуры и более высоких требований к квалификации лаборантов. В идеале подбор фагов-компонентов лекарственного препарата можно было бы делать против инфекции каждого конкретного пациента, но это дорого и на практике неприемлемо.
Другой важный недостаток фагов – их биологическая природа. Кроме того, что бактериофаги для поддержания инфекционности требуют особых условий хранения и транспортировки, такой метод лечения открывает простор для множества спекуляций на тему «посторонней ДНК в человеке». И хотя известно, что бактериофаг в принципе не может заразить человеческую клетку и внедрить в нее свою ДНК, поменять общественное мнение непросто.
Из биологической природы и довольно большого, по сравнению с низкомолекулярными лекарствами (теми же антибиотиками), размера вытекает третье ограничение – проблема доставки бактериофага в организм. Если микробная инфекция развивается там, куда бактериофаг можно приложить напрямую в виде капель, спрея или клизмы, – на коже, открытых ранах, ожогах, слизистых оболочках носоглотки, ушей, глаз, толстого кишечника – то проблем не возникает.
Но если заражение происходит во внутренних органах, ситуация сложнее. Случаи успешного излечения инфекций почек или селезенки при обычном пероральном приеме препарата бактериофага известны. Но сам механизм проникновения относительно крупных (100 нм) фаговых частиц из желудка в кровоток и во внутренние органы изучен плохо и сильно разнится от пациента к пациенту. Бактериофаги бессильны и против тех микробов, которые развиваются внутри клеток, например возбудителей туберкулеза и проказы. Через стенку человеческой клетки бактериофаг пробраться не может.
Нужно отметить, что противопоставлять применение бактериофагов и антибиотиков в медицинских целях не следует. При совместном их действии наблюдается взаимное усиление противобактериального эффекта. Это позволяет, например, снизить дозы антибиотиков до значений, не вызывающих выраженных побочных эффектов. Соответственно, и механизм выработки у бактерий устойчивости к обоим компонентам комбинированного лекарства почти невозможен.
Расширение арсенала противомикробных препаратов дает больше степеней свободы в выборе методики лечения. Таким образом, научно обоснованное развитие концепции применения бактериофагов в противомикробной терапии – перспективное направление. Бактериофаги служат не столько альтернативой, сколько дополнением и усилением в борьбе с инфекциями.
С.М. ЗАХАРЕНКО, к.м.н., доцент, Военно-медицинская академия им. С.М. Кирова, Санкт-Петербург
Бактериофаги – уникальные микроорганизмы, на основе которых создана особая по своим свойствам и характеристикам группа лечебно-профилактических препаратов. Лежащие в основе их действия природные физиологические механизмы взаимодействия фагов и бактерий позволяют прогнозировать бесконечное разнообразие как самих бактериофагов, так и возможных способов их применения. По мере расширения коллекций бактериофагов, несомненно, будут появляться новые целевые патогены, будет расширяться спектр заболеваний, при которых фаги могут применяться как в режиме монотерапии, так и в составе комплексных схем лечения.
Так, использование поливалентного пиобактериофага Секстафаг при лечении инфицированного панкреонекроза (Пермская государственная медицинская академия им. академика Е.А. Вагнера) позволило быстрее восстанавливать у больных основные параметры гомеостаза и функции органов и систем. Также значительно снизилось количество послеоперационных осложнений и летальных исходов: в группе больных, получавших стандартную терапию, летальность составила 100%, в то время как в труппе, получавшей БФ, - 16,6% .
Вследствие безвредности и ареактогенности препаратов БФ возможно их применение в педиатрической практике, в т. ч. и у новорожденных детей. Интересен опыт Нижегородской детской областной клинической больницы, где в период осложнения эпидемиологической ситуации наряду с обычными противоэпидемическими мероприятиями были использованы и БФ - Интести-бактериофаг и БФ Pseucfomonas aeruginosa. Снижение заболеваемости внутибольничной инфекцией синегнойной этиологии в 11 раз показало высокую эффективность применения БФ . Препараты БФ могут назначаться как для лечения дисбактериоза и расстройств пищеварительной системы, так и для предотвращения колонизации слизистых оболочек желудочно-кишечного тракта условно-патогенными бактериями. Поликомпонентные препараты БФ идеальны для немедленного купирования первых признаков расстройства желудочно-кишечного тракта.

На сегодняшний день на предприятии намечен целый ряд приоритетных направлений разработки и производства лечебно-профилактических бактериофагов, которые коррелируют с вновь зарождающимися общемировыми тенденциями. Создаются и внедряются новые препараты: разработаны БФ против серраций и энтеробактерий, ведутся работы по созданию фагового препарата против Helicobacter pylori.
Лишь один производитель этих препаратов – НПО «Микроген», по докладу замглавы управления науки и инновационного развития Аллы Лобастовой, выпускает более 2 млн упаковок ежегодно .
К сожалению, представления многих врачей о бактериофагах далеки от объективности. Не многие знают, что бактериофаги, активные в отношении одного и того же возбудителя, могут относиться к разным семействам, обладать различным жизненным циклом и т. п. Так, например, бактериофаги P. aeruginosa относятся к семействам Myoviridae, Podoviridae, Siphoviridae, имеют литический жизненный цикл или умеренный. Разные штаммы одного и того же патогена могут обладать различной чувствительностью к бактериофагам.
Большинство специалистов знают (слышали, кто-то применял) о существовании жидкой и таблетированной лекарственной формы лечебно-профилактических препаратов бактериофагов. Однако их спектр существенно шире, что может быть отнесено к безусловным преимуществам, особенно в сочетании с многообразием путей введения (прием внутрь, введение в клизмах, аппликации, орошение ран и слизистых оболочек, введение в раневые полости и т. п.) .
К очевидным преимуществам бактериофагов традиционно относят специфическое воздействие на достаточно ограниченную популяцию бактерий, ограниченное во времени существование (пока не исчезнет целевая популяция микроорганизмов), отсутствие таких побочных эффектов, как токсические и аллергические реакции, дисбиотические реакции и др. Эти препараты могут применяться в самых разных возрастных группах и при беременности .
Сами бактериофаги не являются значимыми аллергенами. Случаи непереносимости препаратов бактериофагов связаны в своем большинстве с реакцией на компоненты питательной среды. Все крупные производители этой группы препаратов стремятся к максимальному качеству используемых компонентов, что уменьшает вероятность таких реакций.
В условиях роста антибиотикорезистентности некоторые авторы предлагают рассматривать бактериофаги как наилучшую альтернативу антибиотикам.
Лечебно-профилактические препараты бактериофагов представляют собой коктейль из специально подобранных комбинаций (комплекс поликлональных высоковирулентных бактериальных вирусов, специально подобранных против наиболее часто встречающихся групп возбудителей бактериальных инфекций) на основе коллекций фагов производителя . Филиалы ФГУП «НПО «Микроген» в Уфе, Перми и Нижнем Новгороде – современные центры производства таких препаратов. Возможность создания адаптированных к конкретным патогенным микроорганизмам лечебно-профилактических препаратов бактериофагов – еще одно важнейшее преимущество этой группы препаратов.
Рост устойчивости бактерий к антимикробным препаратам и часто встречающаяся полиэтиологичность современных инфекционных заболеваний требуют проведения комбинированной антибиотикотерапии (двух, трех, а иногда и более антимикробных препаратов). Для выбора эффективной схемы терапии антибиотиками, помимо собственно чувствительности бактерии к препарату, необходимо учесть достаточно большое число факторов. Фаготерапия в этом отношении также имеет определенные преимущества.
С одной стороны, применение комбинации бактериофагов не сопровождается их взаимодействием между собой и не ведет к изменению схем их применения. В рамках имеющегося набора лечебных бактериофагов существуют ряд хорошо себя зарекомендовавших комбинаций – бактериофаг колипротейный, пиобактериофаг поливалентный, интести-бактериофаг. С другой стороны, бактерии не имеют общих механизмов устойчивости к антибиотикам и фагам, следовательно, могут они применяться как при устойчивости патогена к одному из препаратов, так и в комбинации «антибиотик + бактериофаг». Особенно эффективна такая комбинация для разрушения микробных биопленок.
В эксперименте убедительно показано, что комбинированное применение антагонистов железа и бактериофага способно нарушать формирование биопленок Klebsiella pneumoniae . При этом отмечается как достоверное уменьшение численности микробной популяции, так и уменьшение числа «молодых» клеток.
Еще одной важной особенностью действия бактериофагов является такой феномен, как индукция апоптоза. Некоторые штаммы E. coli имеют гены, вызывающие гибель клетки после внедрения в нее бактериофага Т4 . Так, в ответ на экспрессию поздних генов фага Т4 ген lit (кодирует протеазу, разрушающую необходимый для синтеза белков фактор элонгации EF-Tu ) блокирует синтез всех клеточных белков. Ген prrC кодирует нуклеазу, расщепляющую лизиновую тРНК. Нуклеаза активируется продуктом гена stp фага Т4. У инфицированных фагом Т4 клеток гены rex (относятся к геному фага и экспрессируются в лизогенных клетках) вызывают формирование ионных каналов, ведущих к потере клетками жизненно важных ионов и впоследствии к гибели. Предотвратить гибель клетки может сам фаг Т4, закрывая каналы своими белками, продуктами генов rII .
В случае формирования устойчивости бактерий к антибиотику приходится искать новые варианты модификации активной молекулы или принципиально новые вещества. К сожалению, за последние годы темпы внедрения новых антибиотиков существенно замедлились. Ситуация с бактериофагами принципиально иная. Коллекции крупных производителей насчитывают десятки готовых штаммов бактериофагов и постоянно пополняются новыми активными фагами . Благодаря постоянно проводимому мониторингу чувствительности выделяемых патогенов к бактериофагам производители корректируют поставляемые в регионы фаговые композиции . Благодаря адаптированным бактериофагам удается ликвидировать вспышки внутригоспитальных инфекций, вызываемых резистентными к антибиотикам штаммами .

При пероральном приеме бактериофаги быстро достигают очагов локализации инфекции: при пероральном приеме больными с гнойно-воспалительными заболеваниями уже через час фаги попадают в кровь, через 1–1,5 ч выявляются из бронхолегочного экссудата и с поверхности ожоговых ран, через 2 ч – из мочи, а также из ликвора больных с черепно-мозговыми травмами .
Таким образом, бактериофаги – уникальные микроорганизмы, на основе которых создана особая по своим свойствам и характеристикам группа лечебно-профилактических препаратов. Лежащие в основе их действия природные физиологические механизмы взаимодействия фагов и бактерий позволяют прогнозировать бесконечное разнообразие как самих бактериофагов, так и возможных способов их применения. По мере расширения коллекций бактериофагов, несомненно, будут появляться новые целевые патогены, будет расширяться спектр заболеваний, при которых фаги могут применяться как в режиме монотерапии, так и в составе комплексных схем лечения. Современный взгляд на дальнейшую судьбу фаготерапии должен быть основан как на высокой специфичности их действия, так и на необходимости строго соблюдения всех правил фаготерапии. Противопоставление бактериофагов любым средствам этиотропной терапии является ошибочным.
Впервые, предположение, что бактериофаги являются вирусами сделал. Д.Эррель. В дальнейшем открыты вирусы грибков и тд, называть стали фаги.
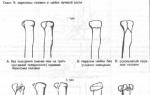
Морфология фага.
Размеры - 20 - 200нм. Большинство фагов имеют форму головастиков. Наиболее сложно устроенные фаги состоят из многогранной головки, в которой располагается нуклеиновая кислота, шейка и отростки. На конце отростка располагается базальная пластинка, с отходящими от нее нитями и зубцами. Эти нити и зубцы служат для прикрепления фага к оболочке бактерии. У наиболее сложноорганизованных фагов в дистальной части отростка, содержится фермент - лизоцим . Этот фермент способствует растворению оболочки бактерий при проникновении фаговой НК в цитоплазму. У многих фагов отросток окружен чехлом, который у некоторых фагов может сокращаться.
Различают 5 морфологических групп
- Бактериофаги с длинным отростком и сокращающимся чехлом
- Фаги с длинным отростком, но не сокращающимся чехлом
- Фаги с коротким отростком
- Фаги с аналогом отростка
- Нитевидные фаги
Химический состав.
Фаги состоят из нуклеиновой кислоты и белков. Большинство из них содержит 2хнитевую ДНК, замкнутую в кольцо. Некоторые фаги содержат одну нить ДНК или РНК.
Оболочка фагов - капсид , состоит из упорядоченных белковых субъединиц - капсомеров.
У наиболее сложноорганизованных фагов в дистальной части отростка, содержится фермент - лизоцим . Этот фермент способствует растворению оболочки бактерий при проникновении фаговой НК в цитоплазму.
Фаги хорошо переносят замораживание, нагревание до 70, высушивание. Чувствительны к кислотам, УФ и кипячению. Фаги инфицируют строго определенные бактерии, взаимодействую со специфическими рецепторами клеток.
По специфичности взаимодействия -
Полифаги - взаимодействующие с несколькими родственными видами бактерий
Монофаги - видовые фаги - взаимодействуют с одним видом бактерий
Типовые фаги - взаимодействуют с отдельными вариантами бактерий внутри вида.
По действию типовых фагов вид можно разделить на фаговый ряд . Взаимодействие фагов с бактериями может протекать по продуктивному, апродуктивному и интегративному типу.
Продуктивный тип - образуется фаговое потомство, а клетка лизируется
При апродуктивном - клетка продолжает существовать, процесс взаимодействия обрывается на начальной стадии
Интегративный тип - геном фага интегрирует в хромосому бактерий и сосуществует с ним.
В зависимости от типов взаимодействия различают вирулентные и умеренные фаги.
Вирулентные взаимодействуют с бактериями по продуктивному типу. В начале происходит абсорбция фага на оболочке бактерий, за счет взаимодействия специфических рецепторов. Имеет место проникновение или пенетрация вирусной нуклеиновой кислоты в цитоплазму бактерий. Под действием Лизоцима в оболочке бактерии образуется небольшое отверстие, чехол у фага сокращается и НК впрыскивается. Оболочка фага за пределами бактерии. Далее осуществляется синтез ранних белков. Они обеспечивают синтез фаговых структурных белков, репликацию фаговой нуклеиновой кислоты и репрессию деятельности бактериальной хромосом.
После этого происходит синтез структурных компонентов фагов и репликация нуклеиновой кислоты. Из этих элементов происходит сборка нового поколения фаговых частиц. Сборка носит название морфогенез, новых частиц, которых в одной бактерии может образовываться 10-100. Далее лизис бактерии и выход нового поколения фагов во внешнюю среду.
Умеренные бактериофаги взаимодействуют либо по продуктивному, либо по интегративному типу. Продуктивный цикл идет аналогично. При интегративном взаимодействии - ДНК умеренного фага после попадания в цитоплазму встраивается в хромосому в определенном участке, причем при делении клетки реплицируется синхронно с бактериальной ДНК и вот эти структуры передаются дочерним клеткам. Такая встроенная ДНК фага - профаг , а бактерия, содержащая профаг, называется лизогенной, а явление - лизогения.
Спонтанно, или под влиянием ряда внешних факторов профаг может вырезаться из хромосомы, т.е. переходить в свободное состояние, проявлять свойства вирулентного фага, что будет приводить к образованию нового поколения бактериальных тел - индукция профага .
Лизогенезация бактерий лежит в основе фаговой(лизогенной) конверсии. Под этим понимают изменение признаков или свойств у лизогенных бактерий, по сравнению с нелизогенными того же вида. Изменяться могут разные свойства - морфологические, антигенные и тд.
Умеренные фаги могут быть дефектными - не способными образовывать фаговое потомство не в естественных условиях и в индукции.
Вирион - полноценная вирусная частица, состоящая из НК и белковой оболочки
Практическое применение фагов -
- Применение в диагностике. В отношение ряда вида бактерий монофаги, используются в реакция фаголизабельности, как один из критериев идентификации культуры бактерии, типовые фаги применяют для фаготипирования, для внутривидовой дифференциации бактерий. Проводятся с эпидимиологоическими целями, для установления источника инфекции и путей устранения
- Для лечения и профилактики ряда бактериальных инфекций - брюшной тип, стафилококковы и стрептококковые инфекции(таблетки с кислотоустойчивым покрытием)
- Умеренные бактериофаги применяют в генной инженерии в качестве вектора, способных вносить генетический материал в живую клетку.
Генетика бактерий
Бактериальный геном состоит из генетических элементов, способных к самовоспроизведению - репликонов. Репликонами является бактериальные хромосомы и плазмиды. Бактериальная хромосома формирует нуклеоид, замкнутым кольцом не связанным с белками и несет гаплоидный набор генов.
Плазмиды представляет собой также замкнутое кольцо молекулы ДНК, но гораздо меньших размеров чем хромосома. Наличии плазмид в цитоплазме бактерий не обязательно, но они придают преимущество в окружающей среде. Крупные плазмиды редуцируются с хромосомой и количество их в клетке небольшое. А число мелких плазмид может достигать нескольких десятков. Некоторые плазмиды способны обратимо встраиваться в бактериальную хромосому в определенном ее участке и функционировать в виде единого репликона. Такие плазмиды называются интегративными. Некоторые плазмиды способны передаваться от одной бактерии к другой при непосредственном контакте - коньюгативные плазмиды. Они содержат гены, ответственные за образование F-пилей, формирующих коньюгативный мостик, для передачи генетического материалы.
Основные типы плазмидов-
F - интегративная коньгативная плазмида. Половой фактор, определяет способность бактерий быть донорами при коньюгации
R - плазмиды. Резистентная. Содержит гены, детерминирующие синтез факторов, разрушающих антибактериальные препараты. Бактерии, обладающие такими плазмидами не чувствительны ко многим препаратам. Поэтому формируются устойчивые к препаратам фактор.
Токс плазмиды - детерминирующие факторы патогенности -
Ent - плазмиды - содержит ген за выработку энтеротоксинов.
Hly - разрушают эритроцит.
Подвижные генетические элементы. К ним относятся вставочные - инсерционные элементы . Общепринятое обозначение - Is. Это участки ДНК, способные перемещаться как внутри репликона, так и между ними. Они содержат только гены, необходимые для их собственного перемещения.
Транспозоны - более крупные структуры, обладающие темиже свойствами, что и Is, го помимо они содержат структурные гены, определяющие синтез биологических веществ, например токсинов. Подвижные генетические элементы могут вызывать инактивацию гена, повреждение генетического материала, слияние репликонов и распространение генов в популяции бактерий.
Изменчивость у бактерий.
Все виды изменчивости подразделяют на 2 группы - ненаследственная(фенотипическая, модификационная) и наследственная(генотипическая).
Модификации - фенотипчиеские не наследуемые изменения признаков или свойств. Модификации не затрагивают генотипа, а поэтому не передаются по наследству. Они являются адаптивными реакциями, на изменение каких то конкретных условий внешней среды. Как правило утрачиваются в первом поколении, после прекращения действия фактора.
Генотипическая изменчивость затрагивает генотип организма, а поэтому способна передаваться потомкам. Генотипическая изменчивость подразделяется на мутации и рекомбинации.
Мутации - стойкие, наследуемые изменения признаков или свойств организма. Основа мутаций - качественное или количественное изменение последовательности нуклеотидов в молекуле ДНК. Мутации могут изменять практически любые свойства.
По происхождению мутации - спонтанные и индуцируемые.
Спонтанные мутации происходит в естественных условиях существования организма, а индцированные возникают в результате направленного действия мутагенного фактора. ПО характеру изменений в первичной структуре ДНК у бактерий различают генные или точковые мутации и хромосомные аберрации.
Генные мутации происходят внутри одного гена и минимально захватывают один нуклеотид. Этот тип мутаций может быть следствием замены одно нуклеотида на другой, выпадения нуклеотида или вставления лишнего.
Хромосомные - могут затрагивать несколько хромосом.
Может быть делеция - потеря участка хромосомы, дупликация - удвоения участка хромосомы. Поворот участка хромосомы на 180 градусов - инверсия.
Любая мутация возникает под действием определенного мутагенного фактора. По своей природе мутагены - физические, химические и биологические. Ионизирующая радиация, рентгеновские лучи, УФ лучи. К химическим мутагенам - аналоги азотистых оснований, саму азотистую кислоту, и даже некоторые лекарственные средства, цитостатики. К биологическим - некоторые вирусы и трансфазоны
Рекомбинация - обмен участками хромосом
Трансдукция - перенос генетического материала с помощью бактериофага
Репарация генетического материала - восстановление возникших в результате мутаций повреждений.
Существует несколько видов репарации
- Фотореактивация - этот процесс обеспечивается специальным ферментом, который активируется в присутствии видимого света. Этот фермент перемещается по цепочке ДНК и восстанавливает повреждения. Объединяет тимеры, которые образуются при действии УФ. Более значимы результаты темновой репарации. Она не зависит от света и обеспечивается несколькими ферментами - вначале нуклеазы вырезают поврежденный участок цепи ДНК, затем ДНК полимераза, на матрице сохранившейся комплементарно цепи синтезирует заплату, а лигазы вшивают заплатку на поврежденное место.
Репарации подвергаются генные мутации, а хромосомные как правило нет
- Генетические рекомбинации у бактерий. Характеризуются проникновением генетического материала от бактерии донора в бактерию реципиента с формированием дочернего генома, содержащим генов обеих исходных особей.
Включение фрагмента ДНК донора в рецепиента происходит кроссинговером
Три типа передачи -
- Трансформация - процесс, при котором происходит передача фрагмента изолированной ДНК донора. Зависит от компетентности рецепиента и состояния донорской ДНК. Компетентность - способность поглощать ДНК. Она зависит от присутствия в клеточной мембране реципиента особых белков и формируется в определенные периоды роста бактерии. Донорская ДНК обязательно должна быть двухцепочечной и не очень большой по размеру. Донорская ДНК проникает через оболочку бактерий, причем одна из цепочек разрушается, другая встраивается в ДНК реципиента.
- Трансдукция - осуществляется с помощью бактериофагов. Общая трансдукция и специфическая трансдукция.
Общая - происходит при участии вирулентных факторов. В процессе сборки фагов частиц в головку фага по ошибке может включаться не фаговая ДНК, а кусочек хромосомы бактерий. Такие фаги - дефектные фаги.
Специфическая - она осуществляется умеренными фагами. При вырезании, вырезание его строго осуществляется по границе.Встраиваются между определёнными генами и переносят их.
- Коньюгация - передача генетического материала от бактерии донора рецепиенту, при их непосредственном контакте. Необходимым условием - наличие в клетке донора коньгативного плазмида. При коньюгации за счет пилей образуется коньюгационный мостик, по которому генетический материал передается от донора к пациенту.
Генодиагностика
Комплекс методов, позволяющих выявить геном микроорганизма или его фрагмента в исследуемом материале. Первым был предложен метод гибридизации НК. Основан на использовании принципа комплиментарности. Этот метод позволяет выявить в генетическом материале наличие маркерных фрагментов ДНК возбудителя с помощью молекулярных зондов. Молекулярные зонды представляют собой короткие цепочки ДНК, комплементарные маркерному участку. В состав зонда вводится метка - флюорозром, радиоактивный изотоп, фермент. Исследуемый материал подвергается специальнйо обработке, позволяющей разрушить микрооргнаизмы, высвободить ДНК и разделить ее на одноцепочечные фрагменты. После этого материал фиксируется. Затем выявляется активность метки. Этот метод не отличается высокой чувствительностью. Можно выявить возбудителя лишь при достаточно большом его количестве. 10 в 4 микроорганизмов. Он достаточно сложен технически и требует большого количества зондов. Широкого распространения в практике он не нашел. Был разработан новый метод - полимеразная цепная реакция - ПЦР.
Этот метод основан на способности ДНК и вирусных РНК к репликации, т.е. к саморепродукции. Суть у пациента - является многократное копирование - амплификация in vitro фрагмента ДНК, являющего маркерного для данного микроорганищма. Так как процесс проходит при достаточно высоких температурах 70-90, то метод стал возможен после выделения из термофильных бактерий термостабильной ДНК-полимеразы. Механизм амплификации таков, что копирование цепочек ДНК начинается не в любой точке, а только в определенных стартовых блоках для создания которых используют так называемые праймеры. Праймеры представляют собой полинуклеотидные последовательности, комплиментарные концевым последовательностям копируемого фрагмента искомой ДНК, причем праймеры не только инициируют амплификацию, но и ограничивают. Сейчас существует несколько вариантов ПЦР характерны 3 этапа -
- Денатурация ДНК(разделение на 1 цепочечные фрагменты)
- Присоединение праймера.
- Комплиментарное достраивание цепей ДНК до 2хцепочечных
Этот цикл длится 1,5-2 минуты. В результате количество молекул ДНК удваивает 20-40 раз. В результате 10 в 8 степени копий. После амплификации производят электрофорез и выделяются в виде полосок. Она проводится в специальном приборе, который называется амплификатор.
Достоинства ПЦР
- Дает прямые указания на присутствие возбудителя в исследуемом материале, без выделения чистой культуры.
- Очень высокая чувствительность. Теоретически можно обнаружить 1го.
- Материал для исследования может быть сразу дизенфицировать после забора.
- 100% специфичность
- Быстрота получения результатов. Полный анализ - 4-5 часов. Экспресс метод.
Достаточно широко используется для диагностики инфекционных заболеваний, возбудителями которых являются не культивируемые или трудно культивируемые организмы. Хламидии, микоплазмы, многие вирусы - гепатита, герпеса. Разработаны тест системы для определения сибирской язвы, туберкулеза.
Рестрикционный анализ - с помощью ферментов молекула ДНК разделяется по определенным последовательностям нуклеоидов и фрагменты анализируются поп составу. Таким образом можно найти уникальные участки.
Биотехнология и генная инженерия
Биотехнология это наука, которая на основе изучения процессов жизнедеятельности живых организмов использует эти биопроцессы, а также сами биологические объекты для промышленно производства продуктов необходимых для человека, для воспроизведения биоэффектов, не проявляющихся в неестественных условиях. В качестве биологических объектов чаще всего используются одноклеточные микроорганизмы, а также клетки, животных и растений. Клетки очень быстро воспроизводятся, что позволяет за короткое время нарастить биомассу продуцента. В настоящее время биосинтез сложных веществ, таких как белки, антибиотики, экономичнее и технологически доступнее чем другие виды сырья.
Биотехнология использует сами клетки как источник целевого продукта а также крупные молекулы, синтезируемые клеткой, ферменты токсины, антитела и первичные и вторичные метаболиты - аминокислоты, витамины,гормоны. Технология получения продуктов микробного и клеточного синтеза сводится к нескольким типовым стадиям - выбор или создание продуктивного штаба. Подбор оптимальной питательной среды, культивирование. Выделение целевого продукта, его очистка, стандартизация, придание лекарственной формы. Генетическая инженерия сводится к созданию необходимый для человека целевой продукции. Полученный целевой ген сшивают с вектором, а вектором может быть плазмиды и встраивают его в клетку реципиента. Реципиент - бактерия - кишечная палочка, дрожжи. Синтезируемые рекомбинантами целевые продукты, выделяют очищают и используют в практике.
Первыми, были созданы инсулин и человеческий интерферон. Эритропоэтин, гормон роста, монокланальные антитела. Вакцина против гепатита Б.
 Бактериофа ги или фа ги (от др. греч. φᾰγω «пожираю») - вирусы, избирательно поражающие бактериальные клетки. Чаще всего бактериофаги размножаются внутри бактерий и вызывают их лизис. Как правило, бактериофаг состоит из белковой оболочки и генетического материала одноцепочечной или двуцепочечной нуклеиновой кислоты(ДНК или, реже, РНК). Общая численность бактериофагов в природе примерно равна общей численности бактерий (1030 – 1032 частиц). Бактериофаги активно участвуют в круговороте химических веществ и энергии, оказывают заметное влияние на эволюцию микробов и бактерий Структура типичного миовируса бактериофага.
Бактериофа ги или фа ги (от др. греч. φᾰγω «пожираю») - вирусы, избирательно поражающие бактериальные клетки. Чаще всего бактериофаги размножаются внутри бактерий и вызывают их лизис. Как правило, бактериофаг состоит из белковой оболочки и генетического материала одноцепочечной или двуцепочечной нуклеиновой кислоты(ДНК или, реже, РНК). Общая численность бактериофагов в природе примерно равна общей численности бактерий (1030 – 1032 частиц). Бактериофаги активно участвуют в круговороте химических веществ и энергии, оказывают заметное влияние на эволюцию микробов и бактерий Структура типичного миовируса бактериофага.
 Строение бактериофагов 1 - головка, 2 - хвост, 3 - нуклеиновая кислота, 4 - капсид, 5 - «воротничок» , 6 - белковый чехол хвоста, 7 - фибрилла хвоста, 8 - шипы, 9 - базальная пластинка
Строение бактериофагов 1 - головка, 2 - хвост, 3 - нуклеиновая кислота, 4 - капсид, 5 - «воротничок» , 6 - белковый чехол хвоста, 7 - фибрилла хвоста, 8 - шипы, 9 - базальная пластинка
 Бактериофаги различаются по химической структуре, типу нуклеиновой кислоты, морфологии и характеру взаимодействия с бактериями. По размеру бактериальные вирусы в сотни и тысячи раз меньше микробных клеток. Типичная фаговая частица (вирион) состоит из головки и хвоста. Длина хвоста обычно в 2- 4 раза больше диаметра головки. В головке содержится генетический материал - одноцепочечная или двуцепочечная РНК или ДНК с ферментом транскриптазой в неактивном состоянии, окружённая белковой или липопротеиновой оболочкой - капсидом, сохраняющим геном вне клетки. Нуклеиновая кислота и капсид вместе составляют нуклеокапсид. Бактериофаги могут иметь икосаэдральный капсид, собранный из множества копий одного или двух специфичных белков. Обычно углы состоят из пентамеров белка, а опора каждой стороны из гексамеров того же или сходного белка. Более того, фаги по форме могут быть сферические, лимоновидные или плеоморфные. Хвост, или отросток, представляет собой белковую трубку - продолжение белковой оболочки головки, в основании хвоста имеется АТФаза, которая регенерирует энергию для инъекции генетического материала. Существуют также бактериофаги с коротким отростком, не имеющие отростка и нитевидные.
Бактериофаги различаются по химической структуре, типу нуклеиновой кислоты, морфологии и характеру взаимодействия с бактериями. По размеру бактериальные вирусы в сотни и тысячи раз меньше микробных клеток. Типичная фаговая частица (вирион) состоит из головки и хвоста. Длина хвоста обычно в 2- 4 раза больше диаметра головки. В головке содержится генетический материал - одноцепочечная или двуцепочечная РНК или ДНК с ферментом транскриптазой в неактивном состоянии, окружённая белковой или липопротеиновой оболочкой - капсидом, сохраняющим геном вне клетки. Нуклеиновая кислота и капсид вместе составляют нуклеокапсид. Бактериофаги могут иметь икосаэдральный капсид, собранный из множества копий одного или двух специфичных белков. Обычно углы состоят из пентамеров белка, а опора каждой стороны из гексамеров того же или сходного белка. Более того, фаги по форме могут быть сферические, лимоновидные или плеоморфные. Хвост, или отросток, представляет собой белковую трубку - продолжение белковой оболочки головки, в основании хвоста имеется АТФаза, которая регенерирует энергию для инъекции генетического материала. Существуют также бактериофаги с коротким отростком, не имеющие отростка и нитевидные.
 Систематика бактериофагов Большое количество выделенных и изученных бактериофагов определяет необходимость их систематизации. Этим занимается Международный комитет по таксономии вирусов (ICTV). В настоящее время, согласно Международной классификации и номенклатуре вирусов, бактериофаги разделяют в зависимости от типа нуклеиновой кислоты и морфологии. На данный момент выделяют девятнадцать семейств. Из них только два РНКсодержащих и только пять семейств имеют оболочку. Из семейств ДНКсодержащих вирусов только два семейства имеют одноцепочечные геномы. У девяти ДНК-содержащих семейств геном представлен кольцевой ДНК, а у других девяти - линейной. Девять семейств специфичны только для бактерий, остальные девять только для архей, а (Tectiviridae) инфицирует как бактерий, так и архей
Систематика бактериофагов Большое количество выделенных и изученных бактериофагов определяет необходимость их систематизации. Этим занимается Международный комитет по таксономии вирусов (ICTV). В настоящее время, согласно Международной классификации и номенклатуре вирусов, бактериофаги разделяют в зависимости от типа нуклеиновой кислоты и морфологии. На данный момент выделяют девятнадцать семейств. Из них только два РНКсодержащих и только пять семейств имеют оболочку. Из семейств ДНКсодержащих вирусов только два семейства имеют одноцепочечные геномы. У девяти ДНК-содержащих семейств геном представлен кольцевой ДНК, а у других девяти - линейной. Девять семейств специфичны только для бактерий, остальные девять только для архей, а (Tectiviridae) инфицирует как бактерий, так и архей

 Взаимодействие бактериофага с бактериальными клетками По характеру взаимодействия бактериофага с бактериальной клеткой различают вирулентные и умеренные фаги. Вирулентные фаги могут только увеличиваться в количестве посредством литического цикла. Процесс взаимодействия вирулентного бактериофага с клеткой складывается из нескольких стадий: адсорбции бактериофага на клетке, проникновения в клетку, биосинтеза компонентов фага и их сборки, выхода бактериофагов из клетки. Первоначально бактериофаги прикрепляются к фагоспецифическим рецепторам на поверхности бактериальной клетки. Хвост фага с помощью ферментов, находящихся на его конце (в основном лизоцима), локально растворяет оболочку клетки, сокращается и содержащаяся в головке ДНК инъецируется в клетку, при этом белковая оболочка бактериофага остаётся снаружи. Инъецированная ДНК вызывает полную перестройку метаболизма клетки: прекращается синтез бактериальной ДНК, РНК и белков. ДНК бактериофага начинает транскрибироваться с помощью собственного фермента транскриптазы, который после попадания в бактериальную клетку активируется. Синтезируются сначала ранние, а затем поздние и. РНК, которые поступают на рибосомы клетки-хозяина, где синтезируются ранние (ДНК-полимеразы, нуклеазы) и поздние (белки капсида и хвостового отростка, ферменты лизоцим, АТФаза и транскриптаза) белки бактериофага. Репликация ДНК бактериофага происходит по полуконсервативному механизму и осуществляется с участием собственных ДНК-полимераз. После синтеза поздних белков и завершения репликации ДНК наступает заключительный процесс - созревание фаговых частиц или соединение фаговой ДНК с белком оболочки и образование зрелых инфекционных фаговых частиц
Взаимодействие бактериофага с бактериальными клетками По характеру взаимодействия бактериофага с бактериальной клеткой различают вирулентные и умеренные фаги. Вирулентные фаги могут только увеличиваться в количестве посредством литического цикла. Процесс взаимодействия вирулентного бактериофага с клеткой складывается из нескольких стадий: адсорбции бактериофага на клетке, проникновения в клетку, биосинтеза компонентов фага и их сборки, выхода бактериофагов из клетки. Первоначально бактериофаги прикрепляются к фагоспецифическим рецепторам на поверхности бактериальной клетки. Хвост фага с помощью ферментов, находящихся на его конце (в основном лизоцима), локально растворяет оболочку клетки, сокращается и содержащаяся в головке ДНК инъецируется в клетку, при этом белковая оболочка бактериофага остаётся снаружи. Инъецированная ДНК вызывает полную перестройку метаболизма клетки: прекращается синтез бактериальной ДНК, РНК и белков. ДНК бактериофага начинает транскрибироваться с помощью собственного фермента транскриптазы, который после попадания в бактериальную клетку активируется. Синтезируются сначала ранние, а затем поздние и. РНК, которые поступают на рибосомы клетки-хозяина, где синтезируются ранние (ДНК-полимеразы, нуклеазы) и поздние (белки капсида и хвостового отростка, ферменты лизоцим, АТФаза и транскриптаза) белки бактериофага. Репликация ДНК бактериофага происходит по полуконсервативному механизму и осуществляется с участием собственных ДНК-полимераз. После синтеза поздних белков и завершения репликации ДНК наступает заключительный процесс - созревание фаговых частиц или соединение фаговой ДНК с белком оболочки и образование зрелых инфекционных фаговых частиц

 Жизненный цикл Умеренные и вирулентные бактериофаги на начальных этапах взаимодействия с бактериальной клеткой имеют одинаковый цикл. Адсорбция бактериофага на фагоспецифических рецепторах клетки. Инъекция фаговой нуклеиновой кислоты в клетку хозяина. Совместная репликация фаговой и бактериальной нуклеиновой кислоты. Деление клетки. Далее бактериофаг может развиваться по двум моделям: лизогенный либо литический путь. Умеренные бактериофаги после деления находятся в состоянии профаза (лизогенный путь) Вирулентные бактериофаги развиваются по литической модели: Нуклеиновая кислота фага направляет синтез ферментов фага, используя для этого белоксинтезирующий аппарат бактерии. Фаг тем или иным способом инактивирует ДНК и РНК хозяина, а ферменты фага совсем расщепляют её; РНК фага «подчиняет» себе клеточный аппарат синтеза белка. Нуклеиновая кислота фага реплицируется и направляет синтез новых белков оболочки. Образуются новые частицы фага в результате спонтанной самосборки белковой оболочки (капсид) вокруг фаговой нуклеиновой кислоты; под контролем РНК фага синтезируется лизоцим. Лизис клетки: клетка лопается под воздействием лизоцима; высвобождается около 200- 1000 новых фагов; фаги инфицируют другие бактерии.
Жизненный цикл Умеренные и вирулентные бактериофаги на начальных этапах взаимодействия с бактериальной клеткой имеют одинаковый цикл. Адсорбция бактериофага на фагоспецифических рецепторах клетки. Инъекция фаговой нуклеиновой кислоты в клетку хозяина. Совместная репликация фаговой и бактериальной нуклеиновой кислоты. Деление клетки. Далее бактериофаг может развиваться по двум моделям: лизогенный либо литический путь. Умеренные бактериофаги после деления находятся в состоянии профаза (лизогенный путь) Вирулентные бактериофаги развиваются по литической модели: Нуклеиновая кислота фага направляет синтез ферментов фага, используя для этого белоксинтезирующий аппарат бактерии. Фаг тем или иным способом инактивирует ДНК и РНК хозяина, а ферменты фага совсем расщепляют её; РНК фага «подчиняет» себе клеточный аппарат синтеза белка. Нуклеиновая кислота фага реплицируется и направляет синтез новых белков оболочки. Образуются новые частицы фага в результате спонтанной самосборки белковой оболочки (капсид) вокруг фаговой нуклеиновой кислоты; под контролем РНК фага синтезируется лизоцим. Лизис клетки: клетка лопается под воздействием лизоцима; высвобождается около 200- 1000 новых фагов; фаги инфицируют другие бактерии.
 Применение В медицине Одной из областей использования бактериофагов является антибактериальная терапия, альтернативная приёму антибиотиков. Например, применяются бактериофаги: стрептококковый, стафилококковый, клебсиеллёзный, дизентерийныйиполив алентный, пиобактериофаг, коли, протейный и колипротейный и другие. В России зарегистрировано и применяется 13 медицинских препаратов на основе фагов. В настоящее время их применяют для лечения бактериальных инфекций, которые не чувствительны к традиционному лечению антибиотиками, особенно в республике Грузия. Обычно, применение бактериофагов сопровождается большим, чем антибиотики, успехом там, где присутствуют биологические мембраны, покрытые полисахаридами, через которые антибиотики обычно не проникают. В настоящее время терапевтическое применение бактериофагов не получило одобрения на Западе, хотя и применяются фаги для уничтожения бактерий, вызывающих пищевые отравления, таких, как листерии. В многолетнем опыте в объёме крупного города и сельской местности доказана необычайно высокая лечебная и профилактическая эффективность дизентерийного бактериофага (П. М. Лернер, 2010). В России терапевтические фаговые препараты делают давно, фагами лечили ещё до антибиотиков. В последние годы фаги широко использовали после наводнений в Крымске и Хабаровске, чтобы предотвратить дизентерию.
Применение В медицине Одной из областей использования бактериофагов является антибактериальная терапия, альтернативная приёму антибиотиков. Например, применяются бактериофаги: стрептококковый, стафилококковый, клебсиеллёзный, дизентерийныйиполив алентный, пиобактериофаг, коли, протейный и колипротейный и другие. В России зарегистрировано и применяется 13 медицинских препаратов на основе фагов. В настоящее время их применяют для лечения бактериальных инфекций, которые не чувствительны к традиционному лечению антибиотиками, особенно в республике Грузия. Обычно, применение бактериофагов сопровождается большим, чем антибиотики, успехом там, где присутствуют биологические мембраны, покрытые полисахаридами, через которые антибиотики обычно не проникают. В настоящее время терапевтическое применение бактериофагов не получило одобрения на Западе, хотя и применяются фаги для уничтожения бактерий, вызывающих пищевые отравления, таких, как листерии. В многолетнем опыте в объёме крупного города и сельской местности доказана необычайно высокая лечебная и профилактическая эффективность дизентерийного бактериофага (П. М. Лернер, 2010). В России терапевтические фаговые препараты делают давно, фагами лечили ещё до антибиотиков. В последние годы фаги широко использовали после наводнений в Крымске и Хабаровске, чтобы предотвратить дизентерию.
 В биологии Бактериофаги применяются в генной инженерии в качестве векторов, переносящих участки ДНК, возможна также естественная передача генов между бактериями посредством некоторых фагов (трансдукция). Фаговые векторы обычно создают на базе умеренного бактериофага λ, содержащего двухцепочечную линейную молекулу ДНК. Левое и правое плечи фага имеют все гены, необходимые для литического цикла (репликации, размножения). Средняя часть генома бактериофага λ (содержит гены, контролирующие лизогению, то есть его интеграцию в ДНК бактериальной клетки) не существенна для его размножения и составляет примерно 25 тысяч пар нуклеотидов. Данная часть может быть заменена на чужеродный фрагмент ДНК. Такие модифицированные фаги проходят литический цикл, но лизогения не происходит. Векторы на основе бактериофага λ используют для клонирования фрагментов ДНК эукариот (то есть более крупных генов) размером до 23 тысяч пар нуклеотидов (т. п. н.). Причём, фаги без вставок - менее 38 т. п. н. или, напротив, со слишком большими вставками - более 52 т. п. н. не развиваются и не поражают бактерии. Поскольку размножение бактериофага возможно только в живых клетках, бактериофаги могут быть использованы для определения жизнеспособности бактерий. Данное направление имеет большие перспективы, поскольку, одним из основных вопросов при разных биотехнологических процессах является определение жизнеспособности используемых культур. С помощью метода электрооптического анализа клеточных суспензий была показана возможность изучения этапов взаимодействия фаг-микробная клетка
В биологии Бактериофаги применяются в генной инженерии в качестве векторов, переносящих участки ДНК, возможна также естественная передача генов между бактериями посредством некоторых фагов (трансдукция). Фаговые векторы обычно создают на базе умеренного бактериофага λ, содержащего двухцепочечную линейную молекулу ДНК. Левое и правое плечи фага имеют все гены, необходимые для литического цикла (репликации, размножения). Средняя часть генома бактериофага λ (содержит гены, контролирующие лизогению, то есть его интеграцию в ДНК бактериальной клетки) не существенна для его размножения и составляет примерно 25 тысяч пар нуклеотидов. Данная часть может быть заменена на чужеродный фрагмент ДНК. Такие модифицированные фаги проходят литический цикл, но лизогения не происходит. Векторы на основе бактериофага λ используют для клонирования фрагментов ДНК эукариот (то есть более крупных генов) размером до 23 тысяч пар нуклеотидов (т. п. н.). Причём, фаги без вставок - менее 38 т. п. н. или, напротив, со слишком большими вставками - более 52 т. п. н. не развиваются и не поражают бактерии. Поскольку размножение бактериофага возможно только в живых клетках, бактериофаги могут быть использованы для определения жизнеспособности бактерий. Данное направление имеет большие перспективы, поскольку, одним из основных вопросов при разных биотехнологических процессах является определение жизнеспособности используемых культур. С помощью метода электрооптического анализа клеточных суспензий была показана возможность изучения этапов взаимодействия фаг-микробная клетка
 А также в ветеринарии для: профилактики и лечения бактериальных заболеваний птиц и животных; лечения гнойно-воспалительных заболеваний слизистых глаз, полости рта; профилактики гнойно-воспалительных осложнений при ожогах, ранениях, операционных вмешательствах; в генной инженерии: для трансдукции - естественной передачи генов между бактериями; как векторы, переносящие участки ДНК; с помощью фагов можно конструировать направленные изменения в геноме хозяйской ДНК; в пищевой промышленности: в массовом порядке фагосодержащими средствами уже обрабатывают готовые к употреблению продукты из мяса и домашней птицы; бактериофаги применяют в производстве продуктов питания из мяса, мяса птицы, сыров, растительной продукции, и пр. ;
А также в ветеринарии для: профилактики и лечения бактериальных заболеваний птиц и животных; лечения гнойно-воспалительных заболеваний слизистых глаз, полости рта; профилактики гнойно-воспалительных осложнений при ожогах, ранениях, операционных вмешательствах; в генной инженерии: для трансдукции - естественной передачи генов между бактериями; как векторы, переносящие участки ДНК; с помощью фагов можно конструировать направленные изменения в геноме хозяйской ДНК; в пищевой промышленности: в массовом порядке фагосодержащими средствами уже обрабатывают готовые к употреблению продукты из мяса и домашней птицы; бактериофаги применяют в производстве продуктов питания из мяса, мяса птицы, сыров, растительной продукции, и пр. ;
 в сельском хозяйстве: распыление фагопрепаратов для защиты растений и урожая от гниения и бактериальных заболеваний; для защиты скота и птицы от инфекций и бактериальных заболеваний; для экологической безопасности: антибактериальная обработка семян и растений; очистка помещений пищеперерабатывающих предприятий; санитарная обработка рабочего пространства и оборудования; профилактика помещений больниц; проведение экологических мероприятий
в сельском хозяйстве: распыление фагопрепаратов для защиты растений и урожая от гниения и бактериальных заболеваний; для защиты скота и птицы от инфекций и бактериальных заболеваний; для экологической безопасности: антибактериальная обработка семян и растений; очистка помещений пищеперерабатывающих предприятий; санитарная обработка рабочего пространства и оборудования; профилактика помещений больниц; проведение экологических мероприятий
 Таким образом, на сегодняшний день бактериофаги пользуются большой популярностью в жизни человека и животных. На предприятиях намечен целый ряд приоритетных направлений разработки и производства лечебнопрофилактических бактериофагов, которые коррелируют с вновь зарождающимися общемировыми тенденциями. Создаются и внедряются новые препараты, для лечения многих заболеваний . Изучением и применением бактериофагов занимаются бактериологи, вирусологи, биохимики, генетики, биофизики, молекулярные биологи, экспериментальные онкологи, специалисты по генной инженерии и биотехнологии
Таким образом, на сегодняшний день бактериофаги пользуются большой популярностью в жизни человека и животных. На предприятиях намечен целый ряд приоритетных направлений разработки и производства лечебнопрофилактических бактериофагов, которые коррелируют с вновь зарождающимися общемировыми тенденциями. Создаются и внедряются новые препараты, для лечения многих заболеваний . Изучением и применением бактериофагов занимаются бактериологи, вирусологи, биохимики, генетики, биофизики, молекулярные биологи, экспериментальные онкологи, специалисты по генной инженерии и биотехнологии