Краткодействащият бета 2 агонист е лекарство. В2-агонисти: роля и място в лечението на бронхиална астма. Странични ефекти на бета-агонисти
За цитиране: Sinopalnikov A.I., Klyachkina I.L. b2-агонисти: роля и място в лечението на бронхиална астма // BC. 2002. № 5. С. 236
Държавен институт за следдипломно медицинско образование на Министерството на отбраната на Руската федерация, Москва
Въведение Терапията на бронхиалната астма (БА) може условно да се раздели на две основни направления. Първата е симптоматична терапия, която бързо и ефективно облекчава бронхоспазма, водещ клиничен симптом на БА. Втората е противовъзпалителната терапия, която допринася за промяна на основния патогенетичен механизъм на заболяването, а именно възпалението на респираторната лигавица (АР).
Централното място сред средствата за симптоматичен контрол на астма, очевидно, заема b 2 -агонисти, които се характеризират с изразена бронходилататорна активност (и бронхопротективно действие) и минимален брой нежелани странични ефекти, когато се използват правилно.
Кратка история b 2 -агонисти Историята на употребата на b-агонисти през 20-ти век е последователното развитие и въвеждане в клиничната практика на лекарства с непрекъснато нарастваща b2-адренергична селективност и нарастваща продължителност на действие.
За първи път симпатикомиметик адреналин (епинефрин) е използван при лечението на пациенти с AD през 1900 г. Първоначално епинефринът се използва широко както в инжекционна форма, така и под формата на инхалации. Въпреки това, недоволството на лекарите от кратката продължителност на действие (1-1,5 часа), голям брой отрицателни странични ефекти на лекарството беше стимул за по-нататъшно търсене на по-„привлекателни“ лекарства.
През 1940 г. се появява изопротеренол - синтетичен катехоламин. Той се разрушава в черния дроб толкова бързо, колкото адреналин (с участието на ензима катехол-о-метилтрансфераза - COMT), поради което се характеризира с кратка продължителност на действие (1-1,5 часа), а метаболитите, образувани в резултат на биотрансформацията на изопротеренол (метоксипреналин) има b-адренергично блокиращо действие. В същото време изопротеренолът е свободен от такива нежелани реакции, присъщи на адреналина, като главоболие, задържане на урина, артериална хипертония и др. Изследването на фармакологичните свойства на изопротеренола доведе до установяване на хетерогенност на адренорецепторите. По отношение на последния адреналинът се оказа универсален директен a-b-агонист, а изопротеренолът - първият краткодействащ неселективен b-агонист.
Първият селективен b 2 -агонист е представен през 1970 г. салбутамол , характеризиращ се с минимална и клинично незначима активност срещу a- и b1-рецепторите. Той с право придоби статута на "златен стандарт" в редица b 2 -агонисти. Салбутамолът е последван от въвеждането в клиничната практика на други b2-агонисти (тербуталин, фенотерол и др.). Тези лекарства се оказаха също толкова ефективни, колкото и бронходилататорите, както и неселективните b-агонисти, тъй като бронходилататорният ефект на симпатикомиметиците се осъществява само чрез b2-адренергичните рецептори. В същото време b 2 -агонистите показват значително по-слабо изразен стимулиращ ефект върху сърцето (батмотропен, дромотропен, хронотропен) в сравнение с b 1 -b 2 -агониста изопротеренол.
Някои разлики в селективността на b2-агонистите нямат сериозно клинично значение. По-високата честота на неблагоприятните сърдечно-съдови ефекти при фенотерол (в сравнение със салбутамол и тербуталин) може да се обясни с по-високата ефективна доза на лекарството и отчасти по-бързата системна абсорбция. Новите лекарства запазват скоростта на действие (начало на ефекта през първите 3-5 минути след инхалация), характерна за всички предишни b-агонисти, със забележимо увеличаване на продължителността на действието им до 4-6 часа (по-малко изразено при тежка астма). Това подобри способността за контролиране на симптомите на астма през деня, но "не спаси" от нощни атаки.
Възможността за перорално приемане на отделни b2-агонисти (салбутамол, тербуталин, формотерол, бамбутерол) до известна степен реши проблема с контролирането на нощните астматични пристъпи. Въпреки това, необходимостта от приемане на значително по-високи дози (почти 20 пъти повече, отколкото при вдишване) допринесе за появата на нежелани реакции, свързани със стимулирането на a- и b1-адренергичните рецептори. Освен това беше разкрита и по-ниска терапевтична ефикасност на тези лекарства.
Появата на пролонгирани инхалаторни b 2 -агонисти - салметерол и формотерол - значително промени възможностите за терапия на БА. За първи път се появи на пазара салметерол - високо селективен b 2 -агонист, показващ продължителност на действие най-малко 12 часа, но с бавно начало на действие. Скоро той се присъедини формотерол , който също е високоселективен b 2 -агонист с 12-часов ефект, но със скорост на развитие на бронходилататорния ефект, подобна на тази на салбутамола. Още в първите години на използване на продължителни b 2 -агонисти беше отбелязано, че те допринасят за намаляване на екзацербациите на БА, намаляване на броя на хоспитализациите, както и намаляване на необходимостта от инхалаторни кортикостероиди (IGCS).
Най-ефективният начин за прилагане на лекарства при AD, включително b 2 -агонисти, е признат за инхалация. Важни предимства на този път са възможността за директно доставяне на лекарства до целевия орган (което до голяма степен осигурява скоростта на действие на бронходилататорите) и минимизирането на нежеланите ефекти. От известните в момента средства за доставяне най-често използваните са дозирани аерозолни инхалатори (MAI), по-рядко дозирани инхалатори (DPI) и пулверизатори. Пероралните b 2 -агонисти под формата на таблетки или сиропи се използват изключително рядко, главно като допълнително средство за чести нощни симптоми на астма или висока нужда от инхалаторни краткодействащи b 2 -агонисти при пациенти, получаващи високи дози ICS (еквивалентни до 1000 mcg беклометазон на ден или повече).
Механизми на действие b 2 -агонисти b 2 -агонистите причиняват бронходилатация предимно в резултат на директно стимулиране на b 2 -адренергичните рецептори на гладките мускули на DP. Доказателство за този механизъм е получено като инвитро(под въздействието на изопротеренола настъпва релаксация на човешките бронхи и сегменти на белодробната тъкан) и in vivo(бърз спад на резистентността на DP след инхалация на бронходилататор).
Стимулирането на b-адренергичните рецептори води до активиране на аденилатциклазата, която образува комплекс с G-протеина (фиг. 1), под влиянието на който се повишава съдържанието на вътреклетъчния цикличен аденозин-3,5-монофосфат (цАМР). Последното води до активиране на специфична киназа (протеин киназа А), която фосфорилира някои вътреклетъчни протеини, което води до намаляване на вътреклетъчната концентрация на калций (активното му „изпомпване“ от клетката в извънклетъчното пространство), инхибиране на хидролизата на фосфоинозитид, инхибиране на киназите на леката верига на миозина и накрая се отварят големи калциево-активирани калиеви канали, причинявайки реполяризация (отпускане) на гладкомускулните клетки и секвестриране на калций в извънклетъчното депо. Трябва да се каже, че b2-агонистите могат да се свържат с калиевите канали и директно да причинят релаксация на гладкомускулните клетки, независимо от повишаването на вътреклетъчната концентрация на сАМР.
Фиг. 1. Молекулярни механизми, участващи в бронходилататиращия ефект на b 2 -агонистите (пояснения в текста). K Ca - голям калциево активиран калиев канал; АТФ - аденозин трифосфат; cAMP - цикличен аденозин-3,5-монофосфат
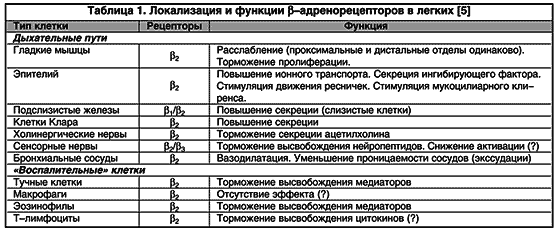
b 2 -агонистите се считат за функционални антагонисти, причиняващи обратното развитие на бронхоконстрикция, независимо от възникналия констрикторен ефект. Това обстоятелство изглежда изключително важно, тъй като много медиатори (медиатори на възпалението и невротрансмитери) имат бронхоконстрикторен ефект.В резултат на въздействието върху b-адренергичните рецептори, локализирани в различни части на DP (Таблица 1), се разкриват допълнителни ефекти на b2-агонисти, което обяснява възможността за профилактична употреба на лекарства. Те включват инхибиране на освобождаването на медиатори от възпалителни клетки, намаляване на пропускливостта на капилярите (предотвратяване на развитието на оток на бронхиалната лигавица), инхибиране на холинергичното предаване (намаляване на холинергичната рефлексна бронхоконстрикция), модулиране на производството на слуз от субмукозните жлези и, следователно, оптимизиране на мукоцилиарния клирънс (фиг. 2).

Ориз. 2. Директен и индиректен бронходилататорен ефект на b 2 -агонисти (пояснения в текста). Е - еозинофил; TK - мастоцит; CN - холинергичен нерв; HmC - гладкомускулна клетка
Според теорията на микрокинетичната дифузия на G. Andersen, продължителността и времето на начало на действие на b 2 -агонистите са свързани с техните физикохимични свойства (предимно липофилност / хидрофилност на молекулата) и характеристиките на механизма на действие. Салбутамол - хидрофилно съединение. Попадайки във водната среда на извънклетъчното пространство, той бързо прониква в "ядрото" на рецептора и след прекратяване на комуникацията с него се отстранява чрез дифузия (фиг. 3). Салметерол , създаден на базата на салбутамол, силно липофилно лекарство, бързо прониква в мембраните на клетките на дихателните пътища, които изпълняват функцията на депо, след което бавно дифундира през рецепторната мембрана, причинявайки неговото продължително активиране и по-късно начало на действие. Липофилност формотерол по-малко от това на салметерол, поради което образува депо в плазмената мембрана, откъдето дифундира в извънклетъчната среда и след това едновременно се свързва с b-адренорецептора и липидите, което определя както скоростта на настъпване на ефекта, така и увеличаването в неговата продължителност (фиг. 3). Дългосрочният ефект на салметерол и формотерол се обяснява с тяхната способност да остават в двуслойната мембрана на гладкомускулните клетки за дълго време в непосредствена близост до b2-адренергичните рецептори и да взаимодействат с тях.

Ориз. 3. Механизъм на действие на b 2 -агонистите (пояснения в текста)
При изследване инвитроспазматичният мускул се отпуска по-бързо с добавянето на формотерол, отколкото на салметерол. Това потвърждава, че салметеролът е частичен β2 рецепторен агонист спрямо формотерола.
Рацемати Селективните b 2 -агонисти са рацемични смеси (50:50) от два оптични изомера - R и S. Установено е, че фармакологичната активност на R-изомерите е 20-100 пъти по-висока от тази на S-изомерите. Доказано е, че R-изомерът на салбутамола проявява бронходилататорни свойства. В същото време S-изомерът проявява директно противоположни свойства: провъзпалителен ефект, повишаване на хиперреактивността на DP, увеличаване на бронхоспазма, освен това се метаболизира много по-бавно. Наскоро беше създадено ново лекарство, съдържащо само R-изомера ( левалбутерол
). Засега съществува само в разтвор за пулверизатори и има по-добър терапевтичен ефект от рацемичния салбутамол, тъй като левалбутерол показва еквивалентен ефект при доза, равна на 25% от рацемичната смес (няма антагонистичен S-изомер и броят на нежеланите реакции са намалени).
Селективност б 2 -агонисти Целта на употребата на селективни b2-агонисти е да се осигури бронходилатация и в същото време да се избегнат нежелани реакции, предизвикани от стимулиране на a- и b1-рецепторите. В повечето случаи умерената употреба на b2-агонисти не води до развитие на нежелани реакции. Селективността обаче не може напълно да елиминира риска от тяхното развитие и има няколко обяснения за това.
На първо място, селективността за b2-адренергичните рецептори винаги е относителна и зависима от дозата. Лекото активиране на a- и b1-адренергичните рецептори, незабележимо при обичайните средни терапевтични дози, става клинично значимо с увеличаване на дозата на лекарството или честотата на неговото приложение през деня. Дозозависимият ефект на b2-агонистите трябва да се вземе предвид при лечението на екзацербации на астма, особено животозастрашаващи състояния, когато многократните инхалации за кратко време (няколко часа) са 5-10 пъти по-високи от допустимата дневна доза .
b2 рецепторите са широко представени в DP (Таблица 1). Тяхната плътност се увеличава с намаляване на диаметъра на бронхите и при пациенти с астма плътността на b 2 рецепторите в дихателните пътища е по-висока, отколкото при здрави хора. Многобройни b2-адренергични рецептори се намират на повърхността на мастоцитите, неутрофилите, еозинофилите и лимфоцитите. И в същото време b 2 -рецепторите се намират в различни тъкани и органи, особено в лявата камера, където те съставляват 14% от всички b-адренергични рецептори, а в дясното предсърдие - 26% от всички b-адренергични рецептори. рецептори. Стимулирането на тези рецептори може да доведе до развитие на нежелани събития, включително тахикардия, предсърдно трептене и миокардна исхемия. Стимулирането на b 2 рецепторите в скелетните мускули може да причини мускулен тремор. Активирането на големи калиеви канали може да допринесе за развитието на хипокалиемия и в резултат на това удължаване на QT интервала и сърдечни аритмии, вкл. фатален. При системно приложение на големи дози лекарства могат да се наблюдават метаболитни ефекти (повишаване на нивото на свободните мастни киселини в кръвния серум, инсулин, глюкоза, пируват и лактат).
Когато се стимулират васкуларните b2-рецептори, се развива вазодилатация и е възможно намаляване на диастолното кръвно налягане. Нежеланите сърдечни ефекти са особено изразени в условия на тежка хипоксия по време на екзацербации на БА - увеличаването на венозното връщане (особено в позицията на ортопнея) може да доведе до развитие на синдрома на Bezold-Jarisch с последващ сърдечен арест.
Връзка между b 2 -агонисти и възпаление в ДП Във връзка с широкото използване на b 2 -агонисти с кратко действие, както и въвеждането в клиничната практика на продължителни инхалаторни b 2 -агонисти, въпросът дали тези лекарства имат противовъзпалителен ефект стана особено актуален. Несъмнено противовъзпалителният ефект на b 2 -агонистите, допринасящ за модификацията на острото възпаление на бронхите, може да се счита за инхибиране на освобождаването на възпалителни медиатори от мастоцитите и намаляване на капилярната пропускливост. В същото време при биопсия на бронхиална лигавица на пациенти с БА, които редовно приемат b 2 -агонисти, се установява, че броят на възпалителните клетки, вкл. и активирани (макрофаги, еозинофили, лимфоцити) не намалява.
В същото време, теоретично, редовният прием на b 2 -агонисти може дори да доведе до влошаване на възпалението в DP. По този начин бронходилатацията, причинена от b2-агонисти, позволява по-дълбоко дишане, което може да доведе до по-масивно излагане на алергени.
В допълнение, редовната употреба на b2-агонисти може да маскира развиващото се обостряне, като по този начин забавя започването или засилването на истинската противовъзпалителна терапия.
Потенциален риск от употреба b 2 -агонисти Толерантност Честата редовна употреба на инхалаторни b 2 -агонисти може да доведе до развитие на толерантност (десенсибилизация) към тях. Натрупването на сАМР допринася за преминаването на рецептора в неактивно състояние. Прекомерно интензивното стимулиране на b-адренергичните рецептори допринася за развитието на десенсибилизация (намаляване на чувствителността на рецепторите в резултат на отделяне на рецептора от G-протеин и аденилатциклаза). Докато се поддържа прекомерна стимулация, броят на рецепторите на клетъчната повърхност намалява („надолу“ регулация). Трябва да се отбележи, че b-рецепторите на гладките мускули на DP имат доста значителен резерв и следователно са по-устойчиви на десенсибилизация от рецепторите на нереспираторните зони (например скелетни мускули или регулиране на метаболизма). Установено е, че здрави индивиди бързо развиват толерантност към високи дози салбутамол, но не и към фенотерол и тербуталин. В същото време при пациенти с БА рядко се проявява толерантност към бронходилататорния ефект на b 2 -агонисти, много по-често се развива толерантност към техния бронхопротективен ефект.
Намаляването на бронхопротективното действие на b 2 -агонистите с тяхната редовна, честа употреба се отнася еднакво както за краткодействащи, така и за продължителни лекарства, дори на фона на основната терапия с инхалаторни кортикостероиди. В същото време не говорим за пълна загуба на бронхопротекция, а за леко намаляване на първоначалното й ниво. H.J. van der Woude et al. установи, че на фона на редовната употреба на формотерол и салметерол от пациенти с астма, бронходилататорният ефект на последния не намалява, бронхопротективният ефект е по-висок при формотерол, но бронходилататорният ефект на салбутамол е много по-слабо изразен.
Десенсибилизацията се развива дълго време, в продължение на няколко дни или седмици, за разлика от тахифилаксията, която се развива много бързо и не е свързана с функционалното състояние на рецепторите. Това обстоятелство обяснява намаляването на ефективността на лечението и изисква ограничаване на честотата на употреба на b 2 -агонисти.
Индивидуалната вариабилност в отговор на b 2 -агонисти и развитието на толерантност към техния бронходилатативен ефект много изследователи свързват с генетичния полиморфизъм на гените. Генът на b2-адренергичния рецептор е локализиран на 5q хромозома. Значително влияние върху хода на БА и ефективността на лечението има промяна в аминокиселинната последователност на b2-адренергичните рецептори, по-специално движението на аминокиселини в кодони 16 и 27. Влиянието на генния полиморфизъм не се простира върху променливостта на бронхопротективния ефект. Честно казано, трябва да се отбележи, че тези данни не се потвърждават във всички произведения.
b 2 -агонисти и смъртност при пациенти с БА
Сериозни съмнения относно безопасността на инхалаторните b-агонисти възникват през 60-те години на ХХ век, когато в редица страни, включително Англия, Австралия, Нова Зеландия, избухва "епидемия от смъртни случаи" сред пациенти с астма. В същото време се предполага, че има връзка между симпатикомиметичната терапия и повишената смъртност от AD. По това време не е установена причинно-следствена връзка между употребата на b-агонисти (изопротеренол) и повишената смъртност и е почти невъзможно да се докажат въз основа на резултатите от ретроспективни проучвания. Доказана е връзката между употребата на фенотерол и увеличаването на смъртността от астма в Нова Зеландия през 80-те години на миналия век, тъй като беше установено, че това лекарство се предписва по-често в случаи на фатална астма, в сравнение с добре контролирано заболяване. Тази връзка беше косвено потвърдена от намаляването на смъртността, което съвпадна с премахването на широкото използване на фенотерол (с общо увеличение на продажбите на други b 2 -агонисти). В тази връзка показателни са резултатите от епидемиологично проучване в Канада, което имаше за цел да проучи възможна връзка между честотата на смъртните случаи и предписаните лекарства. Доказано е, че увеличаването на честотата на смъртните случаи е свързано с терапия с високи дози с който и да е от наличните инхалаторни b2-агонисти. Рискът от фатален изход е най-висок при фенотерол, но когато се поръча в сравнение с еквивалентни дози салбутамол, нивата на смъртност не се различават значително.
В същото време връзката между терапията с високи дози с b 2 -агонисти и увеличаването на смъртността от AD не може да бъде надеждно доказана, тъй като пациентите с по-тежка и лошо контролирана AD са по-склонни да прибягнат до високи дози b 2 - агонисти и, обратно, по-рядко към помощта на ефективни противовъзпалителни лекарства. В допълнение, високите дози b2-агонисти маскират признаците на нарастващо фатално обостряне на БА.
Дозов режим Инхалаторни краткодействащи b2-агонисти Няма съмнение, че инхалаторните краткодействащи b 2 -агонисти са лекарствата на избор за ситуационен симптоматичен контрол на астмата, както и за превенция на развитието на симптоми на индуцирана от физическо натоварване астма (AFA). Редовната употреба на инхалаторни b-агонисти може да доведе до загуба на адекватен контрол върху хода на заболяването. Например в изследване на М.Р. Сиърс и др. в Нова Зеландия са изследвани бронхиална хиперреактивност, сутрешна PSV, ежедневни симптоми и нужда от инхалаторни кортикостероиди при пациенти, използващи b 2 агонисти при поискване, в сравнение с пациенти, използващи фенотерол редовно 4 пъти на ден. В групата пациенти с редовен прием на фенотерол се наблюдава лош контрол на симптомите на астма, освен това има по-чести и тежки екзацербации в сравнение с групата пациенти, използващи b 2 -агонисти "при поискване" в продължение на шест месеца. При последното се наблюдава подобрение на параметрите на функцията на външното дишане, сутрешния PSV, намаляване на отговора на бронхопровокационен тест с метахолин. Увеличаването на бронхиалната хиперреактивност на фона на редовния прием на краткодействащи b2-агонисти най-вероятно се дължи на наличието на S-енантомери в рацемичната смес на лекарството.
По отношение на салбутамол не могат да бъдат установени такива модели, въпреки че, както в случая с фенотерола, редовният му прием е придружен от леко повишаване на бронхиалната хиперреактивност. Има някои доказателства, че редовната употреба на салбутамол е придружена от увеличаване на честотата на епизодите на AFU и увеличаване на тежестта на възпалението в DP.
Краткодействащите b 2 -агонисти трябва да се използват (включително като част от монотерапия) само "при поискване". Малко вероятно е обичайно препоръчваният режим на дозиране на b 2 -агонисти "при поискване" да може да влоши контрола върху хода на астмата, но когато се използват високи дози от лекарството, влошаването на контрола става реално. Освен това, много пациенти стават особено чувствителни към агонисти в присъствието на полиморфизъм на b2-адренергичните рецептори, което води до по-бързо влошаване на контрола. Установената връзка между повишения риск от смърт при пациенти с астма и употребата на високи дози инхалаторни b2-агонисти отразява само тежестта на заболяването. Възможно е също високите дози инхалаторни b2-агонисти да имат вреден ефект върху хода на AD. Пациентите, получаващи високи дози b 2 -агонисти (повече от 1,4 аерозолни кутии на месец), със сигурност се нуждаят от ефективна противовъзпалителна терапия, вкл. и за да се намали дозата на b2-агонистите. При увеличаване на нуждата от бронходилататори (повече от три пъти седмично) е показано допълнително предписване на противовъзпалителни лекарства и при използване на b 2 -агонисти повече от 3-4 пъти на ден за облекчаване на симптомите, увеличаване на тяхната доза е посочена.
Приемането на краткодействащи b 2 -агонисти с цел бронхопротекция също е ограничено до "разумни граници" (не повече от 3-4 пъти на ден). Бронхопротективните свойства на b 2 -агонистите позволяват на много висококвалифицирани спортисти, страдащи от астма, да се състезават на международно ниво (правилата позволяват използването на краткодействащи b 2 -агонисти за профилактика на AFU, при условие че заболяването е медицински потвърдено) . Например, 67 спортисти на AFU участваха в Олимпийските игри през 1984 г. в Лос Анджелис, от които 41 получиха медали с различни деноминации. Известно е, че пероралните b 2 -агонисти повишават ефективността чрез увеличаване на мускулната маса, протеиновия и липидния анаболизъм и психостимулацията. В изследването на C. Goubart и сътр. доказано е, че ефектът на инхалаторните b 2 -агонисти при здрави спортисти е ограничен само до лека бронходилатация, която обаче може значително да допринесе за подобряване на дихателната адаптация в началото на тренировката.
Дългодействащи инхалаторни b2-агонисти
Наличните в момента пролонгирани инхалаторни b 2 -агонисти - формотерол и салметерол имат ефект в рамките на 12 часа с еквивалентен бронходилататорен ефект. Въпреки това, има разлики между тях. На първо място, това е скоростта на формотерол (под формата на DPI), сравнима с времето на начало на действие на салбутамол (под формата на PAI), което позволява използването на формотерол като линейка, вместо краткосрочно действащи b 2 -агонисти. В същото време нежеланите реакции при употребата на формотерол са значително по-малко, отколкото при употребата на салбутамол. Тези лекарства могат да се използват като монотерапия при пациенти с лека астма като бронхопротектори при AFU. При използване на формотерол повече от 2 пъти седмично "при поискване" е необходимо да се добави ICS към лечението.
Трябва да се отбележи, че монотерапията с дългодействащи β2-агонисти на регулярна основа не се препоръчва, тъй като все още няма надеждни доказателства за техните противовъзпалителни, модифициращи заболяването ефекти.
Има научни доказателства за целесъобразността на комбинираното приложение на ИКС и бронходилататори. Кортикостероидите повишават експресията на b 2 рецепторите и намаляват потенциалната десенсибилизация, докато удължените b 2 агонисти повишават чувствителността на кортикостероидните рецептори към ICS.
Проучванията, проведени до момента, показват възможността за по-ранно назначаване на продължителни инхалаторни b 2 -агонисти. Така например при пациенти с неадекватен контрол на астмата, докато приемат 400-800 µg ICS, допълнителното приложение на салметерол осигурява по-пълен и адекватен контрол в сравнение с увеличаване на дозата на ICS. Formoterol показва подобен ефект и в същото време спомага за намаляване на честотата на обострянията на заболяването. Тези и няколко други проучвания предполагат, че добавянето на дългодействащи инхалаторни b2-агонисти към терапията с ниска средна доза ICS при пациенти с неадекватен контрол на астмата е еквивалентно на удвояване на дозата стероиди.
Понастоящем се препоръчва употребата на продължителни инхалаторни b 2 -агонисти само при пациенти, получаващи едновременно ICS. Фиксираните комбинации като салметерол с флутиказон (Seretide) и формотерол с будезонид (Symbicort) изглеждат обещаващи. В същото време се отбелязва по-добро съответствие, рискът от използване само на едно от лекарствата в рамките на дългосрочната терапия на заболяването е изключен.
Литература:1. Национални институти по здравеопазване, Национален институт по сърцето, белите дробове и кръвта. Доклад на експертната група 2: Насоки за диагностика и лечение на астма. Bethesda, Md: Национални институти по здравеопазване, Национален институт за сърцето, белите дробове и кръвта; Април 1997 г. Публикация на NIH 97-4051.
2. Лорънс Д.Р., Бенит П.Н. Клинична фармакология. В 2 тома. Москва: Медицина; 1991 г
3. Машковски М.Д. Лекарства. Москва: Медицина; 1984 г
4. Покажете M. B2-агонисти, от фармакологичните свойства до ежедневната клинична практика. Доклад от международен семинар (въз основа на семинар, проведен в Лондон, Обединеното кралство на 28-29 февруари 2000 г.)
5 Барнс П. Дж. b-агонисти, антихолинергици и други нестероидни лекарства. В: Алберт Р., Спиро С., Джет Дж., редактори. Комплексна респираторна медицина. Великобритания: Harcourt Publishers Limited; 2001.p.34.1-34-10
6. Актуализиране на насоки за астма при възрастни (редакционни). BMJ 2001; 323:1380-1381.
7. Jonson M. b 2 -адренорецепторни агонисти: оптимален фармакологичен профил. В: Ролята на b 2 -агонистите в лечението на астма. Оксфорд: The Medicine Group; 1993.p. 6-8.
8 Барнс П. Дж. бета-адренергичните рецептори и тяхната регулация. Am J Respir Crit Care Med. 1995 г.; 152:838-860.
9. Kume H., Takai A., Tokuno H., Tomita T. Регулиране на Ca 2 + зависимата K+-канална активност в трахеалните миоцити чрез фосфорилиране. Nature 1989; 341:152-154.
10 Anderson G.P. Дългодействащи инхалаторни бета-адренорецепторни агонисти: сравнителна фармакология на формотерол и салметерол. Агенти Действия Suppl. 1993 г.; 43:253-269.
11. Стайлс GL, Тейлър S, Лефковиц RJ. Човешки сърдечни бета-адренергични рецептори: подтипова хетерогенност, очертана чрез директно радиолигандно свързване. наука за живота. 1983 г.; 33:467-473.
12. Преди JG, Cochrane GM, Raper SM, Ali C, Volans GN. Самоотравяне с перорален салбутамол. BMJ. 1981 г.; 282:1932.
13. Handley D. Подобната на астма фармакология и токсикология на (S)-изомери на бета агонисти. J Allergy Clinic Immunol. 1999; 104: S69-S76.
14. Jonson M., Coleman R. Механизми на действие на бета-2-адренорецепторни агонисти. В: Bisse W., Holgate S., редакционни статии. Астма и ринит. Blackwell Science; 1995. p.1278-1308.
15. Burggsaf J., Westendorp R.G.J., in’t Veen J.C.C.M et al. Сърдечно-съдови странични ефекти на инхалаторен салбутамол при пациенти с хипоксична астма. Торакс 2001; 56:567-569.
16. Van Shayck C.P., Bijl-Hoffland I.D., Closterman S.G.M. et al. Потенциален маскиращ ефект върху усещането за диспнея от кратко- и дългодействащи b2-агонисти при астма. ERJ 2002; 19:240-245.
17. Van der Woude H.J., Winter T.N., Aalbers R. Намален бронходилатиращ ефект на салбутамол при облекчаване на индуцирана от метахолин умерена до тежка бронхоконстрикция по време на лечение с висока доза с дългодействащи b2 агонисти. Торакс 2001; 56:529-535.
18. Нелсън Х.С. Клиничен опит с левалбутерол. J Allergy Clinic Immunol. 1999 г.; 104: S77-S84.
19. Lipworth BJ, Hall IP, Tan S, Aziz I, Coutie W. Ефекти на генетичния полиморфизъм върху ex vivo и in vivo функцията на b2-адренорецепторите при пациенти с астма. Гръден кош 1999; 115: 324-328.
20. Lipworth BJ, Kopelman G.H., Wheatley A.P. et al. b 2 -адренорецепторен промоторен полиморфизъм: разширени халотипове и функционални ефекти в мононуклеарните клетки на периферната кръв. Торакс 2002; 57:61-66.
21. Lima JJ, Thomason DB, Mohamed MH, Eberle LV, Self TH, Johnson JA. Влияние на генетичните полиморфизми на b2-адренергичния рецептор върху фармакодинамиката на бронходилататора на албутерол. Clin Pharm Ther 1999; 65:519-525.
22. Kotani Y, Nishimura Y, Maeda H, Yokoyama M. Полиморфизмите на b2-адренергичните рецептори влияят на реакцията на дихателните пътища към салбутамол при астматици. J Астма 1999; 36:583-590.
23. Тейлър Д.Р., Сиърс М.Р., Кокрофт Д.У. Спорът относно бета-агониста. Med Clin North Am 1996; 80:719-748.
24. Spitzer WO, Suissa S, Ernst P, et al. Употребата на бета-агонисти и рискът от смърт и почти смърт от астма. N Engl J Med 1992; 326:501-506.
25. Sears MR, Taylor DR, Print CG, et al. Редовно лечение с инхалаторни бета-агонисти при бронхиална астма. Lancet 1990; 336:1391-1396.
26. Handley D. Подобната на астма фармакология и токсикология на (S)-изомери на бета агонисти. J Allergy Clinic Immunol. 1999 г.; 104: S69-S76.
27. Нелсън Х.С. Клиничен опит с левалбутерол. J Allergy Clin Immunol 1999; 104: S77-S84.
28. Лигет С.Б. Полиморфизми на b2-адренергичния рецептор при астма. Am J Respir Cri. Care Med 1997; 156: S 156-162.
29. Вой Р.О. Опитът на Олимпийския комитет на САЩ с бронхоспазъм, предизвикан от упражнения. Med Sci Exerc 1986; 18:328-330.
30. Lafontan M, Berlan M, Prud'hon M. Les agonistes beta-adrenergiques. Механизми на действие: липомобилизация и анаболизъм. Reprod Nutr Develop 1988; 28:61-84
31. Martineau L, Horan MA, Rothwell NJ, et al. Салбутамол, а b 2 -адренорецепторен агонист, повишава силата на скелетната мускулатура при млади мъже. ClinSci 1992; 83:615-621.
32 Price AH, Clissold SP. Салбутамол през 80-те години. Преоценка на неговата клинична ефикасност. Наркотици 1989; 38:77-122.
33. Goubault C, Perault M-C, Leleu et al. Ефекти на инхалаторния салбутамол при трениращи спортисти без астма Thorax 2001; 56:675-679.
34. Seberova E, Hartman P, Veverka J, et al. Формотеролът, прилаган от Turbuhaler®, има бързо начало на действие като салбутамол, прилаган от pMDI. Програма и резюмета на Международната конференция на Американското торакално общество от 1999 г.; 23-28 април 1999 г.; Сан Диего, Калифорния Резюме A637.
35. Wallin A., Sandstrom T., Soderberg M. et al. Ефектите на редовния инхалаторен формотерол, будезонид и плацебо върху възпаление на лигавицата и клинични показатели на лека астма. Am J Respir Crit Care Med. 1998 г.; 158:79-86.
36. Greening AP, Ind PW, Northfield M, Shaw G. Добавен салметерол спрямо по-висока доза кортикостероид при пациенти с астма със симптоми на съществуващ инхалаторен кортикостероид. Allen & Hanburys Limited UK Study Group. Ланцет. 1994 г.; 334:219-224.
Всяко лекарство принадлежи към определена фармакологична група. Това означава, че някои лекарства имат същия механизъм на действие, показания за употреба и странични ефекти. Една от основните фармакологични групи са бета-агонистите. Тези лекарства се използват широко при лечението на респираторни и сърдечно-съдови патологии.
Какво представляват В-агонистите?
Бета-агонистите са група лекарства, които се използват за лечение на различни заболявания. В тялото те се свързват със специфични рецептори, разположени в гладката мускулатура на бронхите, матката, сърцето и съдовата тъкан. Това взаимодействие предизвиква стимулиране на бета клетките. В резултат на това се активират различни физиологични процеси. Когато B-агонистите се свързват с рецепторите, се стимулира производството на такива биологични вещества като допамин и адреналин. Друго име за тези съединения е бета-агонисти. Техните основни ефекти са повишаване на сърдечната честота, повишаване на кръвното налягане и подобряване на бронхиалната проводимост.

Бета-агонисти: действие в организма
Бета-агонистите се делят на В1- и В2-агонисти. Рецепторите за тези вещества се намират във вътрешните органи. Когато се свържат с тях, бета-агонистите водят до активиране на много процеси в организма. Различават се следните ефекти на В-агонистите:
- Повишен сърдечен автоматизъм и подобрена проводимост.
- Увеличаване на пулса.
- Ускоряване на липолизата. При употребата на B1-агонисти в кръвта се появяват свободни мастни киселини, които са продукти от разграждането на триглицеридите.
- Повишаване на кръвното налягане. Това действие се дължи на стимулиране на системата ренин-ангиотензин-алдостерон (RAAS).
Свързването на адреномиметиците с В1 рецепторите води до изброените промени в организма. Те се намират в сърдечния мускул, кръвоносните съдове, мастната тъкан и бъбречните клетки.

В2 рецепторите се намират в бронхите, матката, скелетните мускули и централната нервна система. Освен това се намират в сърцето и кръвоносните съдове. Бета-2-агонистите предизвикват следните ефекти:
- Подобряване на бронхиалната проводимост. Това действие се дължи на отпускането на гладките мускули.
- Ускоряване на гликогенолизата в мускулите. В резултат на това скелетните мускули се свиват по-бързо и по-силно.
- Релаксация на миометриума.
- Ускоряване на гликогенолизата в чернодробните клетки. Това води до повишаване на нивата на кръвната захар.
- Увеличаването на сърдечната честота.
Какви лекарства принадлежат към групата на В-агонистите?
Лекарите често предписват бета-агонисти. Лекарствата, принадлежащи към тази фармакологична група, се разделят на краткодействащи и бързодействащи лекарства. Освен това се изолират лекарства, които имат селективен ефект само върху определени органи. Някои лекарства действат директно върху В1 и В2 рецепторите. Най-известните лекарства от групата на бета-агонистите са лекарствата Salbutamol, Fenoterol, Dopamine. B-агонистите се използват при лечението на белодробни и сърдечни заболявания. Също така, някои от тях се използват в интензивното отделение (лекарство "Добутамин"). По-рядко лекарствата от тази група се използват в гинекологичната практика.

Класификация на бета-агонисти: видове лекарства
Бета-агонистите са фармакологична група, която включва голям брой лекарства. Поради това те се разделят на няколко групи. Класификацията на В-агонистите включва:
- Неселективни бета-агонисти. Тази група включва лекарства "Орципреналин" и "Изопреналин".
- Селективни В1-агонисти. Използват се в кардиологията и интензивните отделения. Представители на тази група са лекарствата Добутамин и Допамин.
- Селективни бета-2-агонисти. Тази група включва лекарства, използвани при заболявания на дихателната система. От своя страна селективните В2-агонисти се разделят на лекарства с кратко действие и лекарства с дълготраен ефект. Първата група включва лекарства "Фенотерол", "Тербуталин", "Салбутамол" и "Хексопреналин". Лекарствата с продължително действие са формотерол, салметерол и индакатерол.
Показания за употреба на В-агонисти
Показанията за употребата на B-агонисти зависят от вида на лекарството. Неселективните бета-агонисти в момента практически не се използват. Преди това те са били използвани за лечение на някои видове аритмии, влошаване на сърдечната проводимост и бронхиална астма. Сега лекарите предпочитат да предписват селективни В-агонисти. Предимството им е, че имат много по-малко странични ефекти. В допълнение, селективните лекарства са по-удобни за употреба, тъй като те засягат само определени органи.
Показания за назначаване на B1-агонисти:
- Шок от всякаква етиология.
- Свиване.
- Декомпенсирани сърдечни дефекти.
- Рядко - тежка исхемична болест на сърцето.

B2-агонистите се предписват при бронхиална астма, хронична обструктивна белодробна болест. В повечето случаи тези лекарства се използват под формата на аерозоли. Понякога лекарството "Фенотерол" се използва в гинекологичната практика за забавяне на раждането и предотвратяване на спонтанен аборт. В този случай лекарството се прилага интравенозно.
В какви случаи B-адренергичните агонисти са противопоказани?

В2-агонистите са противопоказани в следните случаи:
- Непоносимост към бета-агонисти.
- Бременност, усложнена от кървене, отлепване на плацентата, заплаха от спонтанен аборт.
- Деца под 2 годишна възраст.
- Възпалителни процеси в миокарда, ритъмни нарушения.
- Диабет.
- Аортна стеноза.
- Артериална хипертония.
- Остра сърдечна недостатъчност.
- тиреотоксикоза.
Лекарство "Салбутамол": инструкции за употреба
Салбутамолът е краткодействащ B2 агонист. Използва се при синдром на бронхиална обструкция. Най-често се използва в аерозоли, 1-2 дози (0,1-0,2 mg). За предпочитане е децата да вдишват през пулверизатор. Има и таблетна форма на лекарството. Дозировката за възрастни е 6-16 mg на ден.
"Салбутамол": цената на лекарството
Лекарството се използва като монотерапия при лека бронхиална астма. Ако пациентът има среден или тежък стадий на заболяването, се използват продължителни лекарства (дългодействащи бета-агонисти). Те са основна терапия при бронхиална астма. За бързо облекчаване на астматичен пристъп се използва лекарството "Салбутамол". Цената на лекарството е от 50 до 160 рубли, в зависимост от производителя и дозата, съдържаща се във флакона.
Групата на бронходилататорите включва симпатикомиметици (бета 2-агонисти), антихолинергици (М-антихолинергици), метилксантини (теофилини).
Бета-2-агонистите се разделят на краткодействащи и дългодействащи препарати според продължителността на действие.
Краткодействащите бета-2-агонисти са най-ефективните бронходилататори за облекчаване на симптоми (хрипове, стягане в гърдите и кашлица) и за лечение на спешни случаи. Те са в състояние бързо да разширят стеснените бронхи. При инхалационна употреба бронходилатиращият ефект настъпва след 5-10 минути. Задайте ги не повече от 4 пъти на ден.
Ефектът от пролонгираните бета-2 агонисти идва по-късно. В тази връзка тези лекарства не са предназначени за облекчаване на пристъпи на бронхоспазъм, но могат да бъдат препоръчани за по-продължителна постоянна терапия за предотвратяване на астматични пристъпи и обостряне на заболяването, а също така са алтернатива на увеличаването на дозите на инхалаторните кортикостероиди. Недостатъкът им е, че пациентите, приемащи тези лекарства, са обречени да носят със себе си през цялото време бързодействащ инхалаторен кортикостероид, в случай че превантивното действие на бета-2 агониста не успее и развият дихателни проблеми. Тези лекарства могат да се използват като допълнителна терапия при умерена до тежка астма. Въпреки това мненията относно целесъобразността на дългосрочната употреба на продължителни симпатикомиметици са доста противоречиви. Някои изследователи смятат, че постоянната употреба на такива лекарства за дълго време може да влоши прогнозата по време на самото заболяване, други се страхуват от по-бързо развитие на тахифилаксия, но това не е недвусмислено и изисква допълнително проучване. симпатикомиметичните лекарства са тяхната висока ефективност и селективност. Страничните ефекти върху сърдечно-съдовата система на такива лекарства са сведени до минимум. Основният недостатък на повечето бета-2-агонисти е кратка продължителност на действие (4-6 часа), изискваща честа употреба през деня и ниска концентрация на лекарството в кръвта през нощта.
Сравнителни характеристики на основните препарати на бета-2-агонисти са представени в таблица 2.
Сравнителна характеристика на основните бета-2-агонисти, използвани при лечението на бронхиална астма.
М-холинолитиците (антихолинергиците) не са лекарства от първа линия при лечението на обостряне на астма, тяхната ефективност при астма е по-ниска от симпатикомиметиците. Антихолинергичните лекарства имат редица ефекти, които затрудняват употребата им: те причиняват сухота на лигавиците на назофаринкса и горните дихателни пътища, намаляват секрецията на бронхиалните жлези и подвижността на ресничките на епитела, т.е. инхибират евакуационна функция на бронхите, увеличаване на броя на сърдечните удари, стимулиране на разширяването на зеницата, зачервяване на кожата. Следователно, при стабилен ход на AD, антихолинергичните лекарства заемат по-скромно място в сравнение с бета-2-агонистите. В Русия най-често срещаното антихолинергично лекарство е ипратропиум бромид (Atrovent®). Предимствата на това лекарство са, че има по-голяма продължителност на действие от симпатикомиметиците, общата продължителност на действието му е приблизително, началото на действието се наблюдава след 5 минути, а пикът на действие настъпва след 1,5 часа.
Основно се използват холинергични лекарства:
С преобладаването на симптомите на бронхит,
С "кашлица астма" (кашлица като еквивалент на астматичен пристъп),
При бронхиална обструкция, провокирана от физическа активност, студ, вдишване на прах, газове;
С бронхообструктивен синдром с тежка бронхорея ("влажна астма"),
При пациенти с БА с противопоказания за назначаване на бета-2-агонисти;
При психогенна астма и хормонални характеристики (предменструална астма, комбинация от астма с тиреотоксикоза), използването на комплекс от антихолинергични и седативни средства има предимство пред бета-2-агонистите;
За нощна астма
При астма, предизвикана от атмосферни замърсители и химически дразнители,
В някои случаи антихолинергиците се използват в комбинация с бета-2-агонисти. Комбинираните лекарства обаче рядко се използват при лечението на БА, т.к лечението със стандартни лекарства, като бета-2 агонисти или ипратропиум бромид, е по-ефективно и позволява селективно дозиране на всяко лекарство. Предимството е, че такава комбинация има синергизъм и намалява риска от странични ефекти на съставните компоненти. Комбинираната терапия също води до по-голям бронходилататорен ефект в сравнение с монотерапията и може значително да увеличи нейната продължителност. Основните комбинирани препарати на ипратропиум с бета-2-агонисти са ипратропиум/фенотерол (Berodual®) и ипратропиум/салбутамол (Combivent®). Тези лекарства се използват главно като част от комплексната терапия на тежки астматични пристъпи - инхалация през пулверизатор.
От метилксантините при лечение на бронхиална астма се използват теофилин и аминофилин.
Поради редица нежелани странични ефекти, които могат да възникнат при предозиране на тези лекарства, е необходимо проследяване на концентрацията на теофилин в кръвта. Аминофилинът (смес от теофилин и етилендиамин, който е 20 пъти по-разтворим от самия теофилин) се прилага интравенозно, много бавно (най-малко 20 минути). Интравенозният аминофилин играе важна роля в облекчаването на тежки астматични пристъпи, които са толерантни към небулизирани форми на бета-2-агонисти. Аминофилин се използва и при пациенти със сърдечна недостатъчност в комбинация с астма или бронхит, с хипертония в белодробната циркулация. В тялото аминофилинът освобождава свободен теофилин.
Съвременните бета-2-адреномиметични лекарства и противовъзпалителни лекарства "натиснаха" теофилиновите лекарства при лечението на астма. Показания за преобладаваща употреба при астма са:
В периода на пристъп на астма под формата на курс на интравенозни капкови инфузии на 5-10 ml 2,4% разтвор заедно с калиеви препарати и (ако е показано) кортикостероиди във физиологичен разтвор;
Индивидуално титрирани формулировки на теофилин (0,1 до 0,5 g) са ефективни за лечение на нощни астматични пристъпи;
При хронична астма употребата на продължителни теофилинови препарати може значително да намали дозата на бета-2-агонистите и да намали тежестта на симптомите на астма.
Можете да се запознаете с анализа на пазара на бронходилататори в доклада на Академията за индустриални пазарни изследвания „Руският пазар на лекарства за лечение на бронхиална астма“.
Академия за индустриални пазарни изследвания
Лекарства
Средства, които стимулират отхрачването
Лекарства с рефлексно действие
Те включват препарати от термопсис, истода, бяла ружа, женско биле, подбел. Когато се приемат перорално, лекарствата от тази група имат умерен дразнещ ефект върху рецепторите на стомаха, което рефлексивно повишава секрецията на слюнчените жлези и лигавичните жлези на бронхите. Действието на тези лекарства е краткотрайно, така че са необходими чести малки дози (на всеки 2-4 часа). От отхрачващите се предписват обилна алкална напитка, настойки и отвари от бяла ружа, термопсис - до 10 пъти на ден. Отхрачващите средства се използват както в периода на обостряне на заболяването, така и в периода на ремисия.
Резорбтивни лекарства: натриев и калиев йодид, натриев бикарбонат и други солни препарати. Те повишават бронхиалната секреция, предизвикват втечняване на бронхиалния секрет и по този начин улесняват експекторацията.
Таблетки и дражета 8, 12, 16 mg. Лекарство във флакон.
сироп. Разтвор за перорално приложение. Възрастните се предписват 8-16 mg 4 пъти на ден.
Таблетки от 8 mg 100 броя в опаковка. Разтвор за перорално приложение. еликсир. Задайте 8-16 mg 4 пъти на ден.
Таблетки от 30 mg 20 броя в опаковка. Капсули ретард 75 mg, 10 и 20 броя в опаковка. Разтвор за перорално приложение от 40 и 100 ml във флакони. Сироп 100 ml във флакони. Обичайната дневна доза от лекарството в таблетки е 60 mg. Приемайте по 1 таблетка 2-3 пъти на ден с храна с малко количество течност. Капсулите с удължено освобождаване (ретард капсули) се предписват 1 сутрин. Разтворът през първите 2-3 дни се предписва по 4 ml 3 пъти на ден, а след това по 2 ml 3 пъти на ден. Лекарството под формата на сироп се препоръчва за възрастни през първите 2-3 дни по 10 ml 3 пъти на ден, а след това по 5 ml 3 пъти на ден.
Таблетки от 30 mg 50 броя в опаковка. Сироп 100 ml във флакони. Задайте 30 mg 2-3 пъти на ден.
Има и голям брой комбинирани лекарства: д-р IOM, бронхолитин, бронхикум и др.
В момента се появи лекарство, което има както противовъзпалителен, така и бронходилататорен ефект. Това лекарство се нарича ереспал (фенспирид). При лечението на Erespalom степента на обструкция на дихателните пътища намалява, количеството отделена храчка намалява, което е свързано както с намаляване на образуването, така и с намаляване на секрецията, т.е. лекарството действа по отношение на намаляване на прекомерното образуване на слуз. Предлага се в таблетки от 80 mg (30 таблетки в опаковка). Лекарството се предписва по 2-3 таблетки на ден.
Аерозолната терапия с фитонциди и антисептици може да се извърши с помощта на ултразвукови инхалатори, които създават хомогенни аерозоли с оптимален размер на частиците, които проникват в периферните части на бронхиалното дърво. Използването на лекарства под формата на аерозоли осигурява тяхната висока локална концентрация и равномерно разпределение на лекарството в бронхиалното дърво. С помощта на аерозоли могат да се вдишват антисептици фурацилин, риванол, хлорофилипт, сок от лук или чесън (разреден с 0,25% разтвор на новокаин в съотношение 1:30), инфузия на ела, кондензат от листа от боровинка, диоксидин. Аерозолната терапия е последвана от постурален дренаж и вибрационен масаж.
По време на периоди на ремисия на хроничен бронхит се предприемат вторични превантивни мерки за предотвратяване на екзацербации. Най-предпочитаният и безопасен начин на приложение на лекарствата е инхалаторният, който обикновено не предизвиква сериозни странични ефекти. При този метод на приложение бронходилататорът навлиза незабавно в бронхите. Има голямо разнообразие от инхалатори, като най-често срещаните са дозираните.
За да се осигури максимално проникване на лекарството в дихателните пътища, е много важно да се използва правилно дозираният инхалатор.
Техниката за използване на инхалатора е следната:
Разклатете инхалатора (за получаване на аерозол с еднакъв размер на частиците); отстранете защитната капачка (много пациенти забравят да направят това); наклонете главата си малко назад (за леко изправяне на горните дихателни пътища и осигуряване на свободния поток на лекарството в бронхите); обърнете инхалатора с главата надолу (мундщукът трябва да е надолу); поемете пълно дъх.
Започвайки да вдишвате, натиснете дъното на инхалатора и вдишайте лекарството дълбоко (направете само едно натискане върху дъното на кутията). Задръжте дъха си за 5-10 секунди (така че лекарството да се утаи на стената на бронхите). Поемете спокойно въздух. Ако е необходимо, повторете манипулацията.
Важно е да се разбере, че въпреки доброто здраве е необходимо редовно лечение. Това се дължи на факта, че прогресията на процеса става неусетно, постепенно, в продължение на много години. Следователно, когато пациентът има изразени промени в благосъстоянието (задух при малко физическо натоварване и в покой), процесът на промени в бронхите вече е значително изразен. Ето защо, за да се спре прогресирането на процеса, е необходимо лечението да започне възможно най-рано, тоест веднага от момента на установяване на диагнозата.
Друг момент, на който бих искал да обърна внимание, е, че лечението на хроничен обструктивен бронхит не е въпрос на временно намаляване на задуха или епизодично курсово лечение с каквото и да е лекарство. Лечението на заболяването е терапия, провеждана редовно в продължение на много месеци и години. Това е единственият начин да се забави прогресията на заболяването и да се поддържа задоволително здравословно състояние и добра физическа активност за дълго време.
Тъй като стесняването на бронхите играе основна роля в развитието и прогресията на хроничния обструктивен бронхит, лекарствата, които разширяват бронхите, се използват главно за трайно лечение на заболяването. Идеалният бронходилататор за лечение на хроничен обструктивен бронхит трябва да отговаря на следните изисквания: висока ефективност; минималния брой и тежест на нежеланите реакции; запазване на ефективността въпреки продължителната употреба.
Днес най-вече на тези изисквания отговарят инхалаторните антихолинергици. Те действат предимно върху големите бронхи. Лекарствата от тази група се характеризират с изразен бронходилататорен ефект и минимален брой странични ефекти. Той включва атровент, тровентол, трувент.
Тези лекарства не предизвикват тремор (треперене), не засягат сърдечно-съдовата система. Лечението с Atrovent обикновено започва с 2 инхалации 4 пъти на ден. Намаляването на бронхиалната обструкция и следователно подобряването на благосъстоянието настъпва не по-рано от 7-10 дни след началото на терапията. Възможно е да се увеличи дозата на лекарството dovdokhov на ден. Лекарствата от тази група се използват за основна дългосрочна бронходилататорна терапия. За предпочитане е да използвате дозиращ инхалатор с спейсър.
Дозиран аерозол. 300 дози по 20 мкг.
Краткодействащи инхалаторни B-2 агонисти
Имат и бронходилататорен ефект. Тези лекарства при хроничен обструктивен бронхит са по-малко ефективни от антихолинергиците. Препаратите от тази група се препоръчват да се използват не повече от 3-4 пъти на ден или като профилактика преди физическа активност. Комбинираната употреба на инхалаторни бета-2-агонисти с кратко действие при пациенти с хроничен обструктивен бронхит е по-ефективна от лечението с бронходилататори от същата група.
Изисква се повишено внимание при употребата на лекарства от групата на бета-2-агонистите при пациенти в напреднала възраст, особено при наличие на сърдечно-съдови заболявания.
Странични ефекти: възможно треперене на ръцете, вътрешно треперене, напрежение, сърцебиене, гадене, повръщане.
Най-често срещаните лекарства от тази група са следните.
Беротек (фенотерол). Дозиран аерозол за инхалация. 300 инхалационни дози от 200 мкг.
Беротек-100 (фенотерол). (Boehringer Ingelheim, Германия). Дозиран аерозол, съдържащ по-ниска доза от лекарството, mcg.
Дозиран аерозол 100 mcg на доза.
Вентолин (салбутамол). Аерозолен инхалатор 100 микрограма на доза.
Има лекарство, което е комбинация от тези две групи лекарства.
Berodual (20 микрограма ипратропиум бромид + 50 микрограма фенотерол). Двата бронходилататора, съдържащи се в Berodual, имат по-силен ефект в комбинация, отколкото всеки от тях поотделно. Ако комбинираното лечение с инхалаторни антихолинергици и бета-2 агонисти с кратко действие е неефективно, Вашият лекар може да Ви препоръча друга група лекарства.
Основният представител на групата на метилксантините е теофилинът. Има по-слаб бронходилататорен ефект в сравнение с инхалаторните антихолинергици и бета-2-агонистите. Въпреки това, в допълнение към бронходилататорното действие, лекарствата от тази група имат редица други свойства: предотвратяват или намаляват умората на дихателните мускули; активират двигателната способност на ресничестия епител; стимулират дишането.
Странични ефекти: дразнене на стомашната лигавица, болка в епигастралната област, гадене, повръщане, диария, възбуда, безсъние, тревожност, главоболие, треперене, сърцебиене, аритмии, понижаване на кръвното налягане.
От лекарствата от групата на теофилина най-голям интерес представляват разширените му форми.
В тази група има голям брой предложени лекарства. Предписват се от лекар. Дозата и режимът на лечение зависят от тежестта на заболяването и някои други индивидуални фактори.
I поколение лекарства (приема се 2 пъти на ден)
Таблетки от 0,3 гр. 50 броя в опаковка.
Бавно запълване Таблетки от 0,1 и 0,2 гр. 100 броя в опаковка.
Капсули ретард от 0,1, 0,2, 0,3 г. 20, 60 и 100 броя в опаковка.
Капсули от 0,125 и 0,25 гр. 40 броя в опаковка.
Таблетки от 0,2 и 0,3 гр. 100 броя в опаковка.
Лекарства от второ поколение (приемат се веднъж дневно)
Капсули ретард от 0,375 и 0,25 г. 20, 50, 100 броя в опаковка.
Друга група лекарства, които могат да бъдат препоръчани като основна терапия, са глюкокортикостероидите. При хроничен обструктивен бронхит те се предписват в случаите, когато обструкцията на дихателните пътища остава тежка и причинява инвалидност въпреки спирането на тютюнопушенето и оптималната бронходилататорна терапия. Обикновено лекарят предписва тези лекарства под формата на таблетки на фона на текущата терапия с бронходилататори. Най-често срещаният от тази група е преднизолон.
Всички горепосочени лекарства са основна терапия, тоест, когато са предписани, те трябва да се приемат редовно за дълго време. Само в този случай можете да разчитате на успеха на терапията. Още веднъж бихме искали да подчертаем необходимостта от спиране на тютюнопушенето като един от факторите, които значително влошават състоянието и ускоряват прогресията на заболяването.
При хроничен бронхит се използват методи за повишаване на неспецифичната резистентност на организма. За тази цел се използват адаптогени - екстракт от елеутерокок по 40 капки 3 пъти на ден, тинктура от женшен по 30 капки 3 пъти на ден, тинктури от аралия, родиола розова, пантокрин в същите дози, сапарал по 0,05 g 3 пъти на ден. Действието на тези лекарства е многостранно: те имат положителен ефект върху функционирането на имунната система, метаболитните процеси, повишават устойчивостта на организма към неблагоприятни влияния на околната среда и влиянието на инфекциозни фактори.
Източник: Енциклопедия на традиционната и алтернативна медицина
Лечение и профилактика
бързо повлияват бронхиалната обструкция, подобрявайки благосъстоянието на пациентите за кратко време. При продължителна употреба на β2-агонисти се развива резистентност към тях, след прекъсване на приема на лекарствата се възстановява бронходилататорният им ефект. Намаляването на ефективността на β2-адренергичните стимуланти и в резултат на това влошаването на бронхиалната проходимост е свързано с десенсибилизация на β2-адренергичните рецептори и намаляване на тяхната плътност поради продължително излагане на агонисти, както и с развитието на "rebound синдром", характеризиращ се с остър бронхоспазъм. "Rebound syndrome" се причинява от блокада на β2-адренергичните рецептори на бронхите от метаболитни продукти и нарушение на дренажната функция на бронхиалното дърво поради развитието на синдрома на "затваряне на белия дроб". Противопоказания за употребата на β2-агонисти при ХОББ са свръхчувствителност към който и да е компонент на лекарството, тахиаритмии, сърдечни дефекти, аортна стеноза, хипертрофична кардиомиопатия, декомпенсиран захарен диабет, тиреотоксикоза, глаукома, заплашващ аборт. Тази група лекарства трябва да се използва с особено внимание при пациенти в напреднала възраст със съпътстващо сърдечно заболяване.
Характеристики на b2-агонисти с кратко (салбутамол, фенотерол) и дълготрайно (формотерол, салметерол) действие.
Инхалатор с отмерена доза 100 mcg/доза за инхалиране zamkg/6-8 h (максимум mg/ден) Diskhalermkg/blistermkg/6-8 h (максимум 1600 mcg/ден Небулизатор 2,5-5,0 mg на всеки 6 часа
Най-честите нежелани реакции са: Тремор Главоболие Възбуда Хипотония Зачервяване Хипокалиемия Тахикардия Световъртеж
Инхалатор с отмерена доза 100 mcg/доза за инхалиране x kg/6-8 часа (максимум mg на ден) Пулверизатор 0,5-1,25 mg на всеки 6 часа
Начало на действие: 5-10 мин. Максимално действие: мин. Продължителност на действие: 3-6 ч.
Мониторинг на страничните ефекти Анализ на симптомите Мониторинг на кръвното налягане Мониторинг на сърдечната честота Мониторинг на електролитите
12 mcg/капсула 12 mcg/12 часа (максимум 48 mcg/ден)
Начало на действие: мин. Продължителност на ефекта: 12 часа
Инхалатор с дозирана доза 25 mcg/доза за инхалация zamkg/12 h (максимум 100 mcg/24 h) Diskhaler 50 mcg/блистер 50 mcg/12 h Diskus 50 mcg/доза за инхалация 50 mcg/12 h
Начало на действие: 10-2 минути Продължителност на действие: 12 часа
добавени към терапията с недостатъчна ефективност на първите две групи лекарства, те намаляват системната белодробна хипертония и увеличават работата на дихателната мускулатура.
Тези лекарства имат изразена противовъзпалителна активност, въпреки че при пациенти с ХОББ тя е много по-слабо изразена, отколкото при пациенти с астма. Кратки (10-14 дни) курсове на системни стероиди се използват за лечение на екзацербации на ХОББ. Продължителната употреба на тези лекарства не се препоръчва поради риск от странични ефекти (миопатия, остеопороза и др.).
Доказано е, че те не повлияват прогресивното намаляване на бронхиалната проходимост при пациенти с ХОББ. Техните високи дози (напр. флутиказон пропионат 1000 mcg/ден) могат да подобрят качеството на живот на пациентите и да намалят честотата на екзацербациите на тежка и изключително тежка ХОББ.
Причините за относителната стероидна резистентност на възпалението на дихателните пътища при ХОББ са обект на интензивни изследвания. Може би това се дължи на факта, че кортикостероидите увеличават продължителността на живота на неутрофилите, като инхибират тяхната апоптоза. Молекулярните механизми, лежащи в основата на глюкокортикоидната резистентност, не са добре разбрани. Има съобщения за намаляване на активността на хистон деацетилазата, която е мишена за стероидите, под въздействието на тютюнопушенето и свободните радикали, което може да намали инхибиторния ефект на глюкокортикоидите върху транскрипцията на "възпалителни" гени и да отслаби техните анти- - възпалителен ефект.
СИНДРОМ И СПЕШНИ РЕСПИРАТОРНИ ЗАБОЛЯВАНИЯ.
5.1 ИЗСЛЕДВАНЕ НА БРОНХИАЛНА АСТМА
Бронхиалната астма е заболяване, основано на хронично алергично възпаление и бронхиална хиперреактивност, клинично проявяващо се с променяща се във времето бронхиална обструкция. Повтарящите се епизоди, натрапчивата непродуктивна кашлица, особено през нощта и/или рано сутрин, са симптоми на често срещана, но променлива обструкция на бронхиалното дърво, частично обратима спонтанно или изчезваща под въздействието на лечението.
Известни са четири механизма на обструкция на дихателните пътища:
Спазъм на гладката мускулатура;
Подуване на лигавицата на дихателните пътища;
Хиперсекреция с образуване на лигавични тапи;
Склероза на бронхиалната стена с дълъг и тежък ход на заболяването.
По този начин БА е хронично, алергично възпаление на дихателните пътища, водещо до бронхиална хиперреактивност, бронхиална обструкция поради бронхоконстрикция, оток на лигавицата и запушване на вискозната секреция, клинично проявени с респираторни симптоми.
Диагностични критерии за БА
Диагнозата БА на доболничния етап се поставя въз основа на оплакванията, анамнезата на заболяването и клиничния преглед.
1. Оплаквания и анамнеза.
Наличието на астматични пристъпи или задух, появата на хрипове, кашлица и тяхното изчезване спонтанно или след употреба на бронходилататори и противовъзпалителни лекарства. Асоцииране на тези симптоми с рискови фактори за астма (вижте рискови фактори за астма). Пациентът или неговите близки имат анамнеза за установена астма или други алергични заболявания.
2. Клиничен преглед.
Принудително положение, участие на спомагателни дихателни мускули в акта на дишане, сухи хрипове, които се чуват от разстояние и / или по време на аускултация над белите дробове.
При наличие (включително на пациента) на пикфлоуметър или спирометър се регистрира значителна бронхиална обструкция - форсиран експираторен обем за 1 секунда (FEV1) или пиков експираторен дебит (PSV) под 80% от правилните или нормални стойности.
Критерии за екзацербация на астма
Обострянето на астмата може да възникне под формата на остра атака или продължително състояние на бронхиална обструкция.
Астматичният пристъп е остро развита и/или прогресивно влошаваща се експираторна диспнея, затруднено и/или хрипове, спазматична кашлица или комбинация от тези симптоми, с рязко намаляване на пиковата скорост на издишване.
Екзацербацията под формата на продължително състояние на бронхиална обструкция се характеризира с продължително (дни, седмици, месеци) затруднено дишане, с клинично изразен синдром на бронхиална обструкция, на фона на който могат да се появят остри атаки на БА с различна тежест.
Екзацербациите на бронхиалната астма са водеща причина за спешни повиквания и хоспитализация на пациенти.
Екзацербацията на астмата се оценява чрез клинични признаци и (ако е наличен пикфлоуметър) чрез функционални респираторни тестове. Екзацербацията по тежест може да бъде лека, умерена, тежка и под формата на астматичен статус.
Таблица 1. Класификация на тежестта на екзацербацията на астмата * .
Рязко намалена, принудителна позиция
Рязко намален или липсващ
Не се променя, понякога възбуда
Възбуда, страх, "паника при дишане"
Объркване на съзнанието, кома
Ограничено, говори отделни фрази
Нормална честота на дишане при будни деца (честота на дишане за минута)
Нормално или ускорено до 30% от нормата
Тежка експираторна диспнея. Повече от 30-50% от нормата
Изразена експираторна диспнея над 50% от нормата
Тахипнея или брадипнея
Участие на спомагателна дихателна мускулатура;
ретракция на югуларната ямка
Не се произнася
Парадоксално торако-абдоминално дишане
Дишане при аускултация
Хрипове, обикновено в края на издишването
Изразени хрипове при вдишване и издишване или мозаечно задържане на дъха
Тежки хрипове или намалена проводимост
Липса на дишане, „мълчалив бял дроб“
Нормална сърдечна честота при будни деца (bpm)
PSV ** (% от нормата или най-добър индивидуален показател)
Честотата на прием на бронходилататори през последните
Не са използвани или са използвани ниски/средни дози. Ефективността е недостатъчна, необходимостта е повишена спрямо индивидуалната норма
Използвани са високи дози.
* - Тежестта на екзацербацията се показва от наличието на поне няколко параметъра
** - PSV - използва се при възрастни и деца над 5 години
***-В момента се определя основно в болницата
Таблица 2. Стандарти за показатели на дихателната функция при деца
Тактиката на доболничната терапия се определя изцяло от тежестта на обострянето на БА, следователно, когато се формулира диагноза от лекар на SS и NMP, е необходимо да се посочи тежестта на обострянето на БА.
Тактиката на лекаря при лечението на пристъп на бронхиална астма има няколко общи принципа:
При преглед лекарят трябва да оцени тежестта на екзацербацията според клиничните данни, да определи PSV (ако е наличен пиков дебиломер).
Ако е възможно, ограничете излагането на причинно значими алергени или отключващи фактори.
Според анамнезата, изяснете предишното лечение:
бронхоспазмолитични лекарства, начин на приложение; доза и честота на назначаване;
време на последния прием на лекарството; дали пациентът получава системни кортикостероиди, в какви дози.
Изключете усложнения (напр. пневмония, ателектаза, пневмоторакс или пневмомедиастинум).
Осигурете спешна помощ в зависимост от тежестта на атаката.
Оценете ефекта от терапията (задух, сърдечна честота, кръвно налягане. Повишаване на PSV> 15%).
Избор на лекарство, доза и начин на приложение
Съвременната грижа за пациенти с обостряне на астма включва използването само на следните групи лекарства:
1. Селективни бета-2-агонисти на краткодействащи адренергични рецептори (салбутамол, фенотерол).
2. Антихолинергици (ипратропиум бромид); тяхното комбинирано лекарство беродуал (фенотерол + ипратропиев бромид).
Селективни краткодействащи бета-2 агонисти.
Тези лекарства, които имат бронхоспазмолитичен ефект, са лекарства от първа линия при лечението на астматични пристъпи.
САЛБУТАМОЛ (вентолин, салбен, вентолин небули и 0,1% разтвор на салгим за небулизаторна терапия) е селективен бета-2 адренорецепторен агонист.
Бронходилататорният ефект на салбутамола настъпва след 4-5 минути. Ефектът на лекарството постепенно се увеличава до максимум за минута. Времето на полуживот е 3-4 часа, а продължителността на действие е 4-5 часа.
Начин на приложение : С помощта на пулверизатор, 2,5 ml небули, съдържащи 2,5 mg салбутамол сулфат във физиологичен разтвор. За инхалация се предписват 1-2 небули (2,5 - 5,0 mg) в неразредена форма. Ако няма подобрение, се извършват повторни инхалации на салбутамол 2,5 mg на всеки 20 минути в продължение на един час. В допълнение, лекарството се използва под формата на PDI (спейсър), спейсър или дисхалер (100 mcg на инхалация на 1-2 вдишвания) или циклохалер (200 mcg на инхалация на 1 вдишване).
ФЕНОТЕРОЛ (Беротек) и Беротек разтвор за небулизаторна терапия е краткодействащ селективен бета-2-агонист. Бронходилататорният ефект настъпва след 3-4 минути и достига максимален ефект след 45 минути. Времето на полуживот е 3-4 часа, а продължителността на действие на фенотерола е 5-6 часа.
Начин на приложение:С помощта на пулверизатор - 0,5-1,5 ml разтвор на фенотерол във физиологичен разтвор за 5-10 минути. Ако няма подобрение, повторете инхалациите на същата доза от лекарството на всеки 20 минути. Деца 0,5-1,0 ml (10-20 капки) за 1 инхалация. Berotek се използва и под формата на PAI (100 mcg за 1-2 вдишвания).
Странични ефекти.При използване на бета-2-агонисти са възможни тремор на ръцете, възбуда, главоболие, компенсаторно повишаване на сърдечната честота, нарушения на сърдечния ритъм, артериална хипертония. Страничните ефекти са по-очаквани при пациенти със заболявания на сърдечно-съдовата система, в по-високи възрастови групи и при деца; при многократна употреба на бронхоспазмолитик, зависи от дозата и начина на приложение на лекарството.
Относителни противопоказаниякъм употребата на инхалаторни бета-2-агонисти - тиреотоксикоза, сърдечни дефекти, тахиаритмия и тежка тахикардия, остра коронарна патология, декомпенсиран захарен диабет, свръхчувствителност към бета-агонисти.
Ipratropium bromide (atrovent) е антихолинергично средство с много ниска (под 10%) бионаличност, което води до добра поносимост на лекарството. Ипратропиум бромид се използва в случай на неефективност на бета-2-агонисти, като допълнително средство за засилване на бронходилататорното им действие, с индивидуална непоносимост към бета-2-агонисти, при пациенти с хроничен бронхит.
Начин на приложение:Инхалация - чрез пулверизатор - 1,0 - 2,0 ml (0,25 - 0,5 mg). Ако е необходимо, повтаряйте всяка минута.С помощта на PDI или спейсър.
БЕРОДУАЛ е комбиниран бронхоспазмолитик, съдържащ два бронходилататора - фенотерол и ипратропиум бромид. Една доза berodual съдържа 0,05 mg фенотерол и 0,02 mg ипратропиев бромид.
Начин на приложение:С помощта на пулверизатор за спиране на атака се вдишва разтвор на berodual 1-4 ml във физиологичен разтвор за 5-10 минути. Ако не настъпи подобрение, повторете инхалацията след 20 минути. Дозата на лекарството се разрежда във физиологичен разтвор. С помощта на DAIVdoh, ако е необходимо, след 5 минути - още 2 дози, последващото вдишване трябва да се извърши не по-рано от 2 часа.
тежко и животозастрашаващо обостряне на астма
облекчаване на астматичен пристъп при пациент с хормонално зависима форма на астма
анамнестични индикации за необходимостта от употреба на глюкокортикоиди за облекчаване на обостряне на астма в миналото.
Странични ефекти:артериална хипертония, възбуда, аритмия, кървене от язва
Противопоказания: Пептична язва на стомаха и дванадесетопръстника, тежка артериална хипертония, бъбречна недостатъчност.
Преднизолонът е дехидрогениран аналог на хидрокортизон и принадлежи към синтетичните глюкокортикостероидни хормони. Полуживотът е 2-4 часа, продължителността на действие е часа. Прилага се парентерално при възрастни в доза най-малко 60 mg, при деца - парентерално или перорално 1-2 mg / kg.
МЕТИЛПРЕДНИЗОЛОН (solumedrol, metipred) Нехалогенирано производно на преднизолон, което има по-силен противовъзпалителен ефект (5 mg преднизолон е еквивалентен на 4 mg метилпреднизолон) и значително по-слаба минералкортикоидна активност.
Лекарството се характеризира с кратък, като преднизолон, полуживот, по-слабо стимулиране на психиката и апетита. За лечение на екзацербации на бронхиална астма се използва като преднизолон, но в по-малки дози (на базата на метилпреднизолон-преднизолон като 4: 5).
Инхалаторните глюкокортикоиди (будезонид) могат да бъдат ефективни. Препоръчително е да използвате инхалаторни глюкокортикоиди чрез пулверизатор.
БУДЕЗОНИД (пулмикорт) - суспензия за пулверизатор в пластмасови контейнери 0,25-0,5 mg (2 ml).
По време на биотрансформацията на будезонид в черния дроб, той образува метаболити с ниска глюкокортикостероидна активност.
Суспензията Pulmicort за пулверизатор може да се разрежда с физиологичен разтвор, както и да се смесва с разтвори на салбутамол и ипратропиев бромид. Дозата за възрастни е 0,5 mg (2 ml), за деца - 0,5 mg (1 ml) два пъти на всеки 30 минути.
EUFILLIN е комбинация от теофилин (80%), който определя фармакодинамиката на лекарството и етилендиамин (20%), който определя неговата разтворимост. Механизмите на бронходилататорното действие на теофилин са добре известни.
При предоставяне на спешна помощ лекарството се прилага интравенозно, докато действието започва незабавно и продължава до 6-7 часа. Теофилинът се характеризира с тясна терапевтична ширина, т.е. Дори при малко предозиране на лекарството могат да се развият нежелани реакции. Полуживот при възрастни. Около 90% от приетото лекарство се метаболизира в черния дроб, метаболитите и непромененото лекарство (7-13%) се екскретират с урината през бъбреците. При юноши и пушачи метаболизмът на теофилин се ускорява, което може да наложи увеличаване на дозата на лекарството и скоростта на инфузия. Чернодробна дисфункция, застойна сърдечна недостатъчност и напреднала възраст, напротив, забавят метаболизма на лекарството, увеличават риска от странични ефекти и налагат намаляване на дозата и намаляване на скоростта на интравенозна инфузия на аминофилин.
Показания за употреба при БА:
облекчаване на астматичен пристъп при липса на инхалаторни средства или като допълнителна терапия при тежко или животозастрашаващо обостряне на астма.
от страна на сърдечно-съдовата система - понижаване на кръвното налягане, сърцебиене, нарушения на сърдечния ритъм, кардиалгия
от стомашно-чревния тракт - гадене, повръщане, диария;
от страна на централната нервна система - главоболие, световъртеж, тремор, конвулсии.
Взаимодействие (вижте Таблица 3)
лекарството е несъвместимо с разтвор на глюкоза.
Доза при деца: 4,5-5 mg/kg интравенозно (в продължение на минути) във физиологичен разтвор.
Целта на терапията с пулверизатор е да достави терапевтична доза от лекарството под формата на аерозол директно в бронхите на пациента и да получи фармакодинамичен отговор за кратък период от време (5-10 минути).
Небулизаторната терапия се извършва с помощта на специално устройство, състоящо се от самия пулверизатор и компресор, който създава поток от частици с размер 2-5 микрона със скорост най-малко 4 l / min.
Думата "небулизатор" идва от латинската дума nebula, което означава мъгла. Небулизаторът е устройство за превръщане на течност в аерозол с особено фини частици, способни да проникнат главно в периферните бронхи. Този процес се осъществява под въздействието на сгъстен въздух през компресор (компресорен пулверизатор) или под въздействието на ултразвук (ултразвуков пулверизатор).
Небулизаторната терапия, създаваща високи концентрации на лекарството в белите дробове, не изисква координиране на вдишването с акта на вдишване, което има значително предимство пред PAI.
Ефективността на инхалациите зависи от дозата на аерозола и се определя от редица фактори:
Количеството произведен аерозол
съотношението на вдишване към издишване
анатомия и геометрия на дихателните пътища
Експерименталните данни показват, че аерозолите с диаметър на частиците 2-5 микрона са оптимални за навлизане в дихателните пътища и съответно се препоръчват за употреба. По-малки частици (под 0,8 микрона) навлизат в алвеолите, където бързо се абсорбират или издишват, без да се задържат в дихателните пътища, без да оказват терапевтичен ефект. По-големи частици (повече от 10 микрона) се утаяват в орофаринкса. Благодарение на небулизаторната терапия се постига по-висок терапевтичен индекс на лекарствените вещества, което определя ефективността и безопасността на лечението.
необходимостта от използване на високи дози лекарства;
насочена доставка на лекарството в дихателните пътища;
ако има усложнения при употребата на конвенционални дози лекарства и честотата на употреба на инхалаторни кортикостероиди и други противовъзпалителни средства е висока;
при деца, особено през първите години от живота;
Тежест на състоянието (липса на ефективно вдъхновение)
няма нужда да координирате дишането с приема на аерозол;
възможността за използване на високи дози от лекарството и получаване на фармакодинамичен отговор за кратък период от време;
· непрекъснато подаване на медицински аерозол с фини частици;
Бързо и значително подобрение на състоянието поради ефективно навлизане в бронхите на лекарственото вещество;
техника на лека инхалация.
Препаратите за небулизаторна терапия се използват в специални контейнери, мъглявини, както и разтвори, произведени в стъклени флакони. Това дава възможност за лесно, правилно и точно дозиране на лекарството.
За инхалация през пулверизатор трябва:
излейте течността от мъглявината или накапете разтвора от флакона (единична доза от лекарството);
Добавете физиологичен разтвор до необходимия обем от 2-3 ml (съгласно инструкциите за пулверизатора;
прикрепете мундщука или маската за лице;
Включете компресора, свържете пулверизатора и компресора;
Извършете инхалация, докато разтворът се изразходва напълно;
При деца предпочитание се дава на вдишване през устата с помощта на мундщук;
При деца от първите години от живота може да се използва плътно прилепваща маска.
Първичната дезинфекция на пулверизатора се извършва в подстанцията. За тази цел е необходимо да разглобите пулверизатора, да изплакнете дюзите с топла вода и препарат и да ги изсушите (не можете да използвате четка). След това пулверизаторът и дюзите се стерилизират в автоклав при 120°C и 1,1 атмосфера (OST5).
Веднъж годишно се извършва технически преглед на пулверизаторите.
Таблица 3. Лечение на екзацербация на астма в доболничния етап
ventolin 2,5 mg (1 мъглявина) или salgim 2,5 mg (1/2 бутилка) през пулверизатор за 5-10 минути;
berodual 1-2 ml (20-40 капки) през пулверизатор за 5-10 минути;
.
ventolin 1,25-2,5 mg (1/2-1 мъглявина) през пулверизатор за 5-10 минути или salgim 1,25-2,5 mg (1/4-1/2 флакон).
berodual 0,5 ml - 10 капки. (деца под 6 години) и 1 ml - 20 капки (деца над 6 години) през пулверизатор за 5-10 минути;
Оценете терапията след 20 минути
без ефект, повторете подобна инхалация на бронходилататор.
ventolin 2,5-5,0 mg (1-2 небули) или salgim 2,5-5,0 (1/2-1 флакон) mg през пулверизатор за 5-10 минути
berodual 1-3 ml (20-60 капки) през пулверизатор за 5-10 минути;
орален преднизолон, IV 60-90 mg или метилпреднизолон IV; или пулмикорт през пулверизатор MGK (1-2 небули) за 5-10 минути
Оценете терапията след 20 минути
Ако ефектът е незадоволителен, повторете подобна инхалация на бронходилататор
ventolin 2,5 mg (1 мъглявина) през пулверизатор за 5-10 минути или salgim (1/2 флакон)
berodual 0,5 ml - 10 капки. при деца под 6 години и 1 ml - 20 капки (при деца над 6 години) през пулверизатор за 5-10 минути;
преднизолон - перорално; IV 1 mg/kg
pulmicort (1/2-1 nebulamkg) през пулверизатор за 5-10 минути;
Оценете терапията след 20 минути
Ако ефектът е незадоволителен, повторете подобна инхалация на бронходилататор
Хоспитализация за деца
вентолин, салгим или беродуал в същите дози и орален преднизолон, интрамускулно mg (или интравенозно метилпреднизолон и пулмикорт през пулверизатор mcg 1-2 небули за 5-10 минути.
Ventolin или salgim или berodual в същите дози и преднизолон за деца - i.vmg или перорално 1-2 mg/kg
pulmicort през пулверизатор 000 mcg за 5-10 минути.
Хоспитализация в болница
вентолин, салгим или беродуал в същите дози и интравенозен преднизолон (или интравенозен метилпреднизолон и пулмикорт през пулверизатор μg 1-2 небули за 5-10 минути;
При неефективност, трахеална интубация, механична вентилация
вентолин или салгим или беродуал в същите дози и преднизолон за деца - най-малко mg IV или 1-2 mg/kg перорално
pulmicort през пулверизатор за 5-10 минути;
Трахеална интубация, IVL
2. Хоспитализация в интензивно отделение
* При неефективност на терапията за тежка степен на обостряне и заплаха от спиране на дишането е възможно да се прилага адреналин на възрастни 0,1% - 0,5 ml подкожно. Деца 0,01 ml/kg, но не повече от 0,3 ml
** При липса на пулверизатори или при постоянно искане на пациента е възможно да се приложи 2,4% разтвор на аминофилин от 10,0-20,0 ml интравенозно за 10 минути.
*** Животозастрашаващи признаци: цианоза, мълчалив бял дроб, отслабване на дишането, обща слабост, при по-големи деца PSV е под 33%. В този случай незабавна хоспитализация, използване на бета-2 агонисти в необходимата доза и честота, перорален преднизолон, кислородна терапия
Критерии за ефективност на лечението:
1. „Добър“ се счита за отговор на продължаващата терапия, ако:
състоянието е стабилно, задухът и броят на сухите хрипове в белите дробове са намалели; PSV
се увеличава с 60 l / min, при деца - с 12-15% от оригинала.
2. „Непълен“ отговор на текущата терапия се счита, ако:
състоянието е нестабилно, симптомите са същите, области с
лошо провеждане на дишането, без повишаване на PSV.
3. „Лош“ е отговорът на продължаващата терапия, ако:
симптоми на предишната степен или увеличаване, PSV се влошава.
Таблица 4. За лечение на бронхиална астма
респираторна депресия поради действието на централния мускулен релаксант
потискане на дихателния център
Антихистамини от 1-во поколение
влошава бронхиалната обструкция чрез увеличаване на вискозитета на храчките, афинитетът на дифенхидрамин към H1-хистаминовите рецептори е значително по-нисък от този на самия хистамин, хистаминът, който вече се е свързал с рецепторите, не се измества, но има само превантивен ефект, хистаминът не играят водеща роля в патогенезата на пристъп на бронхиална астма.
Ефектът не е доказан, показана е само адекватна рехидратация, за да се попълнят загубите на течности с пот или поради повишена диуреза след употреба на аминофилин
Нестероидни противовъзпалителни лекарства (аспирин)
противопоказан при "аспиринова" астма, риск от непоносимост към аспирин
ЧЕСТИ ГРЕШКИ В ТЕРАПИЯТА.
При екзацербация на астма е нежелателно използването на неселективни бета-агонисти като ипрадол и асмапент поради високия риск от странични ефекти. За лечение на бронхиална обструкция традиционно използваните антихистамини (дифенхидрамин и др.) Са неефективни, тъй като техният афинитет към Н1-хистаминовите рецептори е много по-нисък от този на самия хистамин и те не изместват хистамин, който вече е свързан с рецепторите. Освен това хистаминът не играе водеща роля в патогенезата на астматичния пристъп. Употребата на адреналин, макар и ефективна, е изпълнена със сериозни странични ефекти. Понастоящем, когато има голям избор от селективни агонисти, употребата на епинефрин е оправдана само за лечение на анафилаксия. Използването на коргликон е неразумно поради неефективност при деснокамерна недостатъчност. Комбинацията от коргликон с еуфилин повишава риска от развитие на дигиталисови аритмии (включително камерни аритмии). Освен това няма връзка между дозата и ефекта на сърдечните гликозиди върху активността на синусовия възел, така че ефектът им върху сърдечната честота при синусовия ритъм е непредсказуем.
Според съвременните концепции хидратацията с въвеждането на големи количества течност е неефективна (само рехидратацията е показана за попълване на загубите на течност чрез пот или поради повишена диуреза след употребата на аминофилин).
Използването на наркотични аналгетици е абсолютно неприемливо поради заплахата от потискане на дихателния център. Употребата на атропин също не се препоръчва поради възможно нарушение на дренажната функция на бронхите поради инхибиране на мукоцилиарната система и повишаване на вискозитета на секрета в бронхите.
Магнезиевият сулфат има определени бронходилататорни свойства, но употребата му като средство за облекчаване на астматични пристъпи не се препоръчва.
Астматичният пристъп често е придружен от тежки емоционални разстройства (страх от смъртта и др.), Но употребата на транквиланти, които потискат дишането поради централно мускулно релаксиращо действие, е противопоказано.
И накрая, погрешна тактика е използването на аминофилин след адекватна инхалационна терапия с бета-2-агонисти, както и многократни интравенозни инжекции (особено при пациенти, получаващи продължителни теофилини) - рискът от странични ефекти (тахикардия, аритмия) от такова лечение надвишава ползата от приложението на аминофилин. Късното прилагане на глюкокортикоиди (често в неадекватни дози) в тази ситуация може да се дължи на преувеличен страх от тяхната употреба.
ПОКАЗАНИЯ ЗА ХОСПИТАЛИЗАЦИЯ:
Хоспитализацията е показана за пациенти с тежко обостряне на астма и заплаха от спиране на дишането; при липса на бърз отговор на бронходилататорна терапия или при по-нататъшно влошаване на състоянието на пациента на фона на започнатото лечение; при продължителна употреба или наскоро преустановени системни кортикостероиди. Също така пациентите, които са били хоспитализирани в интензивното отделение няколко пъти през последната година, трябва да бъдат изпратени в болницата; пациенти, които не се придържат към план за лечение на астма и пациенти, страдащи от психични заболявания.
Клиничен пример за ефективността на небулизаторната терапия .
Пневмония (P) е остро инфекциозно заболяване с предимно бактериална етиология, характеризиращо се с фокални лезии на респираторните отдели на белите дробове с интраалвеоларна ексудация, открити по време на физикален и / или рентгенов преглед и изразени в различна степен на фебрилна реакция и интоксикация.
ЕТИОЛОГИЯ И ПАТОГЕНЕЗА .
P са причинени от инфекциозен агент. Най-често срещаните са пневмококи, грипен бацил, стрептококи, стафилококи, микоплазми и хламидии. Широко разпространената и не винаги оправдана употреба на антибиотици, особено широкоспектърни антибиотици, доведе до селекция на резистентни щамове и развитие на антибиотична резистентност. Вирусите също са способни да причинят възпалителни промени в белите дробове, засягащи трахеобронхиалното дърво, създавайки условия за проникване на пневмотропни бактериални агенти в респираторните отдели на белите дробове.
Основният път на заразяване е въздушно-капковият път на проникване на патогени или аспирация на секрети, съдържащи микроорганизми, от горните дихателни пътища.
По-рядко срещан е хематогенният път на разпространение на патогени (ендокардит на трикуспидалната клапа, септичен тромбофлебит на тазовите вени) и директното разпространение на инфекция от съседни тъкани (чернодробен абсцес) или инфекция с проникващи рани на гръдния кош.
КЛИНИЧНА КАРТИНА И КЛАСИФИКАЦИЯ.
В зависимост от условията на възникване, клиничното протичане, състоянието на имунологичната реактивност на пациента се разграничават следните видове P:
Амбулаторно (домашен, извънболничен)
Болница (нозокомиална, нозокомиална)
На фона на имунодефицитни състояния
Тази класификация се използва за оправдаване на емпиричната терапия. Детайлизирането на P, като се вземат предвид рисковите фактори (хронична алкохолна интоксикация, на фона на ХОББ, вирусни инфекции, злокачествени и системни заболявания, хронична бъбречна недостатъчност, предишна антибиотична терапия и др., Ви позволява да вземете предвид целия набор от възможни патогени и повишава насочеността на започване на антибиотична терапия
Клиничната картина на P се определя както от характеристиките на патогена, така и от състоянието на пациента и се състои от извънбелодробни симптоми и признаци на увреждане на белите дробове и бронхите.
1) Бронхопулмонални: кашлица, задух, болка в гърдите, храчки, понякога хемоптиза, тъпота на перкуторния звук, отслабване на везикуларното или бронхиално дишане, крепитус, шум от плеврално триене;
2) Извънбелодробни: хипотония, слабост, тахикардия, изпотяване, втрисане, треска, объркване, остра психоза, менингеални симптоми, декомпенсация на хронично заболяване
При пациенти с хронична алкохолна интоксикация или тежки съпътстващи заболявания (захарен диабет, застойна сърдечна недостатъчност, мозъчен инфаркт и др.) или при пациенти в напреднала възраст извънбелодробните симптоми могат да преобладават над бронхопулмоналните.
Когато P е локализиран в долните части на белите дробове и когато диафрагмалната плевра е включена в процеса (с крупозна пневмония - плевропневмония), болката може да се излъчва в коремната кухина, симулирайки картина на остър корем.
Плевропневмонията в някои случаи трябва да се диференцира от белодробен инфаркт, който също се характеризира с внезапна поява на болка, често хемоптиза, задушаване. Но в началото на заболяването наличието на висока температура и интоксикация не са патогномонични. При тези пациенти е възможно да се идентифицират възможните източници на тромбоемболизъм (тромбофлебит на долните крайници, сърдечни заболявания, постинфарктна кардиосклероза). При регистриране на ЕКГ се откриват симптоми на претоварване на дясното сърце (блокада на десния крак на снопа His, знак S I -Q III.).
При спонтанен пневмоторакс острото развитие на синдрома на болката може да се комбинира с нарастваща дихателна недостатъчност (напрегнат спонтанен пневмоторакс). Перкусията разкрива тимпанит, отслабване на дишането, понякога увеличаване на обема и ограничаване на дихателните екскурзии на съответната половина на гръдния кош.
Усложненията на P са плеврит, образуване на абсцес, пиопневмоторакс и плеврален емпием, синдром на респираторен дистрес при възрастни, инфекциозно-токсичен шок, бронхообструктивен синдром, съдова недостатъчност. При тежки случаи с тежка интоксикация, изтощените пациенти могат да развият сепсис, инфекциозен ендокардит, увреждане на миокарда и бъбреците.
Лобарната пневмония, задължително свързана с пневмококова инфекция, е една от най-тежките форми на P. Характеризира се с: остро начало на заболяването със силно втрисане, кашлица, болка в гърдите при дишане, ръждиви храчки, отчетливи перкуторни и аускултаторни промени в белите дробове, критично падане на телесната температура; възможно развитие на хипотония, остра съдова недостатъчност, респираторен дистрес - синдром на възрастни, инфекциозно-токсичен шок.
При стафилококови Р, които са по-чести по време на грипна епидемия, се развива тежка интоксикация и гнойни усложнения.
При възрастни хора и при хора с алкохолна зависимост те често се причиняват от грам-отрицателна флора, по-специално Klebsiella pneumoniae. При тези P има обширно увреждане на белодробната тъкан с разрушаване, гнойни усложнения и интоксикация.
СПИСЪК С ВЪПРОСИ КЪМ ПАЦИЕНТ С ПНЕВМОНИЯ.
1) Време на поява на заболяването.
2) Наличието на рискови фактори, които влошават хода на P
Хронични заболявания, лоши навици и др.
3) Изясняване на епидемиологичната анамнеза.
Идентифициране на признаци на възможно инфекциозно заболяване.
4) Продължителността и характера на повишаването на температурата.
5) Наличието на кашлица, храчки, нейната природа, хемоптиза.
6) Наличието на болка в гърдите, връзката й с дишането, кашлицата
7) Има ли задух, астматични пристъпи
ДИАГНОСТИЧНИ КРИТЕРИИ ЗА ПНЕВМОНИЯ.
1. Оплаквания на пациента от кашлица, храчки, болки в гърдите, задух
2. Остро начало на заболяването
3. Промени в перкусията (тъпота на перкуторния звук) и аускултацията (отслабване на везикуларното дишане, бронхиално дишане, крепитус, шум от плеврално триене) на белите дробове, прояви на бронхиална обструкция
4. Повишаване на температурата
5. Симптоми на интоксикация
При изследване на пациент е необходимо да се измери температурата, дихателната честота, кръвното налягане, сърдечната честота; за палпиране на корема, за идентифициране на симптоми на декомпенсация на съпътстващи заболявания.
Ако подозирате AMI, PE, в напреднала възраст, със съпътстваща атеросклероза, е необходимо да се проведе ЕКГ изследване.
Откриването на пневмонична инфилтрация по време на радиографско изследване потвърждава диагнозата P.
Лабораторните данни (анализ на периферна кръв, биохимични изследвания), определянето на газовия състав на кръвта са важни за оценка на тежестта на състоянието на пациента и избор на терапия.
Цитологичното изследване на храчките ви позволява да изясните естеството на възпалителния процес и неговата тежест.
Бактериологичното изследване на храчки, бронхиално съдържимо, кръв е важно за корекция на антибиотичната терапия, особено при тежка форма на P.
Клиничен пример. Пациент В., 44 г., се обажда на екипа на СС и НМП поради внезапна поява на втрисане, температура до 38,5, остри болки в дясната страна, усилващи се при дишане и движение. История на злоупотреба с алкохол.
Той е хоспитализиран с диагноза остър холецистит. При преглед в спешното отделение се изключва хирургична патология, но се установява притъпяване на перкуторния звук вдясно в долните части на белите дробове, както и учестено дишане и бронхофония. Лекарят в спешното отделение се съмнява за пневмония. Рентгеновото изследване потвърди диагнозата пространна плевропневмония на долния лоб. Така, в този случай, при пациент с дясна плевропневмония, плевралната болка се разпространява в десния хипохондриум и имитира картината на остър холецистит.
За лекаря на LUTS разделянето на P според тежестта е от голямо значение, което позволява да се идентифицират пациенти, които се нуждаят от хоспитализация и интензивно лечение в предболничния етап. Основните клинични критерии за тежестта на заболяването са степента на дихателна недостатъчност, тежестта на интоксикацията, наличието на усложнения, декомпенсацията на съпътстващи заболявания.
Критерии за тежка пневмония (Niederman et al., 1993).
1. NPV > 30 на минута.
2. Температура над 38,5 С
3. Извънбелодробни огнища на инфекция
4. Нарушение на съзнанието
5. Необходимост от механична вентилация
6. Състояние на шок (SBP под 90 mmHg или DBP под 60 mmHg)
7. Необходимостта от използване на вазопресори за повече от 4 часа.
8. Диуреза< 20 мл/ч или проявления острой почечной недостаточности.
На хоспитализация подлежат и пациенти с рискови фактори за усложнения и смърт.
Рискови фактори, които увеличават вероятността от усложнения и смъртност от пневмония (Niederman et al., 1993).
1. Хронична обструктивна белодробна болест
2. Диабет
3. Хронична бъбречна недостатъчност
4. Левокамерна сърдечна недостатъчност
5. Хронична чернодробна недостатъчност
6. Хоспитализации през предходната година.
7. Нарушение на преглъщането
8. Нарушение на висшите нервни функции
12. Възраст над 65 години
На хоспитализация подлежат пациенти с умерена и тежка П, с усложнен ход, при наличие на рискови фактори. Някои пациенти в предболничния стадий могат да развият симптоми, които изискват корекция от LUTS лекаря.
АЛГОРИТЪМ НА ТАКТИКАТА НА ДОКТОР ЛУТС ПРИ ПНЕВМОНИЯ
Артериална хипотонияпри пациенти с крупозен P (плевропневмония) възниква поради генерализирано намаляване на тонуса на гладките мускули на стените на артериолите и малките артерии и намаляване на общото периферно съпротивление. Според някои автори причината за това е незабавният отговор на съдовата стена по време на анафилактична реакция на сенсибилизиран организъм към пневмококови разпадни продукти, които в този случай действат не като токсини, а като антигени. Не трябва да започвате антибиотична терапия преди хоспитализация, да предписвате антипиретични или аналгетични лекарства, тъй като това може да доведе до спад на кръвното налягане, което е особено опасно при транспортиране на пациента.
За да се осигури поддържане на SBP на ниво от 100 mm Hg. въвеждат се течности (в / в капкови изотонични разтвори на натриев хлорид, декстроза, декстран 40 в общ обем от 0 ml).
Остра респираторна недостатъчност - синдром на респираторен дистрес при възрастни (ARDS). ARDS се развива по-често със сепсис, бактериален шок, при пациенти с P на фона на имунодефицит (хронична алкохолна интоксикация, неутропения, наркомания, HIV инфекция). В отговор на инфекцията се развива локална възпалителна реакция, водеща до вазодилатация, повишаване на пропускливостта на съдовата стена, освобождаване на редица клетъчни компоненти (лизозомни ензими, вазоактивни амини, простагландини) и се активира системата на комплемента, привличане на неутрофили в белодробната микроциркулация. Гранулоцитите и мононуклеарните клетки се натрупват на мястото на нараняване и образуват конгломерат с локални фибробласти и ендотелни клетки. Адхезията на неутрофилите към ендотела стимулира освобождаването на увреждащи токсични вещества. В резултат на увреждане на ендотела на белодробните капиляри се развива белодробен оток, клинично изявен с тежък задух и тежка хипоксемия, резистентна на кислородотерапия, което предизвиква повишена нужда от кислород. Пациентите се нуждаят от IVL. Диуретиците са неефективни при белодробен оток при пациенти с ARDS. Въвеждането на фуроземид в / в може да подобри обмяната на газ, без да намалява степента на белодробен оток, което може да се дължи на преразпределението на белодробния кръвен поток (увеличаването му в добре вентилирани зони на белите дробове).
Основната цел на терапията при лечението на дихателна недостатъчност е поддържане на оксигенацията на тъканите. При ARDS консумацията на кислород в периферията е право пропорционална на доставянето му. При артериална хипотония и намаляване на сърдечния дебит е показана интравенозна инфузия на добутамин в дози kg/kg min.
Периферните вазодилататори влошават белодробната хипоксемия чрез увеличаване на интрапулмонарния шунт. Насищането на артериалния хемоглобин с кислород се поддържа над 90%, което е достатъчно за поддържане на доставката на кислород до периферните тъкани. Понастоящем не се счита за доказано, че употребата на глюкокортикостероиди във високи дози отслабва възпалителния процес в белите дробове. В същото време високите дози глюкокортикостероиди увеличават риска от развитие на вторична инфекция.
Инфекциозно-токсичен шокможе да усложни хода на крупозна (плевропневмония), стафилококова П., възниква при П., причинена от грам-отрицателна флора и при пациенти с рискови фактори. Лечението на предболничния етап се състои от инфузионна терапия, въвеждане на добутамин. За повече подробности вижте съответния раздел.
Бронхообструктивен синдром- вижте съответния раздел.
Плеврална болкапонякога изразени толкова силно, че изискват въвеждането на аналгетици. Най-рационалното използване на лекарства от групата на НСПВС (парацетамол 0,5 g per os, ибупрофен - 0,2 g per os; аспирин 0,5 - 1,0 g per os или парентерално под формата на лизин моноацетилсалицилат 2,0 g; диклофенак - 0,075 g per os или парентерално IM дълбоко в глутеалния мускул 0,075 g). Аналгинът, който все още се използва широко като аналгетик, причинява сериозни нежелани реакции (остра анафилаксия, потискане на хемопоезата) много по-често и поради това не може да се препоръчва за употреба.
При пациенти с крупозен P (плевропневмония) приемането на аналгетици може да предизвика хипотония и е по-добре да се въздържат от употребата им на предболничния етап.
ПАРАЦЕТАМОЛ. Максималната концентрация в кръвта се достига след 0,5-2 часа след приложението, продължителността на действие е 3-4 часа.
Показания за употреба са лека до умерена болка, температура над 38 С.
При заболявания на черния дроб и бъбреците, хронична алкохолна интоксикация, лекарството трябва да се използва с повишено внимание.
Противопоказанията са реакции на свръхчувствителност към лекарството в историята.
Нежелани реакции (рядко се развиват): кожен обрив, цитопения, чернодробно увреждане (по-рядко - бъбречно увреждане) в случай на предозиране, особено при прием на алкохол. При продължителна употреба може да се развие остър панкреатит.
При комбинирана употреба с прокинетици и продължителна комбинирана употреба с индиректни антикоагуланти е възможно да се засили действието на прокинетиците и антикоагулантите.
Дози: възрастни се предписват перорално 0,5-1,0 g на всеки час, максималната дневна доза е 4 g.
АСПИРИН (ацетилсалицилова киселина). Максималната концентрация в кръвта се достига 2 часа след приема. Продължителност на действието 4 часа.
Показания: лека до умерена болка, температура над 38 С
При астма, анамнеза за алергични реакции, чернодробни и бъбречни заболявания, дехидратация, по време на бременност и при пациенти в напреднала възраст, лекарството трябва да се използва с повишено внимание.
При деца под 12 години, кърмачки, с пептична язва, хемофилия, свръхчувствителност към аспирин и други НСПВС, тежка бъбречна и чернодробна недостатъчност и през 3-ти триместър на бременността, употребата на аспирин е противопоказана.
Нежеланите реакции включват стомашно-чревна диспепсия, бронхоспазъм, кожни реакции. При продължителна употреба е възможен улцерогенен ефект, увеличаване на времето на кървене, тромбоцитопения и реакции на свръхчувствителност.
Когато се комбинира с други НСПВС и глюкокортикостероиди, рискът от развитие на нежелани реакции се увеличава, с антикоагуланти - увеличаване на риска от кървене. Комбинираната употреба с цитостатици и антиепилептични лекарства повишава токсичността на тези лекарства.
Дози: възрастни - 0,25 - 1,0 g на всеки час, максимална доза 4 g / ден.
Лизин моноацетилсалицилатът е производно на аспирин за парентерално приложение. Превъзхожда го по скорост на развитие и сила на аналгетичния ефект. Единична доза от 2 g, максималната - до 10 g на ден. Нежелани реакции - подобни на действието на аспирина.
ИБУПРОФЕН Максималната концентрация в кръвта се развива 1-2 часа след поглъщане, аналгетичните и антипиретичните ефекти продължават до 8 часа. Ибупрофен се предписва при лека до умерена болка, температура над 38 С
Противопоказания са свръхчувствителност към НСПВС, тежка бъбречна и чернодробна недостатъчност, пептична язва, трети триместър на бременността.
Нежелани лекарствени реакции: стомашно-чревна диспепсия, реакции на свръхчувствителност, бронхоспазъм; цитопения, автоимунни синдроми, с курс на приложение, улцерогенен ефект, влошаване на бъбречна и чернодробна недостатъчност, главоболие, замаяност, нарушение на слуха, ориентация, фоточувствителност, рядко папиларна некроза, асептичен менингит.
Комбинираната употреба с други НСПВС и глюкокортикостероиди увеличава риска от нежелани реакции. При комбиниране с флуорохинолони е възможно развитието на конвулсивен синдром. Когато се комбинира с диуретици, АСЕ инхибитори, бета-блокери, се наблюдава намаляване на терапевтичния ефект на тези лекарства и увеличаване на риска от странични ефекти. При комбиниране с цитостатици, антиепилептични средства, литиеви препарати ефектът им се засилва; когато се комбинира с антикоагуланти, рискът от хеморагични усложнения се увеличава; когато се комбинира със сърдечни гликозиди, НСПВС могат да повишат плазмената си концентрация.
ДИКЛОФЕНАК. Максималната концентрация в кръвта се развива след 0,5 - 2 часа. след поглъщане и през минутата. след i / m приложение.
Показания - виж по-горе
Противопоказания: виж по-горе, както и обостряне на хронични чревни заболявания, порфирия.
Взаимодействия: типични за лекарства от групата на НСПВС (виж по-горе).
Дози: mg / ден в две до три дози, интрамускулно 75 mg дълбоко в глутеалния мускул.
Навременната антибиотична терапия има решаващо влияние върху протичането на П и неговия изход. Когато пациентът постъпи в болница, изборът на антибиотик се извършва, като се вземат предвид горните клинични характеристики.
АНТИБИОТИЧНА ТЕРАПИЯ ПРИ ПНЕВМОНИЯ.
Най-честите патогени
Антибиотици от първа линия
Нетежко протичане при пациенти на възраст под 60 години с неусложнена анамнеза
P при пациенти на 60 и повече години и/или със съпътстващи заболявания
Цефалоспорини от второ поколение
P тежко протичане
Цефалоспорини от 3-то поколение
P при имунокомпрометирани пациенти
трето поколение антипсевдомонални цефалоспорини
(антипсевдомонални пеницилини) + аминогликозиди,
Цефалоспорини от 3-то поколение
амоксицилин - клавуланат + аминогликозид,
5.3 БЕЛОДРОБНА ЕМБОЛИЯ
Белодробната емболия (PE) е синдром, причинен от емболия на белодробната артерия или нейните клонове от тромб и се характеризира с тежки кардиореспираторни нарушения и когато малките клони са блокирани, симптомите на образуване на хеморагични инфаркти на белия дроб.
ЕТИОЛОГИЯ И ПАТОГЕНЕЗА.
Най-честата причина и източник на емболизация на клоновете на белодробната артерия са кръвни съсиреци от дълбоките вени на долните крайници при флеботромбоза (около 90% от случаите), много по-рядко - от дясното сърце при сърдечна недостатъчност и преразтягане на дясната камера. Предразполагащите фактори включват продължителна неподвижност, тазова или долна коремна хирургия, травма, затлъстяване, орални контрацептиви, бременност, злокачествено заболяване, инфаркт на миокарда, дилатативна кардиомиопатия, застойна сърдечна недостатъчност, предсърдно мъждене, сепсис, инсулт, увреждане на гръбначния мозък, еритремия, нефротичен синдром.
КЛИНИЧНА КАРТИНА, КЛАСИФИКАЦИЯ И ДИАГНОСТИЧНИ КРИТЕРИИ.
Няма клинични признаци, патогномонични за PE, диагнозата на предболничния етап може да се подозира въз основа на комбинация от анамнестични данни, резултати от обективно изследване и електрокардиографски симптоми.
КЛИНИЧНА И ЕЛЕКТРОКАРДИОГРАФСКА КАРТИНА НА ПЕЛ.
Внезапна поява с поява на задух (72% от случаите) и остра гръдна болка (86%), често - остра съдова недостатъчност с поява на бледност, цианоза, тахикардия (87%), спад на кръвното налягане до развитието на колапс и загуба на съзнание (12%). С развитието на белодробен инфаркт в 10-50% от случаите се появява хемоптиза под формата на ивици кръв в храчките. При преглед могат да се определят признаци на белодробна хипертония и остро белодробно сърце - подуване и пулсация на цервикалните вени, разширяване на границите на сърцето вдясно, пулсация в епигастриума, усилване при вдишване, акцент и бифуркация на II тон. върху белодробната артерия, уголемяване на черния дроб. Може би появата на сухи хрипове над белите дробове.
ЕКГ признаци (появяват се в 25% от случаите).
Признаци на претоварване на дясното предсърдие (P-pulmonale - висока заострена P вълна в отвеждания II, III, aVF) и дясната камера (синдром на McJean-White - дълбока S вълна в I отвеждане, дълбока Q вълна и отрицателна T вълна в отвеждане III с възможна елевация на ST сегмента; непълна блокада на десния крак на снопа His),
По този начин, въпреки липсата на ясни диагностични критерии, ПЕ може да бъде диагностицирана на предболничния етап въз основа на задълбочена цялостна оценка на историята, данните от прегледа и ЕКГ. Окончателната проверка на диагнозата се извършва в болницата. Понякога рентгеновото изследване разкрива високо стоящ купол на диафрагмата, дискоидна ателектаза, изобилие на един от корените на белите дробове или "нарязан" корен, изчерпване на белодробния модел над исхемичната зона на белия дроб, периферна триъгълна сянка на възпаление или плеврален излив, но при повечето пациенти няма рентгенологични промени. Диагнозата се потвърждава чрез белодробна перфузионна сцинтиграфия, която позволява откриване на характерни триъгълни зони с намалена белодробна перфузия (метод на избор), както и рентгеноконтрастна белодробна ангиография (ангиопулмонография), която разкрива зони с намален кръвен поток.
Клинично се разграничават остра, подостра и рецидивираща БЕ (Таблица 13.).
ВАРИАНТИ НА ПОТОКА НА ТЕЛА.
Характерни клинични признаци
Внезапна поява, болка в гърдите, задух, спадане на кръвното налягане, признаци на остро пулмонално сърце
Прогресираща дихателна и деснокамерна недостатъчност, признаци на инфарктна пневмония, хемоптиза
Повтарящи се епизоди на задух, синкоп, признаци на пневмония
При анализа на клиничната картина лекарят на LUTS трябва да получи отговори на следните въпроси.
1) Има ли задух, ако да, как се е появил (остро или постепенно).
При PE недостигът на въздух се появява остро, ортопнеята не е типична.
2) Имате ли болка в гърдите?
Може да прилича на ангина пекторис, локализирана зад гръдната кост, може да се влоши при дишане и кашляне.
3) Дали е имало немотивиран синкоп.
PE се придружава или се проявява със синкоп в около 13% от случаите.
4) Има ли хемоптиза.
Появява се с развитието на белодробен инфаркт.
5) Има ли подуване на краката (като се обърне внимание на тяхната асиметрия).
Дълбоката венозна тромбоза на краката е често срещан източник на PE.
6) Има ли скорошни операции, наранявания, има ли сърдечни заболявания със застойна сърдечна недостатъчност, ритъмни нарушения, приема ли орални контрацептиви, бременна ли е, наблюдава ли се при онколог.
Наличието на предразполагащи фактори за БЕ (например пароксизмално предсърдно мъждене) трябва да се има предвид от лекаря, ако пациентът развие остри кардиореспираторни нарушения.
АЛГОРИТЪМ ЗА ЛЕЧЕНИЕ НА ПАСТЕТ
Основните насоки на терапията на ПЕ на доболничния етап включват облекчаване на болката, предотвратяване на продължителна тромбоза в белодробните артерии и повтарящи се епизоди на БЕ, подобряване на микроциркулацията (антикоагулантна терапия), корекция на деснокамерна недостатъчност, артериална хипотония, хипоксия (кислородна терапия). ), облекчаване на бронхоспазъм.
При силна болка и за разтоварване на белодробната циркулация и намаляване на задуха се използват наркотични аналгетици (например 1 ml 1% разтвор на морфин интравенозно фракционно). Това позволява не само ефективно спиране на синдрома на болката, но и намаляване на задуха, характерен за PE. За нежелани реакции и противопоказания за употребата на морфин вижте раздела "Инфаркт на миокарда".
С развитието на инфарктна пневмония, когато болката в гърдите е свързана с дишане, кашлица, позиция на тялото, е по-препоръчително да се използват ненаркотични аналгетици (например интравенозно приложение на 2 ml 50% разтвор на аналгин).
Преживяемостта на пациенти с белодробен инфаркт зависи пряко от възможността за ранна употреба на антикоагуланти. Препоръчително е да се използват директни антикоагуланти - хепарин в / в струя в доза от 00 IU. Хепаринът не лизира тромба, но спира тромботичния процес и предотвратява растежа на тромба дистално и проксимално на ембола. Отслабвайки вазоконстриктивното и бронхопатичното действие на тромбоцитния серотонин и хистамин, хепаринът намалява спазъма на белодробните артериоли и бронхиолите, повлиявайки благоприятно хода на флеботромбозата, хепаринът служи за предотвратяване на рецидив на белодробна емболия. За нежелани реакции и противопоказания за употребата на хепарин вижте раздела „Инфаркт на миокарда“.
Ако протичането на заболяването се усложнява от деснокамерна недостатъчност, хипотония или шок, е показана терапия с допамин или добутамин (вижте раздел "Шок"). За подобряване на микроциркулацията реополиглюцин ml се използва допълнително интравенозно със скорост до 1 ml на минута. Reopoliglyukin не само увеличава BCC и повишава кръвното налягане, но също така има антиагрегационен ефект. Ако шокът продължава на фона на това лечение, преминават към терапия с пресорен аминамиг на допамин, разреден в 400 ml реополиглюкин, докато 1 ml от получения разтвор съдържа 500 μg допамин, а една капка съдържа 25 μg. Началната скорост на приложение е 5 μg / kg min под контрола на кръвното налягане с постепенно увеличаване на дозата до 15 μg / kg min. 2 ml 0,2% разтвор на норадреналин се разреждат в 250 ml изотоничен разтвор на натриев хлорид и се прилагат с начална скорост от капки в минута (когато хемодинамиката се стабилизира, скоростта се намалява до капки в минута).
При ПЕ е показана дългосрочна кислородна терапия. С развитието на бронхоспазъм и стабилно кръвно налягане (SBP не по-ниско от 100 mm Hg) е показано IV бавно (струйно или капково) приложение на 10 ml 2,4% разтвор на аминофилин. Eufillin намалява налягането в белодробната артерия, има антитромбоцитни свойства и има бронходилататорен ефект.
ЧЕСТИ ГРЕШКИ В ТЕРАПИЯТА.
В случай на белодробен инфаркт при пациенти с БЕ, употребата на хемостатични средства е неподходяща, тъй като хемоптиза се появява на фона на тромбоза или тромбоемболия.
Също така е непрактично да се предписват сърдечни гликозиди при остра деснокамерна недостатъчност, тъй като тези лекарства не засягат изолирано дясното сърце и не намаляват последващото натоварване на дясната камера. Дигитализацията обаче е напълно оправдана при пациенти с тахисистолно предсърдно мъждене, което често е причина за тромбоемболия.
ПОКАЗАНИЯ ЗА ХОСПИТАЛИЗАЦИЯ.
При съмнение за БЕ хоспитализацията е задължителна.
5.4 ГНОЙНИ ЗАБОЛЯВАНИЯ НА БЕЛИЯ ДРОБ И ПЛЕВРАТА.
Остър абсцес, гангрена на белия дроб са гнойно-некротично сливане на белодробния паренхим (при гангрена некрозата е по-обширна, без ясни граници, склонна към разпространение; клинично заболяването се проявява с много тежко общо състояние на пациента).
ЕТИОЛОГИЯ И ПАТОГЕНЕЗА.
Основните причини за деструктивни промени в белите дробове са: усложнение на остър П (често постгрипен) - в 63-95% от случаите; аспирация (попадане на инфекциозен агент в белия дроб от устната кухина - кариозни зъби, пародонтоза, хроничен тонзилит). През последните години е установено, че в 50-60% от случаите се аспирира само анаеробна микрофлора (Fusobact. nucleatum, Fusobact. necrophorum, Bacter. fragilis, Bacter. melaninogenus и др.).
В допълнение, най-честите патогени са: хемолитичен стафилокок ауреус и грам-отрицателна микрофлора.
Сред другите причини за развитието на остър абсцес и гангрена на белия дроб е необходимо да се посочи хематогенно-емболичният път (в 0,8-9,0% от случаите), посттравматичен фактор, бронхиална обструкция (тумор, чуждо тяло).
Трябва да се подчертае, че остри абсцеси и гангрена на белия дроб най-често се развиват при пациенти, отслабени от хронични заболявания, при лица с алкохолна зависимост; с тежки системни заболявания, на фона на ХОББ.
острите абсцеси и гангрена на белия дроб са разнообразни и зависят от размера на некротичните участъци на белодробната тъкан, сложното или неусложненото протичане, възрастта на пациента, съпътстващите заболявания, индивидуалните характеристики на организма и др. При белодробен абсцес в началния (първи) период на заболяването (преди отварянето на абсцеса в бронхите) тежестта на състоянието на пациента се определя от гнойна интоксикация поради невъзможността за евакуация на гной и некротични маси от унищожаването кухини по естествен път през дрениращите бронхи. Болните се оплакват от висока температура, втрисане, болка в съответната половина на гръдния кош, кашлица с оскъдна храчка. При физикален преглед от "болната" страна дишането е отслабено, перкуторният звук е скъсен. При голяма лезия на белодробната тъкан се чуват крепитативни хрипове. Рентгеновите данни показват възпалителна инфилтрация на белия дроб без ясни граници.
Първият период на заболяването продължава средно 7-10 дни.
Във втория период на заболяването (след отваряне на абсцеса в бронхите) патогномоничният симптом ще бъде обилно отделяне на гнойни храчки, често с неприятна миризма, "пълна уста". Ако в същото време има арозия на бронхиалните съдове, ще се отбележи белодробно кървене. В същото време температурата намалява, интоксикацията намалява и благосъстоянието се подобрява. По време на физикален преглед е възможно да се идентифицира кухина в белия дроб с перкусия, с аускултация - бронхиално дишане с амфоричен нюанс. Характерна е рентгеновата семиотика - заоблена кухина, заобиколена от инфилтративен вал, с хоризонтално ниво на течност в лумена.
Храчките (макроскопски) имат три слоя: гной, мътна течност, пенест слой.
Белодробната гангрена се характеризира с по-обширна некроза на белодробния паренхим (отколкото при абсцес), без ясни граници, заемаща няколко сегмента, лоб или целия бял дроб. Заболяването протича бързо, с хектична треска, тежка интоксикация, гръдна болка от страната на лезията, задух. Храчките са мръсносиви или кафяви (по-често) на цвят със зловонна миризма, определя се от разстояние, често със секвестри на белодробната тъкан. Понякога заболяването се усложнява от белодробно кървене (хемоптиза), което може да бъде фатално. Над мястото на лезията се определя скъсяване на перкуторния звук и рязко отслабено (или бронхиално) дишане. В изследванията на кръвта и храчките промени, характерни за остър абсцес, но по-изразени. Рентгенографията на белите дробове разкрива масивна инфилтрация без ясни граници, заемаща лоб или целия бял дроб. Ако се е появила кухина на гниене и тя комуникира с лумена на бронха, тогава рентгенологично това се определя като просветление с неправилна форма (единично или множествено), възможно с наличие на свободни или париетални секвестри.
Трябва да се подчертае, че острият абсцес и гангрена на белия дроб са изпълнени с развитието на редица тежки, понякога фатални усложнения: арозивно кървене (особено когато процесът е локализиран в кореновите зони), пиопневмоторакс (с субплеврални абсцеси), сепсис , перикардит, увреждане на противоположния бял дроб.
Остър гноен плеврит
Остър гноен плеврит - възпаление на плеврата, характеризиращо се с образуването на гноен ексудат.
Острият гноен плеврит (плеврален емпием) може да бъде първичен (след проникваща рана на гръдния кош, операции на белите дробове, диагностична торакоскопия, с налагане на изкуствен пневмоторакс) или вторичен (с усложнения на гнойно-възпалителни заболявания на белите дробове и отвори на субплеврално разположени абсцеси). В последния случай, заедно с гной, въздухът навлиза и в плевралната кухина (пиопневмоторакс). Бактериалният спектър на съдържанието на плевралната кухина при 62,5% от пациентите показва асоциация на патогени от 2-5 различни вида (staphylococcus aureus, proteus, Escherichia coli и Pseudomonas aeruginosa). Бактериологичните изследвания в 28% от случаите разкриват различни видове неклостридиални анаероби (бактероиди, фузобактерии, гниещи стрептококи и др.).
остър вторичен емпием на плеврата се характеризира с факта, че възпалителният процес от белия дроб (пневмония, абсцес, каверна, гнойна киста) преминава към плеврата, обикновено от същата страна. Има остри болки в съответната половина на гръдния кош, повишаване на температурата до 38,5-39 ° C, признаци на дихателна недостатъчност (поради компресия на белия дроб от гной и гнойно-деструктивни промени в самата белодробна тъкан), кашлица с гной храчки. При обективен преглед се откриват симптоми на интоксикация, ограничаване на дихателните движения на едната половина на гръдния кош, тъпота на перкуторния звук и рязко отслабване на дишането (или изобщо не се извършва, което се случва по-често). Рентгеновото изследване показва потъмняване от страната на емпиема, изместване на медиастинума в обратна посока. При пиопневмоторакс се определя хоризонталното ниво и газът над него. В зависимост от количеството гнойна течност в плевралната кухина и съответно степента на колапс на белия дроб се различават ограничен, субтотален и тотален пиопневмоторакс.
Спонтанен неспецифичен пневмоторакс
Спонтанният пневмоторакс (SP) е натрупване на въздух в плевралната кухина.Развива се, като правило, без предшестващи симптоми (при пълно здраве). Въздухът навлиза от дефекта(ите) на субплеврално разположените въздушни були. Повечето изследователи смятат, че образуването на були е свързано с вродена непълноценност на белодробния паренхим. Напоследък има съобщения за случаи на фамилна форма на заболяването - наследствен спонтанен пневмоторакс (наследствен емфизем). Предполага се, че причината за него е дефицит на алфа-1 антитрипсин, който се унаследява по автозомно-рецесивен начин. Десният бял дроб е по-често засегнат, двустранен (обикновено редуващ се) пневмоторакс се наблюдава в 17,7% от случаите.
спонтанният пневмоторакс е доста типичен: появата на остри болки в съответната половина на гръдния кош (често без видима причина), задух (неговата тежест зависи от степента на колапс на белия дроб). Болката се разпространява в рамото, шията, епигастричния регион, зад гръдната кост (особено при левостранен пневмоторакс), често симулирайки ангина пекторис или инфаркт на миокарда. Физикалният преглед разкрива задух, тимпанит при перкусия от страната на лезията, отслабване (или липса) на дишане при аускултация. Диагнозата се уточнява по рентгенови данни: наблюдава се пневмоторакс с различна тежест от засегнатата страна и белодробен колапс. При голям пневмоторакс може да има изместване на медиастинума в обратна посока. Необходимо е задълбочено изследване на белите дробове, за да се установи възможната причина за пневмоторакс - булозен емфизем, туберкулозна кухина, абсцес (при тези заболявания пневмотораксът е тяхното усложнение). Понякога големи субплеврално разположени були на първия сегмент могат да бъдат идентифицирани на рентгенография.
ПРИНЦИПИ НА ТЕРАПЕВТИЧНИТЕ МЕРКИ.
Интервенцията на предболничния етап се свежда до симптоматична терапия.
1) Синдром на болката - преди транспортиране на пациента в болница със силна плеврална болка могат да се прилагат ненаркотични аналгетици - кетаролак, трамадол. При пневмоторакс интензивността на болковия синдром може да изисква прилагането на наркотични аналгетици. В този случай 2% разтвор на промедол трябва да се счита за средство за избор. Трябва да се има предвид, че по-мощните лекарства, морфин и фентанил, имат потискащ ефект върху дихателния център и могат да влошат хипоксията.
2) Артериална хипотония - транспортирането на пациентите до болницата, за да се избегне развитието на ортостатичен колапс, трябва да се извършва в легнало положение. При ниско кръвно налягане (SBP< 100) целесообразно во время транспортировки проводить в/в инфузию раствора полиглюкина.
3) Дихателна недостатъчност - развива се с масивна лезия на белодробната тъкан. За да се намали степента на хипоксия по време на транспортиране, се вдишва овлажнен кислород през назални канюли или маска.
4) Увеличаването на дихателната недостатъчност при пневмоторакс може да бъде свързано с клапния механизъм на неговото развитие. В този случай напрегнатият пневмоторакс изисква спешна декомпресия, която се извършва чрез въвеждане на една или повече инжекционни игли с голям диаметър в плевралната кухина. Провеждането на тази манипулация изисква предварителна анестезия с въвеждането на 1 ml 2% разтвор на промедол.
ПОКАЗАНИЯ ЗА ХОСПИТАЛИЗАЦИЯ.
Гнойните белодробни заболявания, както и случаите на развитие на пневмоторакс, изискват спешна хоспитализация на пациенти в отделението по гръдна хирургия.
1. Бета-2 адреномиметици
1.1 Краткодействащи бета-2 адреномиметици:
Салбутамол 90./44/6
(Ventolin 00238/16.01.95, Ventolin Лесно дишане, Ventolin nebula P8242-011022. 06.04.99 Ventodisk 007978/25.11.96. Salben 95/178/11) Фенотерол (Berotek N 011310/01-1999, 10.08.99) Тербуталин (Бриканил 00427/26.01.93) Хексопреналин (Ипрадол 002557/14.07.92)
1.2 Бета-2 дългодействащи агонисти:
Кленбутерол (Spiropent 007200/28.05.96) Формотерол (Foradil 003315/10.09.93, Oxys 011262/21.07.99) Салметерол (Serevent 006227/28.06.95, Salmeter 006936/21.12.95) Салбутамол (Volmaks 0 94/294/9)
2. Метилксантини
2.1 Аминофилин (Euphyllin 72/631/8. 72/334/32; Aminophyllin 002301/10.12.91; 002365/27.01.92)
теофилин
Ипратропиев бромид (Atrovent 00943/09/22/93; 007175/04/04/96; 007655/07/22/96)
4. Комбинирани лекарства:
бета-2 адреномиметик + ипратропиев бромид
фенотерол + ипратропуим бромид (Berodual 01104/04.05.95)
бета-2 адреномиметик + кромоглицинова киселина
фенотерол + кромоглицинова киселина (Дитек 008030/25.02.97) салбутамол + кромоглицинова киселина (Интал плюс 006261/11.07.95)
1. Бета-2 адреномиметик
1.1. Краткодействащ бета-2 агонист
Салбутамол
(Вентолин, Вентолин небула, Ветодиски, Вентолин Лесно дишане, Салбен) Фармакологично действие
Салбутамолът е селективен агонист на бета-2-адренергичните рецептори, локализирани в бронхите, миометриума и кръвоносните съдове.В терапевтични дози, действайки върху бета-2-адренергичните рецептори на бронхиалната гладка мускулатура, той има изразен бронходилататорен ефект и има малък или никакъв ефект върху бета-1-адренергичните рецептори.миокард
При инхалационен път на приложение се абсорбира от тъканите на белите дробове, без да се метаболизира в белите дробове, навлиза в кръвния поток. Лекарството се метаболизира по време на "първото преминаване" през черния дроб и след това се екскретира главно в урината в непроменена форма или под формата на фенол сулфат.
Бронходилататорният ефект настъпва след 4-5 минути, максималният ефект е 40-60 минути, полуживотът е 3-4 часа, продължителността на действие е 4-5 часа Състав и форма на освобождаване
Съставите на салбутамол се предлагат в различни форми и с различни устройства за доставяне в дихателните пътища.
Дозиращ аерозолен инхалатор Ventolinсъдържа 100 mcg салбутамол (като салбутамол сулфат) на доза
Дозиран инхалатор Ventolin Easy Breathingактивира се чрез дишане, което улеснява вдишването, не изисква синхронизация съдържа 100 mcg салбутамол (салбутамол сулфат) на доза
Мъглявината Вентолин(пластмасови ампули) от 2,5 ml, съдържащи 2,5 mg салбутамол във физиологичен разтвор (под формата на салбутамол сулфат) за инхалация през пулверизатор Съставът на лекарството не включва консерванти и оцветители
Вентодиск -прах за инхалация, 200 mcg салбутамол сулфат в 1 доза, в комплект с дисков инхалатор "Ventolin-Diskhaler"
Салбен- сух прах за инхалация, 200 mcg, прилаган с индивидуален инхалатор циклохалер
Дозов режим
Дозиран аерозол Вентолин, Вентолин Лесно дишане, прах Вентодиск, Салбен се прилагат по 100-200 mcg (1 или 2 инхалации), 3-4 пъти на ден.
Ventolin Nebula трябва да се използва под наблюдението на специалисти, като се използва специален инхалатор (пулверизатор) Ventolin Nebula е предназначен за употреба неразреден само за инхалационно приложение 2)
Странични ефекти
Салбутамол може да причини лек тремор на скелетните мускули, който обикновено е най-изразен в ръцете, понякога възбуда и повишена двигателна активност. В някои случаи 16 пациенти имат главоболие, периферна вазодилатация и леко компенсаторно повишаване на сърдечната честота При пациенти с предразположеност към развитие на аритмии са възможни сърдечни аритмии Инхалаторните лекарства могат да причинят дразнене на лигавицата на устната кухина и фаринкса
- Употребата на големи дози салбутамол, както и други бета-2-агонисти, може да причини хипокалиемия, следователно, ако се подозира предозиране, трябва да се следи нивото на калий в кръвния серум
Подобно на други бета-адренергични агонисти, салбутамол може да причини обратими метаболитни промени, като повишаване на концентрацията на глюкоза в кръвта.При пациенти със захарен диабет може да се развие декомпенсация и в някои случаи развитие на кетоацидоза.
Fenoterol hydrobromide (Berotek) Фармакологично действие
Фенотеролът е краткодействащ бета-2-адренергичен стимулант.Високият бронходилатативен ефект е свързан със селективността към бета-2-адренергичните рецептори, както и с активирането на аденилатциклазата, натрупването на сАМР отпуска гладката мускулатура на бронхите; предизвиква стабилизиране на мембраните на мастоцитите и базофилите (намалява освобождаването на биологично активни вещества), подобрява мукоцилиарния клирънс; има токолитичен ефект Състав и форма на освобождаване
Дозов инхалатор Berotek N (с пропелант без CFC) —в 1 доза от 100 mcg фенотерол хидробромид
Berotek разтвор за пулверизираща терапия- 1 ml от разтвора съдържа 1,0 mg фенотерол хидробромид
Дозов режим
а) остър пристъп на бронхиална астма
В повечето случаи една инхалационна доза е достатъчна за облекчаване на симптомите, но ако няма облекчение на дишането в рамките на 5 минути, можете да повторите инхалацията
Ако след две инхалации няма ефект и са необходими допълнителни инхалации, трябва незабавно да потърсите медицинска помощ в най-близката болница.
б) Профилактика на астма, причинена от физическо усилие
1-2 инхалационни дози наведнъж, до 8 дози на ден
в) Бронхиална астма и други състояния, придружени с обратимо стесняване на дихателните пътища
1-2 инхалационни дози на доза, ако са необходими многократни инхалации, тогава не повече от 8 инхалации на ден
Berotek N дозиран аерозол за деца трябва да се предписва само по препоръка на лекар и под наблюдението на възрастни.
Разтворът за инхалация се предписва чрез пулверизатор под строг медицински контрол (дозите Berotek за пулверизатор са дадени в Приложение 2)
Страничен ефект
В резултат на предозиране може да има усещане за прилив на кръв към лицето, тремор на пръстите, гадене, безпокойство, сърцебиене, замаяност, повишено систолно кръвно налягане, понижено диастолично кръвно налягане, възбуда и евентуално екстрасистоли.
Тербуталин (Бриканил) Фармакологично действие
Тербуталин е селективен бета-2 агонист с кратко действие. Бронходилататорният ефект се дължи на стимулиране на бета-2-адренергичните рецептори;
намаляване на тонуса на гладкомускулните клетки и разширяване на мускулите на бронхите.
Състав и форма на освобождаване Дозиращ аерозолен инхалатор Brikanil -в 1 доза 250 mcg тербуталин сулфат Бриканил таблетки- 1 таблетка съдържа: тербуталин сулфат - 2,5 mg
Дозов режим
Вдишване с дозиращ инхалатор, 1-2 вдишвания (0,25) на всеки 6 часа. Доза за перорално приложение 2,5 mg 3-4 пъти на ден.
Хексопреналин (Ипрадол) Фармакологично действие
Ипрадол е селективен бета-2 агонист с кратко действие - катехоламин, съставен от две молекули на норепинефрин, свързани с хексаметиленов мост. Общото за всички тези молекули е селективен бета-2 рецепторен афинитет.
Състав и форма на освобождаване:
Дозиращ аерозолен инхалатор Ипрадол- 1 доза от 200 mcg хексопреналин сулфат
Таблетки- 1 tb - 500 mcg хексопреналин сулфат.
Дозов режим
Инхалацията с ипрадол се предписва на деца над 3 години на 1 вдишване, с интервал от най-малко 30 минути.
Ипрадол под формата на таблетки се предписва на деца с лека до умерена астма, с леки пристъпи на задух в доза от
3-6 месеца 0.125mg (1/4tb) 1-2 пъти/ден
7-12 месеца 0,125 mg (1/4 tb) 1 път/ден
1-3 години 0,125-0,25 mg (1/4-1/2 TB) 1-3 пъти/ден
4-6 години 0,25 мг(1/2 tb) 1-3 пъти/ден
7-10 години 0,5 mg (1 tb) 1 път/ден Страничен ефект
Сред нежеланите реакции при малки деца рядко има повишена възбудимост, раздразнителност, нарушение на съня и промяна в ритъма на съня.
1.2. Дългодействащи бета-2 агонисти
Салметерол (Serevent, Salmeter) Фармакологично действие
Селективен агонист на бета-2-адренергичните рецептори с удължено действие. Началото на действие е 5-10 минути след вдишване с продължително разширяване на бронхите до 12 часа. Салметерол бързо се хидроксилира в черния дроб, основната част от приетата доза се елиминира в рамките на 72 часа.
Форма за освобождаване
Serevent Rotadisk- под формата на кръгли блистери (ротадиски), изработени от фолио с 4 клетки с прах, разположен околовръст. Една клетка съдържа доза от 50 mcg салметерол ксинафоат и лактоза като пълнител. Serevent Rotadisk се използва със специално устройство за инхалация - "Serevent Diskhaler". Цялата доза от лекарството навлиза в дихателните пътища дори при много ниска скорост на вдишване.
Дозиращ аерозолен инхалатор Sereventсъдържа 25 микрограма салметерол ксинафоат на доза.
Дозов режим
Предписва се на деца над 3 години по 25-50 mcg (1-2 вдишвания) 2 пъти на ден.
Редовната (2 пъти на ден) употреба на Serevent е показана в случаите, когато пациентът трябва да използва краткодействащ инхалаторен бронхоспазмолитик повече от 1 път на ден или в комбинация с инхалаторни кортикостероиди. Страничен ефект
Може би развитието на парадоксален бронхоспазъм, главоболие, тахикардия, тремор;
възможна хипокалиемия.
Салбутамол с удължено действие (Volmaks, Saltos) Фармакологично действие
Продължителното действие на бета-2-адренергичния агонист се дължи на осмотично контролирания механизъм на постепенно освобождаване на лекарственото вещество от ядрото на таблетката в рамките на 9-12 часа.
Форма за освобождаване
Волмакс- таблетки от 4 mg и 8 mg салбутамол сулфат.
Салтос- таблетки от 7,23 mg салбутамол сулфат.
Дозов режим
Деца на възраст 3-12 години: 4 mg 2 пъти дневно Таблетките трябва да се поглъщат цели с вода, без да се хапят или дъвчат. Над 12 години - при необходимост дозата може да се увеличи до 8 mg 2 пъти дневно.
Формотерол (Foradil, 0xis) Фармакологично действие
Селективен бета-2-агонист. Началото на бронхоспазмолитично действие след вдишване след 1-3 минути, терапевтичният ефект продължава 12 часа. Активното вещество и неговите метаболити се елиминират напълно от тялото. Фармакокинетичните характеристики на пероралния и инхалаторния формотерол са до голяма степен сходни.
Състав и форма на освобождаване- 1 доза съдържа: формотерол фумарат - 4,5-9 мкг. форадил -прах за инхалация в капсули - 1 капсула съдържа: формотеролов фумарат - 12 mcg
Дозов режимДеца на 5 и повече години се предписват 1-2 пъти на ден.
Кленбутерол (Спиропент) Фармакологично действие
спиропентселективен бета-2 агонист. Има дълъг биологичен полуживот и бърза и пълна абсорбция при перорално приложение. Има ефект след прием в рамките на 10-12 часа.
Състав и форма на освобождаване
Таблетки - 1 TB съдържа 0,02 mg кленбутерол хидрохлорид
Сироп - в 5 мл 0,005 мг кленбутерол хидрохлорид
Дозов режим
Таблетките се предписват на деца над 12 години и възрастни, 1 TB (0,02 mg 2 пъти / ден. При продължителна терапия дозата може да бъде намалена до 0,02 mg / ден.
За деца под 12 години дозата на спиропент е 0,0012 mg/kg телесно тегло.
Spiropent в сироп се предписва на деца:
6-12 години 15 ml (0,015 mg) 2 пъти / ден.
4-6 години 10 ml (0,01 mg) 2 пъти / ден.
2-4 години 5 ml (0,005 mg) 3 пъти / ден.
под 2 години 5 ml (0,005 mg) 2 пъти / ден.
Страничен ефект
Spiropent може да причини тремор на пръстите, рядко възбуда, тахикардия, екстрасистоли.
2.Метилксантини
2.1 Eufillin, Aminofilin Фармакологично действие
Метилксантините имат изразен бронходилатативен ефект, подобряват контракцията на диафрагмата, повишават мукоцилиарния клирънс, намаляват белодробното съдово съпротивление, имат положителен инотропен и умерен диуретичен ефект. Теофилините инхибират освобождаването на алергични медиатори от мастоцитите, стимулират централната нервна система, дихателния център и увеличават отделянето на адреналин от надбъбречните жлези. Действието на лекарствата се дължи на инхибирането на фосфодиестераза и в резултат на това увеличаване на натрупването на цикличен аденозин монофосфат в тъканите. Клиничният ефект зависи от концентрацията на лекарството в кръвния серум. Когато се приема перорално, теофилинът се абсорбира бързо и напълно, но бионаличността зависи от лекарствената форма на лекарството. Основният път на елиминиране на теофилин е неговата биотрансформация в черния дроб, 10% от непромененото лекарство се екскретира в урината.
Форма за освобождаване
Разтвор на еуфилин- за интравенозно приложение - 10 ml 2,4% в ампула
Eufillin таблетки– 1 таблетка съдържа – 150 мг
Дозов режим
Натоварващата доза за интравенозно приложение е 4,5-5 mg/kg за 20-30 минути. Впоследствие аминофилинът може да се прилага чрез продължителна инфузия в доза от 0,6-0,8 mg / kg / час или фракционно в подходящи дози на всеки 4-5 часа под контрола на концентрацията на теофилин в кръвта.
Оралната дневна доза е средно 7-10 mg/kg. Страничен ефект
Безпокойство, нарушения на съня, главоболие, тремор, гадене, повръщане, диария, сърцебиене, ритъмни нарушения.
2.2 Дългодействащ теофилин
Освобождаването на теофилин от лекарствени форми с продължително освобождаване се осъществява по такъв начин, че концентрацията се поддържа в терапевтични граници (8-15 mg / l) почти през всички дни с плавен максимум през нощта и ранните сутрешни часове
Форма за освобождаване Teopak- таблетки -1 таблетка - 100, 200, 300 mg безводен теофилин Retafil- таблетки -1 таблетка - 200, 300 mg безводен теофилин Теотард- капсули - 1 капсула - 200, 350, 500 mg безводен теофилин Еуфилонг- капсули - 1 капсула - 250, 375 mg безводен теофилин. Вентакс- капсули от 100, 200, 300 mg теофилин безводен теофилин безводен Спорофилин-ретард- таблетки от 100, 250 mg безводен теофилин
Дозов режим
Дневната доза за деца 6-8 години е 200-400 mg в 1-2 приема, 8-12 години 400-600 mg, над 12 години 600-800 mg
Страничен ефект
Сърцебиене, аритмии, безпокойство, възбуда, тремор, нарушения на съня, главоболие, гадене, повръщане, диария
3. Блокери на М-холинорецепторите
Ipratropium bromide (ATROVENT) Фармакологично действие
Активното вещество е ипратропиев бромид, конкурентен антагонист на невротрансмитера ацетилхолин Atrovent блокира рецепторите на гладката мускулатура на трахеобронхиалното дърво и потиска рефлексната бронхоконстрикция, предотвратява медиираната от ацетилхолин стимулация на чувствителните влакна на блуждаещия нерв при излагане на различни фактори Atrovent има както превантивен, така и бронходилататорен ефект, предизвиква намаляване на секрецията на бронхиалните жлези
Ефектът на лекарството се появява 25-50 минути след вдишване, достига максимум до края на 1 час и продължава 6-8 часа
Състав и форма на освобождаване
Дозиран аерозолен инхалатор, 1 доза - 20 микрограма ипратропиум бромид
Разтвор за инхалация 1 ml (20 капки)- 250 микрограма ипратропиев бромид Дозов режим
Дозиращ аерозол- 1-2 инхалации 3-4 пъти / ден
Разтвор за инхалация през пулверизатор (Приложение 2) Страничен ефект
Системните ефекти са неизвестни, в някои случаи може да се появи сухота в устата, ако попадне в очите, леки обратими нарушения на акомодацията.
4. Комбинирани лекарства
Бета-2 адреномиметик + ипратропиум бромид (BERODUAL) Фармакологично действие
Berodual е комбиниран бронходилататор, който включва фенотерол (бета-2-агонист) и ипратропиум бромид, блокер на М-холинергичните рецептори. Ипратропиум бромид блокира холинергичните рецептори, бета-2-агонистът предизвиква стимулиране на бета-рецепторите на гладкомускулните клетки и бърза бронходилатация Комбинацията от вещества с различни механизми на действие потенцира бронходилататорния ефект и увеличава неговата продължителност Състав и форма на освобождаване
Дозиращ аерозолен инхалатор Berodual- 1 доза съдържа 50 микрограма фенотерол и 20 микрограма ипратропиум бромид
Разтвор за инхалация Berodual– 20 ml във флакон за небулизаторна терапия’ 1 ml (20 капки) съдържа 500 mcg фенотерол и 250 mcg ипратропиум бромид Дозов режим
Дозиране на аерозол Berodual се предписва на деца над 3 години, 1-2 дози 3 пъти на ден (до 8 дози на ден).
Berodual разтвор за пулверизатор (Приложение 2)
Страничен ефект
Страничните ефекти са незначителни. В случай на относително или абсолютно предозиране са възможни тремор на пръстите, сърцебиене, свързани с наличието на фенотерол в препарата. В някои случаи сухота в устата, леки и обратими нарушения на акомодацията, свързани с наличието на ипратропиев бромид в подготовка
Бета-2 адреномиметик + кромоглицинова киселина (Дитек) Фармакологично действие
Комбинирано лекарство с бронходилататорно и антиалергично действие. Предотвратява и елиминира бронхоспазма, подобрява функцията на ресничестия епител, предотвратявайки дегранулацията на мастоцитите и освобождаването на биологично активни вещества от тях.
Състав и форма на освобождаване
Дозов инхалатор - 1 инхалационна доза съдържа фенотерол хидробромид - 50 mcg и динатриев кромогликат - 1 mg
Дозов режимДеца 4-6 години: 1 доза 4 пъти дневно. Деца над 6 години” 2 инхалационни дози 4 пъти дневно
Страничен ефектВъзможен тремор на пръстите, сърцебиене, безпокойство
Бета-2 адреномиметик + кромоглицинова киселина (Интал плюс) Фармакологично действие
Натриевият кромогликат предотвратява бронхоспазма, като предотвратява дегранулацията на мастоцитите и освобождаването на биологично активни вещества от тях Салбутамол е бета-адренергичен агонист с преобладаващ ефект върху бета-2 рецепторите, има бронходилататорен ефект
Състав и форма на освобождаване
Дозиращ аерозолен инхалатор - 1 доза съдържа натриев кромогликат - 1 mg, салбутамол - 100 мили- Дозов режим
Деца от 6 години 1-2 инхалации 4 пъти на ден. При по-тежки случаи или при контакт с алерген е възможно дозата да се увеличи до 6-8 инхалации на ден.
Страничен ефект
Възможни възпалено гърло, кашлица, бронхоспазъм, главоболие, преходни мускулни крампи, изключително рядко ангиоедем, артериална хипотония, колапс.
(Посетен 221 пъти, 1 посещения днес)
Бета агонисти
Бета-агонисти(син. бета-агонисти, бета-агонисти, β-агонисти, β-агонисти). Биологични или синтетични вещества, които предизвикват стимулация на β-адренергичните рецептори и оказват значително влияние върху основните функции на тялото. В зависимост от способността за свързване с различни подтипове β-рецептори се изолират β1- и β2-агонисти.
Физиологична роля на β-адренорецепторите
Кардиоселективните β1-блокери включват талинолол (Cordanum), ацебутолол (Sektral) и целипролол.
Използването на бета-агонисти в медицината
Неселективни β1-, β2-агонистиизопреналин и орципреналин се използват за кратко време за подобряване на атриовентрикуларната проводимост и ускоряване на ритъма при брадикардия
β1-агонисти: допамин и добутамин се използват за стимулиране силата на сърдечните контракции при остра сърдечна недостатъчност, причинена от миокарден инфаркт, миокардит или други причини.
краткодействащи β2-агонисти, като фенотерол, салбутамол и тербуталин се използват под формата на дозирани аерозоли за облекчаване на астматичен пристъп при бронхиална астма, хронична обструктивна белодробна болест (ХОББ) и други бронхообструктивни синдроми. Интравенозният фенотерол и тербуталин се използват за намаляване на трудовата дейност и при заплаха от спонтанен аборт.
дългодействащи β2-агонистисалметерол се използва за профилактика, а формотерол както за профилактика, така и за облекчаване на бронхоспазъм при бронхиална астма и ХОББ под формата на дозирани аерозоли. Те често се комбинират в един и същ аерозол с инхалаторни глюкокортикостероиди за лечение на астма и ХОББ.
Странични ефекти на бета-агонисти
При използване на инхалаторни бета-агонисти най-често се наблюдават тахикардия и тремор. Понякога - хипергликемия, възбуждане на централната нервна система, понижаване на кръвното налягане. При парентерално приложение всички тези явления са по-изразени.
Предозиране
Характеризира се със спадане на кръвното налягане, аритмии, намаляване на фракцията на изтласкване, объркване и др.
Лечение - използване на бета-блокери, антиаритмични лекарства и др.
Употребата на β2-агонисти при здрави хора временно повишава устойчивостта към физическа активност, тъй като те "поддържат" бронхите в разширено състояние и допринасят за ранното "отваряне на втори вятър". Често това се използва от професионални спортисти, по-специално колоездачи. Трябва да се отбележи, че в краткосрочен план β2-агонистите наистина повишават толерантността към физическо натоварване. Но неконтролираното им използване, както всеки допинг, може да причини непоправима вреда на здравето. Към β2-адреномиметиците се развива пристрастяване (за да "оставите отворени" бронхите, трябва постоянно да увеличавате дозата). Увеличаването на дозата води до аритмии и риск от сърдечен арест.




