Черепно-мозговая травма у детей. Симптомы, диагностика, лечение. Обследование малыша с черепно-мозговой травмой. Реабилитация после черепно-мозговой травмы
Все дети с признаками повреждения черепа и/или головного мозга, независимо от степени их тяжести, подлежат госпитализации в стационар для обследования, динамического наблюдения и, при необходимости, проведения хирургического вмешательства. Пациенты должны наблюдаться неврологом, а при необходимости и нейрохирургом. Нахождение таких детей в травматологических или общехирургических отделениях допустимо только в тех случаях, когда нет возможности их госпитализировать в специализированные нейрохирургические или неврологические отделения.
Общие вопросы хирургической тактики при ЧМТ описаны в настоящем руководстве, а ее особенности у детей представлены в соответствующих разделах данной главы. Здесь же хотелось бы остановиться на общих принципах и особенностях консервативного лечения ЧМТ у детей.
Основное значение при лечении нетяжелой ЧМТ (сотрясение головного мозга и ушиб легкой степени) имеет психоэмоциональный покой. В течение 7—8 дней детям показан постельный режим. Поскольку, как показывает практика, даже в стационаре обеспечить строгое его соблюдение невозможно, поэтому более целесообразно говорить об ограничении двигательной активности ребенка. Рекомендуется десенсибилизирующая терапия (димедрол, супрастин в течение 3—5 дней), при наличии гипертензионных проявлений — прием дегидратационных препаратов в течение 3—5 дней (диакарб по 10—15 мг/кг/с, а при его неэффективности — фуросемид до 1 мг/кг/с) в сочетании с аспаркамом или пантогамом.
Противосудорожная терапия проводится только при наличии припадков в анамнезе или отягощенном фоне.
В случаях сотрясения головного мозга и при наличии хороших бытовых условий, по мнению ряда авторов, дети могут находиться дома.
При ушибах мозга средней степени тяжести постельный режим продлевается до 10—14 дней и проводится симптоматическая терапия, описанная выше.
Консервативное лечение тяжелой ЧМТ является сложной задачей нейрохирургии, неврологии и, в основном, нейрореаниматологии. Лечебные мероприятия могут быть условно разделены на два этапа: догоспитальный и госпитальный.
Основными задачами догоспитального этапа являются: а) раннее выявление и коррекция повреждений, угрожающих жизни ребенка; б) реанимация пациента и стабилизация его жизненно важных функций; в) выявление потенциально опасных сопутствующих повреждений; г) разделение повреждений в порядке их приоритета; д) подготовка пациента к транспортировке и транспортировка в специализированный стационар.
Первичное обследование и реанимация проводятся по четырем параметрам (А, В, С, D).
А — обеспечение проходимости дыхательных путей и исключение возможных дополнительных повреждений шейного отдела позвоночника;
В — поддержание дыхания;
С — поддержание кровообращения и контроль за кровотечением;
D — оценка дисфункции ЦНС.
А. Планируя первичные мероприятия, необходимо учитывать возможность повреждения шейного отдела позвоночника, поэтому, при подозрении на краниоцервикальную травму, до уточнения диагноза шея должна быть иммобилизирована без тракции. С этой целью используют спинальные щиты, мешки с песком и/или жесткие воротники. Необходимо очистить дыхательные пути от секрета, рвотных масс, крови и/или инородных тел. В дальнейшем проходимость дыхательных путей поддерживается путем незначительного разгибания головы и выдвижением вперед нижней челюсти. При наличии рефлекса на роторасширитель, использование воздуховодов противопоказано, т.к. это может вызвать удушье, ларингоспазм или рвоту. Если такой рефлекс отсутствует или имеются сомнения в адекватной проходимости дыхательных путей используются воздуховод Гведела. При проведении ИВЛ, легкие вентилируются 100% О 2 с давлением менее 20 см вод.ст. Более высокое давление вызывает растяжение газом желудка, что повышает риск развития регургитациии ограничивает движения диафрагмы.
К интубации следует прибегать в следующих случаях:, а) апноэ; б) обструкция верхних дыхательных путей в) необходимость защиты нижних дыхательных путей от загрязнения рвотными массами или кровью; г) дыхательная недостаточность; д) угрожающие их или потенциальные нарушения проходимости дыхательных путей, например, после ожогов лица, продолжающихся судорогах после в/ в введения диазепама и пр. (профилактическая интубация); е) повышение ВЧД, требующее гипервентиляции.
Если продырявленная пластинка решетчатой кости цела, то методом выбора является назотрахеальнаяинтубация. При эндотрахеальной интубации у детей целесообразно использовать ларингоскоп с изогнутым клинком. Необходимый размер интубационной трубки примерно соответствует размеру большого пальца ребенка или ноздри. У всех детей до 7 лет следует использовать трубки без манжеток, поскольку необходима небольшая утечка газа вокруг трубки при раздувании легких. Конец интубационной трубки продвигается на 2—5 см (в зависимости от возраста) за голосовые связки. Для контроля положения трубки необходима билатеральная аускультация в подмышечных областях. Интубация детей даже с выраженными угнетениями сознания требует предварительной седации и введения миорелаксантов, что позволяет избежать повышения ВЧД во время ларингоскопии.
Детям с изолированной ЧМТ трахеостомия производится только в случаях неэффективности продленной интубации трахеи. При сочетанной челюстно-лицевой травме показаниями к трахеостомии могут быть невозможность интубации и эффективной санации дыхательных путей.
Переломы передней черепной ямки и костей носа иногда требуют проведения задней тампонады носа в связи с риском аспирации крови.
B. Вентиляция должна быть начата при первых же признаках неадекватности спонтанного дыхания. Если вентиляция маской с мешком неэффективна, необходима интубация трахеи с вентиляцией дыхательным объемом 10 мл/кг и частотой 30—40 в минуту у младенцев и 15—20 — у детей старшего возраста. Дыхательный объем должен равняться 10 мл/кг.
Почти все младенцы и дети в стрессовой ситуации заглатывают большое количество воздуха, а масочная вентиляция может еще увеличить его объем в желудке. Острая его дилятация значительно повышает риск рвоты и аспирации, ограничивает подвижность диафрагмы, сдавливает нижнюю полую вену и снижает венозный возврат. Поэтому введение желудочного зонда является важным профилактическим мероприятием в отношении указанных выше проявлений.
C. Состояние шока при изолированной ЧМТ может развиться только у младенцев, у которых травма сопровождается формированием обширной гематомы головы (вне- или внутричерепной), а также значимым кровотечением из раны скальпа. У более старших детей шок возможен при обширных ранах головы, повреждениях венозных синусов, а также нарушениях симпатического тонуса при тяжелой травме верхних шейных сегментов. Причем, чем младше ребенок, тем чаще шок принимает торпидное течение. У этих детей необходимо обеспечить тщательный мониторинг систолического артериального давления. Ранняя диагностика шока базируется на оценке цвета кожи, температуры конечностей, времени наполнения капилляров (в норме <2 секунд), ЧСС и АД. Степень шока и, следовательно, кровопотеря могут быть оценены по классификации шока (табл. 27—4).
Таблица 27—4. Классификация шока у детей
|
Критерии |
Тяжесть шока (объем кровопотери |
|||
|
1 степень (<15%) |
2 степень (15-25%) |
3 степень (25-40%) |
4 степень (>40%) |
|
|
Тахи/брадикардия |
||||
|
Систолическое АД и пульс снижены |
Систолическое АД и пульс резко снижены |
Тяжелая гипотензия, нетпериферического пульса |
||
|
Тахипноэ (30-40) |
Тахипноэ |
Брадипноэ |
||
|
Прохладная, на периферии холодная, влажная |
Холодная, влажная, цианоз |
Бледная, холодная |
||
|
Возбуждение, спутанность |
Летаргия | |||
|
Норма Удлиненное Резко удлиненное |
||||
* ВНК — время наполнения капилляров
Внутривенный доступ обеспечивается чрезкожным введением катетера в периферические вены. Если две попытки неудачны, следует попытаться катетеризировать верхнюю полую вену доступом через внутреннюю яремную или подключичную вены. При безуспешности — осуществляется венесекция (v.cephalica или v.saphena magna). Внутривенный доступ у детей с гиповолемией (со спавшимися венами) затруднен. В таких случаях может оказаться эффективной внутрикостная инфузия. Ее осуществляют через иглу, введенную перпендикулярно передней поверхности болыиеберцовой кости, на 3 см ниже ее бугристости. Правильность положения иглы подтверждается появлением элементов костного мозга в шприце при легкой аспирациии. При этом растворы вводятся под давлением (обычно шприцом) и они попадают в кровоток менее, чем через 30 сек. Катетеризация подключичной вены опасна, особенно у детей с гиповолемией и при необходимости должна осуществляться только опытным врачом. Начальная инфузионная терапия должна проводиться коллоидами (гелофузин, желатиноль) или 5% раствором альбумина (доза 20 мл/кг вводится болюсно). Пациенты с шоком 3—4 степени нуждаются в гемотрансфузии. Все жидкости должны быть подогреты до температуры тела.
Гемостатическая терапия осуществляется введением препаратов ингибиторов протеолиза: е-аминокапроновой кислоты — 5% раствор до 100,0 мл капельно в течении 8 часов; показано применение препаратов, улучшающих функцию тромбоцитов: дицинона (12,5% раствор 1,0—2,0 мл), адроксона (0,025% раствор по 0,5—1,0 мл в/м 1—3 раз в день), глюконата кальция (10% раствор по 1,0—5,0 мл в/м или в/в ежедневно). Возможно введение свежезамороженной плазмы в начальной дозе 10—15 мл/кг 2—3 раза в сутки в зависимости от клинической картины. После удаления гематом больших размеров нередко возникает необходимость в трансфузии цельной крови.
Для эффективного лечения постгеморрагических состояний у детей необходима их ранняя диагностика. Одними из наиболее чувствительных критериев при этом является содержание гемоглобина в крови и гематокрит. Их возрастные особенности представлены в табл. 27—5.
D. После стабилизации нарушений кардиореспираторной системы и лечения шока проводится полное физикальное обследование с целью раннего выявления факторов, приводящих к вторичным повреждениям головного мозга. Основным из них является церебральная ишемия вследствие респираторной недостаточности или снижения церебрального перфузионного давления (в связи с системной гипотензией или повышением ВЧД). Последнее определяется чаще всего отеком мозга и/ или массивными внутричерепными повреждениями. Первичное повреждение мозга предотвратить нельзя, а вторичное повреждение может быть уменьшено проведением окситенации и поддержанием адекватного церебрального перфузионного давления.
Таблица 27—5. Возрастные особенности содержания гемоглобина крови и гематокрита
Повышение ВЧД из-за диффузного церебрального отека — главная причина смерти у детей с ЧМТ. Получение данных по ШКГ менее 7 баллов является показанием для немедленного активного вмешательства. Начальный комплекс при этом включает в себя: возмещение ОЦК, эндотрахеаль-ную интубацию, адекватную оксигенацию (Sat>90%), гипервентиляцию (РаСО 2 30—35 мм рт.ст.) и назначение маннитола в дозе 0,25—0,5 г/кг.
При возникновении судорог, с целью профилактики их повторения с последующим повышением ВЧД, внутривенно вводится диазепам в дозе 0,15—0,25 мг/кг. Он может вызвать депрессию дыхания, поэтому нужно быть готовым к проведению ивл.
Детям в критических состояниях снижаются дозы всех медикаментов, так как гиповолемия и гипотензия меняют распределение и фармакокинетику лекарств, усиливая их клинический эффект.
Активные лечебные мероприятия продолжаются в стационаре. При тяжелых механических повреждениях (например, падениях с высоты, дорожно-транспортных происшествиях и т.д.) ребенок сразу после поступления в приемное отделение больницы осматривается бригадой врачей, включающей нейрохирурга, реаниматолога, общего хирурга и травматолога. Нередко возникает необходимость в привлечении и других специалистов (например, челюстно-лицевых или пластических хирургов).
Если в результате комплексного обследования ребенка не обнаружено травматических изменений, требующих хирургического лечения, а состояние ребенка тяжелое, ведущая роль в определении тактики консервативного лечения принадлежит реаниматологу. В этих случаях нейрохирург чаще всего осуществляет лишь динамическое наблюдение за ребенком с целью раннего выявления возможных осложнений и своевременного применения хирургических методов лечения.
Если ребенок ранее не интубирован, в первую очередь решается вопрос о необходимости эндотрахеальной интубации. В условиях стационара показания к интубации следующие: а) отсутствие рефлексов на роторасширитель при отсасывании из рта и ротоглотки у детей, находящихся в бессознательном состоянии; б) необходимость защиты дыхательных путей при продолжающемся орофарингеальном кровотечении; в) неадекватность спонтанного дыхания по клиническим или лабораторным данным (РаО 2 <9 кПа при дыхании воздухом или <13 при дополнительной оксингенации; РаСО 2 >5,3 кПа); г) необходимость проведения гипервентиляции для снижения ВЧД.
Важное значение имеет профилактика и коррекция нарушений системной гемодинамики. Динамическое равновесие между артериальным давлением и ВЧД обеспечивает стабильность перфузии головного мозга. Нарастание ВЧД обычно сопровождается компенсаторным повышением систолического АД. Эпизоды снижения АД чреваты углублением имеющихся гипоксических повреждений мозга или возникновением новых зон инфарктов. Вместе с тем, значительное повышение АД может спровоцировать развитие вазогенного отека мозга. Именно поэтому поддержание АД в пределах, несколько более высоких, чем возрастные нормы, является важной задачей. Для се реализации в первую очередь надо обеспечить надежный венозный доступ. При низком АД инфузия проводится в 2—3 сосуда. Продолжаются противошоковые мероприятия, включающие использование кристаллоидов (раствор Рингера, Рингера-Локка). Их количество прямо пропорционально глубине шока и направлено на восполнением дефицита ОЦК в объеме 300—400% от исходного (соотношение крови и плазмозаменителей 3:1). Из коллоидных растворов чаще используются полиглюкин, реополиглюкин 8—10 мл/кг. Если применение этих мероприятий не обеспечивает должного уровня АД, проводится инотропная поддержка (например, допамин по 3—8 мкг/кг в мин.).
У детей с ЧМТ целесообразно придерживаться принципа умеренной гемоделюции. При стабилизации гемодинамики объем инфузии определяется диурезом и проводится в режиме дегидратации, выраженность которой зависит от внутричерепной ги-пертензии.
Сразу после выведения ребенка из шока и обеспечения адекватной вентиляции легких решается вопрос о целесообразности проведения рентгенографии шеи. Она показана при наличии: а) анамнестических сведений о шейно-затылочной травме;
б) внешних признаках механического воздействия на шейную область (ссадины, отечность и пр.);
в) фиксированного положения головы;
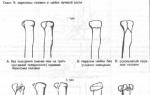
г) болезненности при пальпации шеи и/или легких движениях головой; д) неврологических расстройств, указывающих на повреждение шейного отдела спинного мозга. Рентгенограмма ввтполняется в двух проекциях. Для получения боковых снимков используют горизонтальный ход луча. Особое значение должно придаваться повреждениям С1 и С2 позвонков. Их состояния оцениваются по боковой и трансоральной рентгенограммам. Изучается симметричность атланто-аксиальных сочленений и состояние сустава Крювелье. Необходимо помнить, что у детей младших возрастных групп возможны грубые поперечные повреждения спинного мозга даже при рентгенологически интактном позвоночнике.
До исключения перелома шейного отдела позвоночника соблюдается особая осторожность при перекладывании детей или их транспортировке. Необходимо избегать переразгибания шеи (в т.ч. во время санации или интубации).
Одной из важнейших лечебных задач является профилактика и лечение внутричерепной гипертеизии. Различаются две основные группы причин, приводящих к нарастанию внутричерепной гипертензии: а) внутричерепные причины (отек мозга, гематомы, инфаркты, тяжелые ушибы, судорожные припадки, менингит); б) внечерепные причины (гипокапния, гиперкапния, гипонатриемия, неадекватные седагдия и вентиляция).
В настоящее время используются различные схемы коррекции высокого ВЧД, однако неоспоримых доказательств преимущества того или иного подхода пока нет, что затрудняет выработку единых стандартов терапии.
Голова ребенка должна быть расположена в нейтральной позиции, а головной конец кровати поднят на 30° (для облегчения венозного оттока из полости черепа). Все процедуры, которые могут вызвать сопротивление пациента и вторичный подъем ВЧД (например, санация дыхательных путей, повороты больного, болезненные манипуляции и пр.) должны выполняться под седацией (барбитураты короткого действия илидиазепам) и, если возможно, анальгезией. Обезболивание необходимо даже если пациент получает миорелаксанты.
У детей с тяжелой ЧМТ возможно субклиническое течение эпилептических припадков, не сопровождающееся видимыми двигательными феноменами, но приводящее к нарастанию ВЧД. Поэтому полезно проведение ЭЭГ детям, находящимся в коме.
Наиболее быстрый и эффективный вид терапии повышенного ВЧД является гипервентиляция. Она может быть выполнена как мешком с маской, так и интубацией с использованием механической вентиляции. Если у пациента имеется спонтанное дыхание, несинхронизированное с аппаратом ИВЛ, то увеличение внутри грудного давления будет повышать и ВЧД. Для синхронизации используется седация (диазепам, барбитураты) и миорелаксанты (панкурониум). РСО 2 артериальной крови следует снизить до диапазона 25—30 мм рт. ст.
Уменьшение содержания жидкости в мозге может быть достигнуто путем ограничения ее приема до 75% от физиологической потребности и с помощью использования осмотических или петлевых диуретиков. Осмотические агенты включают маннитол, который наиболее широко используется, мочевину и глицерол. Осмотический диуретик сначала увеличивает внутрисосудистый объем, поэтому, в отсутствии нормальной ауторегуляции, может принести к кратковременному увеличению ВЧД.
В зависимости от степени внутричерепной гипертензии применяют следующие фармакологические схемы.
1. При умеренной внутричерепной гипертензии (в пределах 150—200 мм вод. ст.) в течение 2—3 дней применяются лазикс (0,5—1 мг/кг/сутки) с коррекцией гипокалиемии.
2. При выраженной внутричерепной гипертензии (200—300 мм вод. ст.) применяются маннитол 0,25—0,5 г/кг 1 раз в сутки, преднизолон 3—5 мг/кг
или дексазон 0,5—0,8 мг/кг, увеличивается доза лазикса до 1—2 мг/кг (длительность дегидратационной терапии обычно составляет 5—7 дней).
3. В случаях резко выраженной внутричерепной гипертензии (более 300 мм вод. ст.) и с целью снижения риска возникновения феномена «отдачи» целесообразно чередование маннитола с лазиксом 1,5—3 мг/кг и альбумином 5—10 мг/кг каждые 6—8 часов. Возможно изолированное применение лазикса 4—6 раз в сутки без маннитола. В схему терапии включаются преднизолон (7— Юмг/кг) или дексазон (0,8—1,5 мг/кг).
Возможно использование глицерола энтераль-но (через рот или через желудочный зонд) в дозе 0,5—2,0 г/кг, а внутривенно в виде 10% раствора в дозе 1,0 г/кг (в течение 30 минут). Применение глицерола внутривенно может приводить к гемолизу.
Использование больших доз осмотических диуретиков требует контроля осмолярности плазмы, которая не должна превышать 320 мОсм.
Ограничение жидкости и диуретический эффект могут легко привести к гипотензии. Этого следует избегать ввиду отрицательного ее эффекта на пер-фузионное давление мозга.
Стероиды могут использоваться в лечении внутричерепной гипертензии и эффект связан с их способностью стабилизировать клеточные мембраны и уменьшать церебральный отек. Хотя они обычно используются в лечении травматического отека головного мозга, их эффективность не бесспорна.
Повышение температуры тела увеличивает метаболическую потребность мозга и церебральный кровоток, как следствие нарастает ВЧД. Поэтому гипотермия может оказаться полезным дополнением в лечении внутричерепной гипертензии. При использовании охлаждающих покрывал и антипиретиков температура тела может быть уменьшена до 30-32*С.
При неэффективности других средств лечения высокого ВЧД может быть использована кома, вызванная барбитуратами, которые в больших дозах уменьшают метаболическую потребность мозга и уменьшают мозговой кровоток. Лечебный эффект также связан со способностью барбитуратов удалять свободные радикалы, что может помочь сохранить целостность клетки.
Следует помнить, что барбитураты в высоких дозах, существенно уменьшая системное сосудистое сопротивление, в условиях гиповолемии и диуретической терапии, могут привести к резкой артериальной гипотензии. Поэтомубарбитуровая кома нередко требует предварительного восполнения ОЦК, прессорной терапии и мониторинга системного артериального давления.
Барбитуровая кома достигается, например, внутривенным введением тиопентала в начальной дозе 3,0—5,0 мг/кг и последующей поддерживающей инфузией 1,0—2,0 мг/кг/час (поддержание уровня в плазме 3,0—4,0 мг/дл). Критерий адекватности — значительное уплощение ЭЭГ.
Изменения в схеме противоотечной терапии производятся только через 24 часа после достижения необходимого ВЧД и осуществляются постепенно. Интервал между последовательными изменениями в терапии должен быть как минимум 6—8 часов. В первую очередь отменяются инвазивные процедуры. Поэтому барбитуровая кома должна быть отменена в первую очередь.
Неконтролируемая внутричерепная гипертензия является показанием для декомпрессивной трепанации. Некоторые авторы сомневаются в целесообразности таких операций, объясняя это недоказанностью их эффективности.
При критическом состоянии у детей с клиникой вклинения и верифицированной гематомой на этапе подготовки к ургентной операции оправдано применение мегадоз маннитола (до 1—2 г/кг).
Одним из основных условий выбора оптимальной тактики лечения внутричерепной гипертензии является мониторный контроль ВЧД. Имплантация датчиков для мониторинга ВЧД целесообразна при коме с оценкой по ШКГ менее 8 баллов, КТ-данных, указывающих на отек головного мозга, сдав-ление цистерн и дислокацию структур средней линии. Критерии прекращения мониторинга — нормальное ВЧД в течение 48 часов и четкая положительная динамика при повторных КТ.
С целью седации и анальгезии сильные опиаты и другие лекарства с депрессирующим эффектом на дыхание не применяются, поскольку они могут стать причиной ятрогенного изменения уровня сознания и дыхательной депрессии. Старшим детям назначают парацетамол 250—500 мг каждые 6 часов, детям младшего возраста — 10—15 мг/кг каждые 6 часов.
Для профилактики тошноты и рвоты используются метоклопрамид (церукал) в дозе 0,25—0,5 мг/кг каждые 8 часов в/м или перорально.
Антибиотики показаны при переломах основания черепа, открытых переломах свода черепа, а также при подозрении на менингит. Выбор антибиотика при установленной пневмонии, ранах, или внутричерепной инфекции должен осуществляться на основании определения возбудителя и его чувствительности к препарату. Профилактической дачи антибиотиков следует избегать, и их ценность спорна, поскольку усиливается риск развития резистентной инфекции.
Судорожный синдром у детей с ЧМТ требует исключения компрессии мозга, назначения противосудорожной терапии и усиления дегидратации. Судороги, развившиеся в течение первой недели после ЧМТ, редко приводят к развитию эпилепсии в дальнейшем, однако они могут вызвать дополнительные ишемические повреждения мозга. Поэтому, в случаях возникновения припадка, с целью предотвращения повторения судорог проводится противосудорожная терапия. Например, используют клоназепам 0,25 мг в/в, увеличивая дозу после каждого приступа. Если судороги не купируются, возможно внутривенное введение диазепама в дозе 0,15—0,3 мг/кг, однако, он может вызвать респираторную депрессию. Используется также натрия оксибутирата 20% раствора (100—150 мг/кг в/в медленно); фенобарбитал (доза насыщения в первый день 20 мг/кг, в последующем 3—4 мг/кг внутрь). Для профилактики судорог и для повышения эффективности других средств, в частности, фенобарбитала, показано применение дифе-нина (доза насыщения 20 мг/кг/с, поддерживающая доза 5 мг/кг/с); карбамазепина (финлепсина, тегре-тола) с начальной дозой 5 мг/кг/с с возможным повышением дозы до 10—20 мг/кг/с; антелепсина (0.4 мг/кг/с); бензонала (5 мг/кг/с).
Для снижения потребности мозга в кислороде используют антигипоксаиты". ГОМК (в виде 20% раствора 100—150 мг/кг/сут) с коррекцией гипо-калиемии, высокие дозы барбитуратов (тиопентал натрия 10—15 мг/кг микроструйно медленно или парентеральное двухратное введение фенобарбитала по 10 мг/кг); эффективно внутривенное применение пирацетама (однократная доза 200—240 мг/кг до 2—6 г в сутки). Инфузии должны проводиться медленно, капельно (за исключением случаев шока), избегая артериальной гипертензии и перегрузочной полицитемии, что может существенно ухудшить мозговой кровоток.
Из сосудистых препаратов сразу после травмы можно назначать трентал (2% раствор 0,1 мл/кг) или эуфиллин (2,4% по 10,0). Препараты, способные значительно увеличить кровенаполнение мозга (например, сермион, кавинтон), назначаются после разрешения отека мозга и достижения надежного гемостаза (на 8—9 сутки после травмы).
Для предотвращения вторичных ишемических повреждений применяют ингибиторы протеолиза (контрикал 50 тыс. ед в сутки), мегадозы цереброли-зина (10—30 мл внутривенно), антагонисты Са — нимотоп (с 3—5 суток после ЧМТ внутривенно, по 5 мл в течение первых двух часов, затем при отсутствии заметного падения АД вводится еще 10 мл, курс лечения 5—10 дней).
Для обезболивания применяется внутримышечное введение 50% анальгина по 0,5—1,0 мл. Эффективно использование смеси димедрола, анальгина и седуксена. При сильных болях применяется нейролептанальгезия — внутривенно вводят 0,25% раствор дроперидола в дозе 0,3—0,5 мг/кг, 0,005% раствор фентанила в дозе 0,0025 мг/кг. Возрастные дозы растворяются в 10 мл 5— 10% раствора глюкозы и вводятся очень медленно внутривенно. Возможно угнетение дыхания.
Одной из важнейших задач является профилактика и лечение воспалительных осложнений, которая должна проводиться с первых часов после ЧМТ. Пневмония может возникать уже спустя 12—24 часа после травмы. Для ее профилактики при тяжелой ЧМТ назначаются антибиотики широкого спектра действия, интратрахеально или путем ингаляций вводится по 10 мг трипсина в 8—10 мл физиологического раствора, проводится санация полости рта и трахеи, стимуляция кашля. Применяются иммуностимулирующие препараты (левамизол по 150 мл однократно в течение 3 дней, повторный курс через 4 дня).
Грозным осложнением является развитие менингита. Основа диагноза — анализ ликвора с выявлением нейтрофильного цитоза. Дополнительные сложности возникают в ранней диагностике менингита у детей с массивными субарахноидальными кровоизлияниями. В этих случаях помогает знание пропорции лейкоцитов и эритроцитов при отсутствии воспаления, она равна 1:600, 1:700. При менингите используются мегадозы пенициллина, ами-ногликозиды или цефалоспорины.
При необходимости применяется эндолюмбальное введение цефалоспоринов, канамицина, левомицетина гемисукцината (все в дозировке до 50— 100 мг).
Парентеральное питание обеспечивается внутривенным введением мелкодисперсных жировых эмульсий (липофундин, интралипид), белковых препаратов (альбумин, протеин, плазма), растворов аминокислот (левамин, аминостерил) и витаминов (группы В и С). Постепенно парентеральное питание заменяется на энтеральное через желудочный зонд. Последний через каждые 2—3 дня переставляется то в одну, то в другую половину носа. Перед каждым кормлением полость желудка промывается кипяченой водой. Для кормления можно использовать детские молочные смеси, белковое питание для спортсменов, фруктовые и овощные соки.
При определении общей тяжести состояния и его динамики важным является оценка степени нарушения жизненно важных функций. В табл. 27—6 приводятся критерии такой оценки в зависимости от возраста ребенка.
По мере восстановления сознания переходят на таблетированные препараты: ноотропил, пантогам (при повышенной нервнорефлекторной возбудимости); пиридитол (энцефабол, пиритинол, пиритиоксин), глутаминовая кислота. При выраженном астеническом синдроме используют ацефен (0,05—0,1 3—4 раза в день); адаптогены (дибазол, жень-шенъ, элеутерококк). Применяются также средства, способствующие миелинизации нервной ткани: витамины В1, В6, В12, В15; церебролизин, актовегин.
Таблица 27—6
— таблица составлена совместно с сотрудниками кафедры неотложной медицины СПб МАПО доц. Г.А. Лысовым и асе. Б.А. Бичуном;
** — приведенные абсолютные значения отражают систолическую составляющую АД.
Ряд авторов считает обязательным назначение противосудорожных препаратов в течение 6—12 мес после среднетяжелой и тяжелой ЧМТ], а другие считают, что противосудорожное лечение показано только детям с судорогами в анамнезе или с отягощенным фоном.
Большое значение среди методов ранней реабилитации имеют массаж, ЛФК, а при патологических установках конечностей — использование лечебных ортопедических укладок.
В завершении этой главы хотелось бы еще раз подчеркнуть сложность проблемы ЧМТ у детей и нерешенность многих организационных вопросов при оказании помощи детям с этим видом патологии. Основное противоречие заключается в следующем. С одной стороны, назрела необходимость стандартизации лечебно-диагностических мероприятий, а с другой — они не могут быть универсальными, поскольку уровень технического оснащения регионов России значительно отличается друг от друга. Поэтому целесообразно, очевидно, разработать несколько их вариантов, в зависимости от того, какая модель оказания помощи реализуется в конкретном регионе. Безусловно, это только временный выход, это лишь шаг на пути к использованию единых стандартов.
Однако этот шаг необходим, поскольку делает реальной перспективу повышения эффективности оказания медицинской помощи детям с ЧМТ в России уже в ближайшее время.
А.А. Артарян, А.С. Иова, Ю.А. Гармашов, А.В. Банин
Оказание медицинской помощи детям с ЧМТ принципиально не отличается от таковой у взрослых и включает оказания медицинской помощи на догоспитальном этапе и при поступлении в стационар (специализированная помощь). Современные взгляды на лечение черепно-мозговой травмы концентрируют внимание на раннем выявлении и устранении вторичных внутричерепных и внечерепных факторов, развивающихся после первичного травматического поражения мозга. Они включают мероприятия на системном уровне (артериальное давление, внутричерепное давление, перфузионное давление, вентиляция и газообмен, биохимический гомеостаз, терморегуляция, снятие перевозбуждения нервной системы и гормональной систем), на органном уровне (церебральная ликвородинамика, гематоэнцефалический барьер), на тканевом уровне (оптимизация метаболизма, уменьшение отека-набухания мозга), на клеточном уровне (защита нейронов путем подавления явлений воспаления, нейтрализация свободных радикалов и перекисного окисления липидов, содержания Са2+).
Основной задачей на догоспитальном этапе оказания помощи ребенку с ЧМТ является обеспечение витальных функций организма - дыхания и гемодинамики. Это восстановление проходимости дыхательных путей, обеспечение адекватной вентиляции легких, остановка наружного кровотечения, нормализация артериального давления и объема циркулирующей крови. Проведение этих мероприятий начинается на месте происшествия, продолжается при транспортировке и поступлении в стационар. Задержка в их проведении, особенно у детей, нередко приводит к негативному результату всего комплекса лечебных мероприятий при ЧМТ.
Условно комплекс лечебно-диагностических мероприятий при поступлении пострадавшего с ЧМТ в стационар можно разделить на неотложные, срочные и плановые.
Неотложные мероприятия направлены на стабилизацию витальных функций организма и являются прямым продолжением помощи, проводимой на догоспитальном этапе. Условия их проведения в стационаре более благоприятны и расширены. Они включают обеспечение адекватной вентиляции и оксигенации, стабилизацию артериального давления и восполнение, по необходимости, объема циркулирующей крови, устранение болевого синдрома, психомоторного возбуждения, судорожного синдрома. Все дальнейшие диагностические и лечебные мероприятия проводятся после стабилизации витальных функций.
Срочные мероприятия являются непосредственным продолжением неотложных мероприятий и направлены на проведение всего комплекса лечебнодиагностических мероприятий для решения вопроса дальнейшей тактики лечения. Осуществляется оценка неврологического статуса с учетом обстоятельств травмы, рентгенологическое (КТ, краниография) и ультразвуковое (ЭхоЭГ, НСГ) обследование. Это позволяет выделить группы больных:
1) требующих срочного оперативного лечения;
2)
требующих интенсивной терапии в отделении интенсивной терапии и реанимации;
3) требующие консервативной плановой терапии в условиях нейрохирургического или неврологического отделения.
Особую группу составляют пострадавшие, у которых вопрос о хирургическом лечении либо может быть отсрочен, либо вопрос об операции определяется динамикой развития патологического процесса. Это больные с небольшими вдавленными закрытыми переломами костей свода черепа, незначительной назо- и отореей, ушибами мозга и внутричерепными гематомами без выраженного отека мозга и дислокационного синдрома, находящиеся в субкомпенсированном состоянии.
Показаниями к срочному нейрохирургическому вмешательству является наличие внутричерепных гематом, вдавленных переломов, тяжелых очаговых ушибов мозга, сопровождающихся дислокацией и сдавлением мозга, напряженной пневмоцефалии, открытых проникающих черепно-мозговых ранений, приводящих к сдавлению мозга и развитию компрессионно-дислокационного синдрома.
Показаниями к госпитализации в отделение интенсивной терапии и реанимации являются: нарушения или нестабильность витальных функций; нарушение сознания ниже 8 баллов по шкале Глазго, обнаружение на КТ признаков дислокационного синдрома, не подлежащего хирургическому лечению; психомоторное возбуждение.
Консервативной плановой терапии требуют больные с сотрясением и ушибами мозга легкой- средней степени тяжести.
Основные принципы и особенности консервативной терапии сотрясения головного мозга у детей
Главное значение в лечебных мероприятиях при сотрясении головного мозга придается созданию психо-эмоционального покоя. Это достигается путем ограничения двигательной активности (постельный или полу постельный охранительный режим) на 7-8 дней.
Возрастной диапазон детей с черепно-мозговой травмой от новорожденных до подростков требует учета морфофункциональных особенностей их организма и особенностей фармакодинамики применяемых лекарственных препаратов. Дозы лекарственных средств рассчитываются на килограмм массы тела, на единицу площади тела ребенка или по возрасту. Обычно они приводятся в рецептурных справочниках или в рекомендациях производителя лекарств. При отсутствии их детская доза рассчитывается исходя из возраста ребенка: грудной возраст - 1/25 дозы взрослого, в 1-2 года - 1/12 - 1/8, в 3-6 лет - 1/6 - 1/4, в 7-10 лет - 1/3, в 11-14 лет - 1/2 дозы взрослого. Характерно, что чем младше ребенок, тем менее активно используется медикаментозная терапия и большее значение придается охранительному режиму. С увеличением возраста усиливаются клинические проявления сотрясения мозга и увеличивается число жалоб, что требует соответствующей терапии.
Широко применяются успокаивающие препараты: натрий бромид в виде 3% раствора (микстура) по столовой ложке 3-4 раза в день после еды; настой корня валерианы или травы пустырника, бром - кофеиновая микстура в той же дозировке. Значительно реже у детей приходится прибегать к более мощным седативным средствам: седуксен, феназепам, нозепам, тазепам, элениум, диазепам, рудотель, сибазон.
Выраженность вегето-сосудистых нарушений обосновывает применение антигистаминных десенсибилизирующих препаратов (выборочно): димедрол 0,002 - 0,05 внутрь или 0,005 - 0,02 в свечах 1-3 раза в день, при необходимости препарат вводится внутримышечно 1% по 1 - 2 мл; супрастин 0,025 внутрь или 1- 2% раствор по 1 мл внутримышечно; тавегил по 0,001 внутрь, по 0,01 в свечах или 0,1% раствор 1-2 мл внутримышечно; диазолин по 0,005 - 0,1 внутрь; пипольфен 2,5% раствор 1-2 мл внутримышечно.
Болевой синдром купируется (выборочно): аспирином по 0,25 внутрь 2-3 раза в день после еды; таблеттированными формами содержащими аспирин, фенацетин, кофеин (аскофен, новоцефалгин, цитрамон); аналгином по 0,1 - 0,5 внутрь 2-3 раза в день; пенталгином по 1 таблетке 2-3 раза в день; парацитамолом по 10-15 мг/кг через 6 часов; баралгином по 1 таблетке 2-3 в день; седалгином по 1 таблетке 2-3 раза в день; темпалгином по 1 таблетке 2-3 раза в день. Реже приходится прибегать к инъекциям 50% раствора аналгина по 0,1-1 мл внутримышечно, эффективнее в сочетании с димедролом 1% раствор по 1 мл и седуксеном (диазепам, валиум) 0,1% раствор по 1-2 мл; трамала по 0,1 мл/кг внутривенно. При упорных головных болях, головокружении, рвотах используют введение 25% сернокислой магнезии по 0,1 - 0,2 мл/кг внутримышечно на новокаине; церукал (метоклопрамид) по 0,24 - 0,5 мг/кг внутрь или внутримышечно; пипольфен 2,5% раствор по 1 мл внутримышечно.
Редко используются спазмолитики: эуфиллин по 0,15 внутрь или по 20-40 мл 1% раствора в клизмах, реже в виде внутривенных инъекций по 0,1мл/кг 2,4% раствора на 10-40 мл 40% глюкозы; дибазол по 0,02 внутрь; но-шпа по 0,04 внутрь.
При выраженных головокружениях применяется: беллоид по 1-2 драже 3 раза в день; белласпон по 1 драже 3 раза в день, танакан
Эффективно применение таких вазотропных препаратов как стугерон (циннаризин) по 0,25 внутрь 3 раза в день; трентал по 0,1 мл/кг 2% раствора, курантил 0,5% раствор по 0,05 - 0,1 мл. Они хорошо комбинируются с ноотропными препарата ми: ноотропил в капсулах по 0,2 внутрь 2-3 раза в день, пирацетам по 200-300 мг/кг в день, пиридитол (пиритинол, пиритиоксин) по 0,05 или по 1 мл сиропа 2-3 раза в день.
Необходимость в проведении дегидратационной терапии при сотрясении головного мозга у детей возникает относительно редко. Применяют диакарб из расчета 10-15 мг/кг или фурасемид 1-2 мг/кг на фоне приема панангина (аспаркама) по 1 драже 3 раза в день, оратата калия по 0,25 внутрь 2-3 раза в день.
Развивающуюся астению удается купировать назначением пантагама по 30-50 мг/кг 3 раза в день; ацефена по 0,05-0,1 3 раза в день; адаптогенов (лимонник, жень-шень, элеутерококк ); когитум по 10 мл внутрь 2 раза в день; церебролизина 5% раствор по 1-2 мл внутримышечно; липоцеребрина 0,1-0,25 внутрь по 2 раза в день; аминалона (гаммалона) по 0,25 внутрь 2-3 раза в день; актовегина по 200 мг внутрь 3 раза в день или по 2-5 мл (80-200 мг) внутримышечно; инстенона по 1/2-1 таблетке 2-3 раза в день или по 0,05-0,1 мл/кг внутримышечно.
На длительное время назначаются витамины С и В, поливитамины.
Сроки пребывания больных в стационаре обычно ограничиваются одной неделей с сохранением домашнего охранительного режима еще на 7-10 дней. При достаточном техническом оснащении стационаров (КТ, НСГ),позволяющих исключить более тяжелых повреждений мозга, сроки госпитализации детей могут быть сокращены до 3-4 дней. Ряд зарубежных руководств рекомендуют даже пребывание ребенка дома под наблюдением врача.
Основные принципы консервативной терапии черепно-мозговой травмы средней степени тяжести (ушибы мозга легкой-средней степени тяжести) у детей
Ушибы легкой-средней степени тяжести в младшей возрастной группе практически по клиническим проявлениям не отличаются от сотрясения мозга. В старшей возрастной группе более длительна потеря сознания, более выражена ретроградная амнезия, сильнее и более длительное время сохраняются клинические проявления (головные боли, головокружения, тошноты, вегето-сосудистые нарушения, очаговые неврологические проявления). Следует учитывать, что у детей нередко преморбидный фон определяет выраженность и длительность проявлений ушиба мозга легкой- средней степени тяжести.
Сохраняя общие принципы лечебных мероприятий как и при более легкой черепно-мозговой травме, при травме средней степени тяжести обоснованы мероприятия, направленные на предупреждение вторичных ишемических нарушений мозгового кровообращения, на нормализацию обмена нейромедиаторов, снижение иммунных реакций на антигены поврежденной нервной ткани, на стимуляцию репаративных процессов в ней, предупреждение и купирование интра- и экстракраниальных воспалительных осложнений. При обнаружении субарахноидального кровоизлияния применяется гемостатическая терапия, а при развитии судорожного синдрома - комплекс противосудорожных мероприятий.
Для предупреждения вторичных ишемических нарушений хорошо себя зарекомендовали ингибиторы протеолиза (контрикал по 10 тыс. ЕД, гордокс по 100 тыс. ЕД, трасилол по 50 000 ЕД в сутки внутривенно капельно на физиологическом растворе). Они хорошо сочетаются с церебролизином по 10 - 30 мл внутривенно, тренталом 2% по 0,1 мл/кг.
Для нормализации обмена нейромедиаторов рекомендуются препараты Л-ДОФА (мадопар по 0, 05 2-3 раза в день), препараты, содержащие ионы Mg ++ (25% раствор сернокислой магнезии из расчета 0,2 мл/кг внутривенно). Репаративные процессы стимулируются ноотропами (ноотропил, пирацетам, пиридитол, пиритинол, пиритиоксин, энцефабол), церебролизином, глиатилином.
Снижение иммунологических реакций на антигены нервной ткани достигается приемом антигистаминных препаратов (дипразин по 0,025 г 2-3 раза в день, димедрол по 0,1 г 2-3 раза в день, тавегил по 0, 001 г 2-3 раза в день), иммуномодуляторов (дикарис, тимонил, Т-активин, пентаглобин).
Противосудорожная терапия у детей с черепно-мозговой травмой обоснована при развитии судорожного синдрома после травмы, то есть для его купирования, а также для профилактики развития отсроченной эпилепсии.
Для купирования судорожного синдрома используются: клонозепам по 0,01 - 0,04 мг/кг внутривенно, а затем диазепам 0,2 - 0,4 мг/кг внутривенно (возможно ректальное введение препарата по 5-10 мг) или лоразепам по 0,05 - 2,0 мг/кг внутривенно. Если эти препараты не купируют приступ, используют: фенитоин по 10 - 20 мг/кг внутривенно, натрий оксибутират 20% по 100-150 мг/кг внутривенно или седуксен 0,5% по 0,5 мг/кг внутривенно, фенобарбитал по 4-10 мг/кг внутривенно. Продолжающийся приступ требует перехода на общую анестезию с применением тиопентала натрия по 5 - 15 мг/кг внутривенно или пропофола (болюсная доза 1-3 мг/кг и перфузионная доза 2-4 мг/кг).
Частота развития поздней (после 3 месяцев) посттравматической эпилепсии составляет около 10% всех случаев тяжелой и средней тяжести ЧМТ. Она значительно выше при открытой травме, травме осложненной ликвореей, инфекцией, при потере сознания более 24 часов после травмы, при ранних появлениях эпиприпадков.
Для лечения поздней посттравматической эпилепсии обычно применяется принцип монотерапии. Рекомендуют: карбамазепин (тимонил, финлепсин, тегритол) по 5-10 мг/кг 3 раза в сутки, фенитоин (дифенин) по 3 - 5 мг/кг 2 раза в сутки, клонозепам (антилепсин) по 0,05 -0,1 мг/кг 2-3 раза в сутки, вальпроевую кислоту (депакин, орфирил) по 10- 20 мг/кг 2-3 раза в сутки, примидон по 5 - 10 мг/кг
2-3 раза в сутки при парциальных и тонико-клонических судорогах. Реже используется бензонал 5 мг/кг в сутки. При абсансах хорошо себя зарекомендовал этоксуксимид по 5 - 15 мг/кг 2-3 раза в сутки. Только безэффективность монотерапии обосновывает переход на комбинированное лечение (политерапия).
Международная противоэпилептическая лига рекомендует применение при генерализованных приступах 3 ряда препаратов в зависимости от эффекта. Начинают лечение с препаратов первого ряда - депакин (вальпроат). При его недостаточной эффективности переходят ко второму ряду - ламиктал . И только его неэффективность обосновывает применение препаратов третьего ряда - карбамазепин, клоназепам, фенитоин, фенобарбитал.
У детей младшего возраста (новорожденные) хорошо зарекомендовал себя фенобарбитал по 10-30 мг/кг внутрь или внутривенно, поддерживающая доза - 5 мг/кг в 2-3 приема, не превышая суточной дозы 40 мг/кг. Препаратом второго ряда (при неэффективности фенобарбитала) используется дифенин (фенитион) внутривенно медленно до 50 мг/мин, поддерживающая доза 2,5 - 4 мг/кг, а при его неэффективности применяют лоразепам внутривенно по 0,05 мг/кг, оксибутират натрия, гексенал или тиопентал натрия, миорелаксанты (ардуан, листенон) с переводом ребенка на ИВЛ.
Особая осторожность применения противосудорожной терапии с профилактической целью у детей связана с тем, что действие эпилептогенных разрядов и противоэпилептических препаратов происходит у детей на тех стадиях созревания мозга, когда он особенно раним и чувствительность к вредным воздействиям. Способность к приобретению многочисленных культурных и жизненно-практических навыков убывает с возрастом, поэтому применение противосудорожных препаратов в раннем возрасте требует особого подхода, так как может резко снизить способности ребенка к обучению. В международных «Рекомендациях по лечению тяжелой ЧМТ» вообще не рекомендуется профилактическое применение фенитиона, карбомазепина, фенобарбитала или вальпроата для предупреждения поздних посттравматических припадков. Их назначение оправдано только в группе высокого риска, к которым относятся пострадавшие с наличием корковых ушибов мозга, с вдавленными переломами свода черепа, с внутричерепными гематомами, с проникающими ранениями, с судорожным синдромом в первые 24 часа после травмы, с нарушениями сознания ниже 10 баллов по шкале ком Глазго. У детей, кроме того, к группе высокого риска следует отнести пациентов с последствиями родовой травмы, с наличием эпиприступов в анамнезе и при обнаружении судорожной готовности мозга на ЭЭГ после травмы.
Важное значение в лечебных мероприятиях при черепно-мозговой травме средней степени тяжести принадлежит профилактике и лечению воспалительных осложнений, нередко определяющих течение и исходы травмы. Среди интракраниальных осложнений наиболее грозными являются менингиты, менингоэнцефалиты и абсцессы мозга, а среди экстракраниальных - пневмонии.
Главной причиной развития гнойных осложнений у детей с черепно-мозговой травмой: являются госпитальная инфекция, бациллоносительство, нарушение асептики и снижение сопротивляемости организма больных. Частота интракраниальных гнойных осложнений при «чистых» плановых нейрохирургических операциях составляет 3-5%, а при ургентных вмешательствах она повышается до 10%. В детской нейрохирургической практике частота этих осложнений возрастает из-за незавершенного формирования иммунной системы ребенка, большого числа пациентов, относящихся к группе высокого риска (ранний детский возраст, наличие пороков развития, соматическая патологии, длительное применение кортикостероидов и т.д.).
В этиологической структуре возбудителей, выделенных из ликвора, раневого экссудата, отделяемого трахеобронхиального дерева в 1992-1996 гг., на нашем материале отмечалось доминирование грамотрицательной микрофлоры: энтеробактерий, ацинетобактеров, синегнойной палочки. Грамположительные возбудители были представлены стафилококками, преимущественно эпидермальными, стрептококками.
В последние годы отмечается стойкая тенденция к доминированию грамотрицательной микрофлоры с увеличением частоты выделения Acinetobacter baumannii , уменьшения частоты выделения Pseudomonas aerugi nosa и сохранением частоты выделения Enterobacteriaceae . Среди грамположительных возбудителей наблюдается снижение частоты выделения стафилококков, особенно S . Epidermidis , и повышение частоты выделения Enterococcus spp . и Streptococcus spp . Учет изменения резистентности микроорганизмов к антибиотикам и изменения состава самой флоры потребовал коррекции профилактических и лечебных мероприятий. Практически пришлось отказаться от применения гентамицина (резистентность в 80-96% наблюдений), сократить применение цефалоспоринов II - III поколения (цефокситин, цефотаксим, цефтриаксон), фторхинолонов. Наименьшие уровни устойчивости отмечены к тиенаму, ванкомицину, уназину.
Профилактическое назначение антибиотиков при черепно-мозговой травме у детей, как правило, является эмпирическим. Оно определяется сложившейся структурой возбудителей внутригоспитальной инфекции с учетом резистентности микрофлоры к антибиотикам. Прямыми показаниями для профилактического назначения антибиотикотерапии у детей являются наличие ран мягких тканей, открытые проникающие и непроникающие повреждения, субарахноидальные кровоизлияния, тяжелая черепно-мозговая травма, сопровождающаяся длительным нарушением сознания и витальными нарушениями, а также сведения об отягощенном анамнезе в отношении воспалительных процессов со стороны внутренних органов. Обычно с профилактической целью применяют антибиотики широкого спектра действия: пенициллин G по 100 000 - 200 000 ЕД в сутки через 6-8 часов внутривенно, гентамицин по 2,5 мг/кг каждые 8-12 часов внутривенно и ванкомицин по 10 мг/кг каждые 6-12 часов внутривенно, ампициллин (росциллин) по 2,5 мг/кг каждые 4-6 часов внутривенно или внутримышечно (максимальная суточная доза 100 мг/кг), амписульциллин по 100-150 мг/кг в сутки за 3-4 приема внутримышечно или внутривенно, амоксиклав (амоксициллин) внутривенно до 3 месяцев по 0,03 г/кг через 12 часов, до 12 лет через 8 часов и старше по 1 г/кг через 8 часов. Хорошо себя зарекомендовали препараты цефалоспоринового ряда: цефазолин (рефрил) по 25-100 мг/кг в сутки за 3-4 введения внутримышечно или внутривенно, цефаклор (верцеф) по 20-40 мг/кг в день за 3 приема в суспензии, цефтибуден (цедекс) по 9 мг/кг в день в виде суспензии детям до 10 лет и по 400 мг в день детям старшего возраста, цефтриаксон (лонгацеф, офрамакс ) по 50-75 мг/кг 2 раза в сутки внутривенно или цефотаксим (клафоран) по 50 мг/кг 2-4 раза в сутки внутривенно, цефотазидим по 30-50 мг/кг каждые 8-12 часов внутривенно, цефамандол по 100-150 мг/кг внутривенно в сутки за 3-4 введения. Последним достижением в совершенствовании цефалоспоринов следует считать препарат этой группы IV поколения - цефепим (максипим) . Спектр его действия представляет собой совокупность спектров цефалоспоринов I и II поколений в отношении грамположительных бактерий и цефалоспоринов III поколения в отношении грамотрицательных бактерий. Особая эффективность цефепима отмечена при госпитальных инфекциях, тяжелом сепсисе, полиорганной недостаточности. При септических состояниях с превалированием грамотрицательной флоры рекомендуется сочетание цефепима с аминоглюкозидами (амикин, амикацин, нетилмицин). При смешанной инфекции и полиорганной недостаточности эффективно сочетание цефепима с циклофлоксацином и метранидозолом. Рекомендуемая доза цефипима детям до 2 месяцев составляет 50-100 мг/кг внутривенно или внутримышечно каждые 12 часов; в более старшем возрасте - по 1 г каждые 12 часов.
Заслуживает внимания также препараты группы фторхинолонов, которые во взрослой практике считаются почти идеальными для эмпирической терапии, а в детской практике используются только при отсутствии эффекта от применения цефалоспоринов и аминоглюкозидов (группа резерва). Из препаратов этой группы чаще используют ципрофлоксацин (цифран, ципробай, ципринол, ципролет) по 100-200 мг внутривенно 2 раза в день, офлоксацин (заноцин) по 200-300 мг внутривенно 2 раза в день. В неонатологической практике доза снижается до 20 мг/кг в сутки.
При анаэробной инфекции достаточно часто используется метронидазол (метраджил), хорошо проникающий через гематоэнцефалический барьер. Его дозировка составляет 15-35 мг/кг в сутки, вводимая внутривенно за 2-3 приема.
Первоначальная терапия гнойно-воспалительных осложнений принципиально не отличается от профилактической и назначение терапии является эмпирическим, так как не флора, не ее резистентность к этому моменту неизвестны, а промедление с началом лечения влечет за собой грозные последствия.
Эффективно применение при бактериальных менингитах, развивающихся после травмы, антибиотиков группы карбапенемов (имипенем, тиенам, меропен). В детской практике лучше себя зарекомендовал меронем. Доза для детей неонатального возраста составляет 15-20 мг/кг внутривенно в сутки за 3 введения, в более старшем возрасте по 20- 40 мг 3 раза. Реже используется антимикробный химиопрепарат, производное ди- b -оксихиноксалина, диоксидин , также хорошо проникающий через гематоэнцефалический барьер. Доза новорожденным составляет 10 мг/кг внутривенно капельно в два приема в комбинации с корректором цитогенетического эффекта - бемитилом до 20 мг/кг с сутки.
Выраженность воспалительного процесса и недостаточная эффективность парентерального введения препаратов обосновывают дополнение или переход на интратекальное введение препаратов (эндолюмбально, интравентрикулярно, интракраниально в дренажи). Анализ литературы и накопленный нами опыт позволяет рекомендовать следующие дозировки препаратов детям: гентамицин по 5-10 мг за введение, амикацин по 10-20 мг, хлоркальциевый комплекс стрептомицина по 0,01-0,05 г. Натриевая соль бензилпенициллина по 50 00 ЕД на 5 мл физиологического раствора, ванкомицин по 5-10 мг, канамицин по 50 мг, левомицетин гемисукцинат по 50100 мг, цефазолин по 50-100 мг, полимиксин В сульфат по 1-3 мг. Вводится также диоксидин 0,5% по 210 мг. Все эти препараты разводятся ликвором перед введением или физиологическим раствором.
Накопленный опыт про взаимоусиливающий эффект комбинации препаратов позволяет рекомендовать карбопинемы (парентерально) с аминоглюкозидами (интратекально), карбопинемы (парентерально) с диоксидином (интратекально), ванкомицин (парентерально и интратекально).
Целенаправленная антибиотикотерапия проводится с учетом определения тинкториальных и морфологических свойств флоры (грампозитивные, грамнегативные бактерии, кокки, палочки), учетом их атибиотикорезистентности.
Широкое использование антибиотиков, увеличение частоты инфекционно-воспалительных заболеваний, вызываемых грибками рода Candida , особенно у детей младшего возраста, обусловили увеличение частоты кандидозов в структуре воспалительных осложнений при черепно-мозговой травме у детей. Факторами риска развития кандидоза считаются: рождение от матерей страдающих кандидозом, ранний период жизни ребенка, критические ситуации (реанимация, травма и т.д.), интенсивная антибиотикотерапия и иммуносупрессия. Кроме традиционных антигрибковых препаратов (нистатин, микостатин, леворин) в последние годы широко используется препарат нового класса триазольных соединений - дифлюкан. Он применяется как внутрь в капсулах, так и внутривенно. Профилактическая доза составляет 2,5-5 мг/кг, лечебная 10-12 мг/кг в сутки.
Травматические субарахноидальные кровоизлияния у детей нередко являются единственным или составляющим моментом, определяющим тяжесть черепно-мозговой травмы. Субарахноидальные кровоизлияния практически всегда сочетаются с ушибами мозга, а в младшей возрастной группе и с переломами костей черепа. Выраженность клинических проявлений прямо пропорциональна возрасту ребенка - чем старше ребенок, тем выраженнее менингеальный синдром, вегето-сосудистые нарушения. Для остановки кровотечения используется стандартная гемостатическая терапия. Она включает: ингибиторы протеолиза (аминокапроновая кислота 5% раствор 50 - 100 мл внутривенно), препараты улучшающие функцию тромбоцитов (дицинон 12,5% раствор по 1-2 мл внутримышечно, викасол внутрь по 0,015 г 2-3 раза в день или внутримышечно по 1-2 мл, андроксон 0,025% раствор по 0,5-1 мл внутримышечно или подкожно 1-2 раза в сутки, глюконат кальция 10% раствор по 1-5 мл внутримышечно). Возможно применение свежезамороженной плазмы по 10-15 мл/кг. При незначительной степени геморрагии используются растительные препараты (настойка лагохилиса, экстракты крапивы, тысячелистника, водяного перца, калины, арники). C целью укрепления стенок сосудов применяют рутин по 0,05 - 0,1 г внутрь 2-3 раза в день, витамин Р по 0,05 - 0,1 г внутрь 2-3 раза в день.
В комплекс лечения ушибов мозга, сопровождающихся субарахноидальной геморрагией обычно входят дегидратационная терапия, противовоспалительная терапия, сосудистая терапия, ноотропы, симптоматическая терапия.
Для ускорения санации ликвора и предупреждения развития асептического менингита применяются разгрузочные люмбальные пункции. Извлечение 5 - 10 мл ликвора через 1-2 дня приводит к быстрой санации последнего. Связано это не только с выведением небольшой порции ликвора, стимулирующей его продукцию, но и с медленным пролонгированным поступлением ликвора в мягкие ткани через место прокола твердой мозговой оболочки. Прибегать к использованию длительного люмбального дренирования или промыванию его искусственными аналогами у детей, как правило, не приходится.
Сроки госпитализации детей с черепно-мозговой травмой средней степени тяжести обычно ограничены 14 - 21 днем, но преморбидный фон, особенно перинатальная патология, требуют более длительного стационарного лечения. Охранительный режим, освобождение от занятий в школе продлеваются еще на 20 - 30 дней. Все дети с травмой средней степени тяжести подлежат диспансерному контролю в течение не менее одного года.
Основные принципы и особенности консервативной терапии тяжелой черепно-мозговой травмы у детей
Консервативная терапия тяжелой черепно-мозговой травмы является прямым продолжением срочных и неотложных мероприятий по нормализации витальных функций организма, а также продолжением лечебных мероприятий после хирургического вмешательства. Схематически эта терапия направлена на купирование первичных повреждений и предупреждение и лечение вторичных церебральных и висцеральных нарушений. После первичного повреждения мозговой ткани или его компрессии возникает лавина нарушений, ведущих к выраженным метаболическим аномалиям. Однако даже в зонах первичного поражения имеются «зоны тени», в которых нейроны проявляют тенденцию к спонтанной деструкции как проявление естественного феномена апоптоза, тогда как вторичный каскад приводит к основным церебральным повреждениям. Поэтому именно основные лечебные мероприятия при тяжелой черепно-мозговой травме направлены на предотвращение и воздействие на причины вторичных повреждений экстра- и интракраниального происхождения. Весь комплекс этих мероприятий условно можно разделить на мероприятия по проведению интенсивной терапии и реабилитационные мероприятия, которые между собой тесно переплетаются и на разных этапах лечения имеют превалирующее значение.
Интенсивная терапия включает в себя, в первую очередь, действия по стабилизации витальных функций - дыхания и кровообращения, а также поддержание на необходимом уровне величин перфузионного давления, внутричерепного давления и мозгового метаболизма.
Нарушения адекватной вентиляции легких может быть связано как с нарушениями проходимости дыхательных путей, обусловленными наличием в дыхательных путях инородных тел, рвотных масс, крови, повреждением легких, пневмо- или гематораксе при кранио-торакальной травме, так и нарушениями функции дыхательного центра в результате черепно-мозговой травмы или ее осложнений. После санации верхних дыхательных путей у больных, находящихся в бессознательном состоянии, целесообразно использование временного воздуховода с оксигенацией вдыхаемой воздушной смеси (30% кислорода). Возможно подведение кислорода через назальный катетер или маску с поддержанием сатурации кислорода не ниже 90%, но у детей это сопряжено с возможными осложнениями (заглатывание воздуха и ограничение подвижности диафрагмы, сдавление нижней полой вены с затруднением венозного оттока и повышением внутричерепного давления, рвоты, аспирации, попадание воздуха в полость черепа при переломе основания), риск которых значительно увеличивается при использовании маски с мешком типа АМБУ.
Сохраняющаяся гиповентиляция, не говоря уже об апноэ, требует срочной интубаци, которая у детей требует предварительной седации и миорелаксации. Используется назо- или оротрахеальная интубация, каждая из которых имеет свои преимущества и недостатки. Назотрахеальное положение трубки более физиологично, оно обеспечивает лучшие условия для санации полости рта, позволяет глотать больному, сама трубка менее подвержена смещению. Вместе с тем, назотрахеальная интубация противопоказана при переломах основания черепа с ликвореей из-за высокого риска воспалительных осложнений, хуже условия для санации трахеи и самой трубки в связи с ее большей длиной и меньшим диаметром. Оротрахеальное положение трубки обеспечивает более адекватную санацию трахео-бронхиального дерева, позволяет проводить бронхоскопию, что крайне важно при явлениях аспирации и гнойно-воспалительных осложнениях. Отрицательными моментами оротрахеальной интубации являются легкая смещаемость трубки, затрудненная санация полости рта, необходимость перевода больного на зондовое кормление. Обычно у детей до 7 лет используются трубки без раздувной манжетки.
Недостаточная оксигенация после интубации, необходимость в гипервентиляции в связи с повышением внутричерепного давления, длительное коматозное состояние менее 8 баллов по шкале Глазго обосновывают перевод больного на ИВЛ. Дыхательный объем ориентировочно определяется из расчета 10 мл/кг, частоту дыхания устанавливают у младенцев 30-40 в минуту, у более старших детей - 15-20 в минуту при отсутствии положительного давления в конце выдоха. Их коррекция проводится с учетом показателей газового состава крови. От предлагаемой ранее пролонгированной и ранней гипервентиляции (РаСО2 25 мм Hg и менее) при тяжелой черепно-мозговой травме с целью снижения внутричерепного давления отказались из-за развития ишемических нарушений в результате уменьшения объемного мозгового кровотока и длительного расстройства ауторегуляции мозгового кровообращения. Только длительное, неподдающееся медикаментозной коррекции, повышение внутричерепного давления более 20-25 мм Hg может служить основанием для проведения умеренной гипервентиляции (Ра СО2 30-35 мм Hg ) и то не в первые сутки после травмы.
Невозможность проведения интубации или ее неэффективность требуют проведения экстренной трахеостомии . Она также показана при глубокой длительной коме с необходимостью интубации более 10-14 дней, при пролонгированной ИВЛ более 7-10 дней, при наличии гнойно-воспалительных осложнений со стороны легких у интубированных больных, при наличии стойких и выраженных бульбарных нарушениях.
Стабилизация показателей сердечно-сосудистой деятельности у пострадавших с ЧМТ является важнейшим условием улучшения церебральной перфузии и предупреждения вторичных повреждений мозга. Особенно существенен этот момент у детей, когда даже небольшая кровопотеря сопровождается значительным уменьшением ОЦК, а клинически проявляется только тахикардией. Срыв же компенсации происходит быстро и выражено. Поэтому детям с тяжелой ЧМТ следует сразу наладить внутривенное переливание кристаллоидов (0,9% раствор хлористого натрия, раствор Рингера, раствор Рингера лактата) по контролем АД. При устойчивой артериальной гипотензии применяют коллоидные растворы (полиглюкин , реополиглюкин, декстран, 5% раствор альбумина) из расчета 8-10 мл/кг. Достаточно редко приходится прибегать в педиатрической практике к использованию вазопрессоров (мезатон, метараминол ) и инотропных препаратов (адреналин, норадреналин, допамин, изпреналин ).
У взрослых и детей старшего возраста редко при изолированной ЧМТ развивается картина шока. В противоположность им у младенцев, в связи с малым ОЦК, возможно развитие шока при ранах мягких тканей, при массивных гематомах как экстракраниальных, так и интракраниальных. Наличие и степень шока у младенцев определяется на основании оценки цвета кожи, температуры конечностей, времени наполнения капилляров, частоте сердечных сокращений и величины артериального давления. Терапия принципиально традиционна - обезболивание, восполнение ОЦК путем трансфузии коллоидов, кристаллоидов, крови. Объем ОЦК восполняется 2-3 кратно от исходного. Из коллоидных растворов предпочтение отдается полиглюкину, реополиглюкину и только недостаточная эффективность этих мероприятий обосновывает применение инотропных препаратов (допамин по 3-8 мг/кг).
Важнейшими моментами лечебных мероприятий прим тяжелой ЧМТ является борьба с повышением внутричерепного давления и отеком мозга. Внутричерепное давление является производной величиной соотношения объемов мозга, крови и ликвора в закрытом внутричерепном пространстве. У детей младшего возраста в связи с неполным заращением костных швов и наличием родничков компенсаторные возможности стабилизации внутричерепного давления большие, но одновременно с этим у них выше гидрофильность мозговой ткани, что проявляется выраженным отеком мозга, именно для них характерна реакция гиперемии мозга (набухание), чаще возникают явления гипоксии, артериальной гипотензии, нарушения ауторегуляции мозгового кровообращения. В прямой зависимости с величинами внутричерепного давления находятся показатели церебрального перфузионного давления (разница между средним артериальным и внутричерепным давлением), которые во многом определяют исходы тяжелой ЧМТ. Признано, что снижение церебрального перфузионного давления ниже 60 мм Hg значительно увеличивает смертность и инвалидность.
Для снижения внутричерепного давления используются различные приемы, способы и методы. Наиболее простым и доступным способом является укладка больного с приподнятым головным концом кровати на 25-40 градусов, что улучшает венозный отток из полости черепа и достоверно снижает внутричерепное давление. На аналогичных принципах основано и применение седативных, релаксирующих, обезболивающих средств. Они предупреждают повышение внутрибрюшного и внутригрудного давления путем снятия психомоторного возбуждения, судорог, кашля.
Из медикаментозных средств мощного и быстрого действия, снижающих внутричерепное давление, в первую очередь, следует указать на осмотический диуретик - маннитол . Он вошел в международные стандарты и рекомендации по лечению внутричерепной гипертензии и отека мозга при ЧМТ. Доза препарата обычно составляет 0,25-0,5 г/кг и вводится внутривенно за 30 минут. Эффект применения маннитола проявляется через 5-10 минут и продолжается до 3-6 часов. При необходимости доза маннитола может быть увеличена до 1 г/кг. С целью профилактики почечной недостаточности целесообразно поддерживать осмолярность плазмы ниже 320 мОсм. Хорошо зарекомендовал себя и другой диуретик - маннит (20% раствор в дозе 1 г/кг), а также сочетание глицерина с маннитом (10-20% раствор маннита и 10-15% раствор глицерина из расчета по глицерину 0,7 г/кг), глицерина с 10% раствором альбумина. Среди других дегидратирующих препаратов, нашедших широкое применение в педиатрической практике, следует отметить ингибитор карбоангидразы - фуросемид (лазикс ). Он обладает меньшей активностью в отношении внутричерепного давления, но при гипернатриемии и гиперосмолярности плазмы является основным дегидратирующим средством. Доза препарата составляет
0, 25- 0,5 мг/кг, суточная доза 40-60 мг. Применяется также ацетазоламид (диакарб) по 80-100 мг/кг в сутки.
Среди других препаратов для лечения и профилактики отека мозга используются сорбилакт, реосорбилакт, свежезамороженная плазма по 5-10 мл/кг. Учитывая разный механизм действия различных препаратов, накоплен опыт их комбинированного применения. Так, в младшей возрастной группе эффективна комбинация: введение плазмы из расчета 5-10 мг/кг, затем 0,25 г/кг маннита в течение 10-20 минут и в конце лазикс 2-4 мг/кг. Эффект введения сохраняется в течение суток при отсутствии реакции «рикошета».
Широко используемые ранее глюкокортикоиды в терапии тяжелой ЧМТ, в частности для снижения внутричерепного давления, не нашли подтверждения эффективности в рондомизированных исследованиях. Однако, практически во всех клиниках в комплекс противоотечной терапии включают преднизалон по 5-10 мг/кг или дексазон по 0,5-1,5 мг/кг.
Отсутствие эффекта от проведенных мероприятий по снижению внутричерепного давления обосновывают применение вентрикулярного дренирования, так как выведение даже небольшого количества ликвора заметно снижает внутричерепное давление. Кроме того, наличие вентрикулярного катетера позволяет провести мониторирование внутричерепного давления и своевременную его коррекцию.
Широко применяемая многие годы в остром периоде тяжелой ЧМТ для снижения внутричерепного давления гипервентиляция оценивается в последнее время скорее негативно, чем позитивно. Связано это с высокой частотой ишемических повреждений мозга в результате гипервентиляции. Снижение внутричерепного давления при гипервентиляции связано с сужением сосудов мозга, что ведет к уменьшению мозгового кровотока, который в остром периоде ЧМТ и так снижен. Именно это является причиной увеличения частоты ишемических повреждений при использовании гипервентиляции, а снижение внутричерепного давления не компенсирует такие повреждения, что отражается на конечных результатах лечения. Применение гипервентиляции оправдано только на короткое время при ухудшении состояния, обусловленного повышением внутричерепного давления, которое не удается купировать другими методами и способами. При этом требуется мониторинг церебральной оксигенации, мозгового кровообращения, поддержание церебрального перфузионного давления не ниже 70 мм Hg и снижение РаСО2 менее 30 мм Hg .
Особую группу препаратов, применяемых для снижения внутричерепного давления, составляют барбитураты (тиопентал натрия, фенобарбитал, пентобарбитал) и другие гипнотики (оксибутират натрия, пропофол, этомидат). Являясь антигипоксантами, эти препараты уменьшают метаболизм кислорода в мозге, интенсивность перекисного окисления, снижают мозговой кровоток и внутричерепное давление. Введение больного в лечебный наркоз возможно только при стабильной гемодинамике и мониторировании ее показателей. Для введения в наркоз доза тиопентала натрия составляет 10-15 мг/кг, фенобарбитала и пентобарбитала - 10 мг/кг, оксибутирата натрия 100-150 мг/кг. Поддерживающая доза в течение первых часов уменьшается в два раза, а затем подбирается индивидуально под контролем глубины наркоза.
В комплекс лечебных мероприятий при тяжелой ЧМТ включены действия по предупреждению вторичных ишемических нарушений, гнойно-воспалительных осложнений, нормализации сосудистого тонуса и показателей свертывающей системы крови, уменьшению потребления кислорода, улучшению церебрального метаболизма, снятию болевого синдрома и гипертермии, предупреждению и купированию эпилептического синдрома, обеспечению метаболических потребностей организма. Они тесно переплетаются между собой, на различных этапах лечения являются ведущими или вспомогательными, но всегда остаются важными и существенными.
Для предупреждения вторичных ишемических нарушений используются ингибиторы протеолиза (контрикал по 10 -50 тыс. ЕД, гордокс по 100 тыс. ЕД, трасилол по 50 000 ЕД в сутки внутривенно капельно на физиологическом растворе), которые хорошо сочетаются с церебролизином по 10 - 30 мл внутривенно и сосудистыми препаратами: трентал 2% по 0,1 мл/кг, эуфиллин 2,4% по 0,1 мл/кг, курантил 0,5% раствор по 0,05-0,1 мл, ксантинол никотинат по 0,1 мл/кг. Использование таких сосудистых препаратов как сермион, кавинтон, цинаризин, теоникол целесообразно после купирования отека мозга и надежного гемостаза, обычно на 7-10 сутки после травмы.
Значительна роль в профилактике вторичных повреждений мозга препаратов, обладающих анигипоксическими и антиоксидантными воздействиями. К антигипоксантам относят: цитохром С (по 50 мг в сутки на 100-200 мл физиологического раствора внутривенно), рибоксин (по 200 мг в сутки на 100-150 мл физиологического раствора внутривенно), пирацитам (по 200 мг/кг внутримышечно или внутривенно), ГОМК (20% раствор по 0,4-0,5 мл/кг), кокарбоксилаза (8-10 мг/кг на 10% глюкозе), аскорбиновая кислота (5%раствор по 1-2 мл), рибофлавин мононуклеотид (0,05% раствор по 1-2 мг). Об антигипоксическом влиянии барбитуратов уже указано. Из препаратов антиоксидантного ряда следует указать на витамин Е (по 20 мг/кг), эмоксипин (1% раствор по 10-15 мг/кг внутривенно на 100-200 мл физиологического раствора), альфа-текоферол ацетат (по 15 мг/кг через 6 часов), унитиол (5% раствор по 0, 2 мл/кг), липоевая кислота (0,5% раствор по 0,1 мл/кг), пеницилламин (по 30 мг/кг внутривенно).
Отводится свое место в борьбе со вторичными ишемическими нарушениями и антиагрегантам. Улучшая микроциркуляцию и снижая возможности микротромбообразования препараты этой группы применяются на всех этапах лечения, но наиболее важны они в остром периоде тяжелой ЧМТ. Антиагрегантными качествами обладают: полиглюкин, реополиглюкин, реоглюман, нативная плазма.
Лечебные мероприятия по предупреждению и лечению гнойно-воспалительных осложнений при тяжелой ЧМТ незначительно отличаются от общепринятых стандартов для реанимационных больных. Они направлены, главным образом, на предупреждение, а при необходимости и на лечение, бронхопневмонии, пролежней, уросепсиса, сепсиса и менингоэнцефалита. Ведущее значение при этом имеют уход, санация, санитарно-гигиенический режим отделения, применение одноразовых стерильных медицинских изделий (шприцы, иглы, катетеры, зонды, трубки, системы и т.д.). С другой стороны, это средства и методы, направленные на повышение общей реактивности организма больного, его устойчивости к любым неблагоприятным воздействиям, увеличивающим восприимчивость организма к инфекции. Они включают нормализацию гомеостаза и обмена веществ, восполнение кровопотери, иммунокоррекцию, раннюю активизацию больного (пассивную и активную). Только на третьем месте в комплексе предупреждения гнойно-воспалительных осложнений стоят антимикробные препараты.
Наличие болевого синдрома негативно сказывается на многих показателях гомеостаза травмированного пациента, поэтому аналгезирующая терапия является обязательным компонентом лечения больных с тяжелой ЧМТ. Она включает ненаркотические аналгетики - аналгин 50% по 0,5-1 мл внутримышечно или в сочетании с димедролом, седуксеном, трамал по 0,1 мг/кг внутривенно. Из наркотических аналгетиков применяют фентанил по 1-2 мкг/кг, налоксон или налорфин 0,5% в 10 кратном разведении на физиологическом растворе по 0,2-0,5 мл, ардуан по 0,02-0,1 мг/кг, промедол 1% раствор по 0,1-1 мл. Редко приходится прибегать к нейролептаналгезии (25% раствор дроперидола по 0,3-0,5 мг/кг, 0,005% раствор фентанила по 0,0025 мг/кг, которые разводятся на 10 мл 510% глюкозе и вводятся внутримышечно).
Важным моментом лечения является поддержание нормальной температуры тела , так как повышение ее резко увеличивает энергозатраты, включая усиление мозгового кровотока. Экспериментально подтвержденная эффективность использования гипотермии для снижения потребления кислорода мозгом, в настоящее время не находит широкого применения в практике из- за большого числа осложнений. Из антипиретиков используются аспирин, реоперин, аналгин, парацетамол . Только недостаточная эффективность их применения обосновывает применение физических методов (влажное укутывание, обтирание уксусом, грелки со льдом на область бедренных артерий) и литических смесей, содержащих антигистаминные, нейроплегические и ганглиоблокирующие препараты. Введение литических смесей дополняется введением 1% раствора новокаина и 3-5% раствором соды.
Включение гемостатиков в комплекс лечения острого периода тяжелой ЧМТ обусловлено, с одной стороны, почти постоянным геморрагическим компонентом повреждения мозга, а с другой стороны, с целью профилактики вторичных геморрагических осложнений. Применяется аминокапроновая кислота 0,05 - 0, 1 г/кг 3-4 раза в день, дицинон 12,5% раствор по 1-2 мл, адраксон 0,025% раствор по 0,5 мл/кг, викасол 1% раствор по 0,2-1 мл., свежезамороженная плазма по 1015 мл/кг. Для укрепления стенок сосудов применяют рутин по 0,05 - 0,1 г внутрь 2-3 раза в день, витамин Р по 0,05 - 0,1 г внутрь 2-3 раза в день.
Для улучшения церебрального метаболизма и оптимизации «выхода» больных из тяжелого состояния применяются метаболиты, тонизирующие препараты, биостимуляторы. К ним относятся ноотропил (пирацетам) по 200-300 мг/кг перорально, пиридитол (энцефабол, пиритинол, пиритоксин) по 0,05 г 2-3 раза в день, глютаминовая кислота по 0,05-0,1 г 2-3 раза в день, когитум по 10 мл 2 раза в день, липоцеребрин по 0,125-0,25 г 2 раза в день, церебролизин по 0,5-5 мл внутримышечно или внутривенно, витамины В1, В6, В12 по 30-50 мкг. Используются также алоэ, стекловидное тело, ФиБС, апилак, семакс, жень-шень, лимонник.
Важнейшим моментом терапии больных с тяжелой ЧМТ является восполнение метаболических потребностей организма, осуществляемой путем энтерального и парентерального питания, которые возрастают в остром периоде травматического периода в 1,5- 3 раза. Согласно «Рекомендациям по лечению тяжелой ЧМТ» в течении первой недели необходимо замещение 140% калорической потребности больного с 15% содержанием белка по калоражу. У детей эта потребность еще более высокая. Парентеральное питание проводится с использованием жировых эмульсий (интралипид, липофундин ), белковых препаратов (плазма,альбумин, протеин ), аминокислот (левамин, аминостерил ), витаминов группы С и В. Энтеральное питание осуществляется через тонкие назо-гастральные зонды.
Страница 1 из 2
Практика врачевания ещё в далёком прошлом требовала определенной классификации черепно-мозговой травмы (ЧМТ) для тактических построений лечебного процесса. По-видимому, первое разделение ЧМТ было построено по принципу наличия или отсутствия повреждений костей черепа с выделением травмы закрытой и открытой, проникающей или непроникающей в полость черепа. Последующие тысячелетия характеризовались более углубленным изучением открытой ЧМТ (Гиппократ, А.Цельс, Гален, Ги де Шолиак, В. Карпи, А. Паре) с классификацией переломов костей черепа, повреждений твёрдой мозговой оболочки, вещества мозга. Впервые было обращено внимание на сотрясение головного мозга, его отёк, внутричерепные кровоизлияния. Лишь только в начале XVIII века Бовилем, а затем Ж. Пти было предложено разделение ЧМТ на три главные формы - « comotio , contusio , compresio cerebri ». Эта классификация выдержала трёхвековое испытание и лежит в основе всех современных классификаций ЧМТ. Только внедрение новых неинвазивных методов визуализации мозга (КТ, МРТ) уточнили ряд положений, выдвинув на первый план характер поражения мозговой ткани.
Рассматривая любую классификацию травмы организма, выделяют механизм травмы, вид, тип и характер повреждений, тяжесть и фазу травматической болезни, периоды и исходы. Учёт этих моментов особенно важен для ЧМТ, т.к. они нередко позволяют определить тактические построения и лечебные мероприятия.
По механизму травмирующего воздействия разделяют ЧМТ на ударно-противоударную, ускорения-замедления и смешанную. По особенностям внешнего воздействия выделяют группу действия предмета на ограниченный участок головы (камень, палка, топор, гвоздь и т.д.), сдавление головы (акушерские щипцы, обвалы и т.д.), удары головой о неподвижные предметы (падение с высоты, ДТП и т.д.). Особую группу составляют огнестрельные и взрывные повреждения черепа и головного мозга.
По типу травмирующего воздействия различают изолированную ЧМТ, сочетанную (повреждающее воздействие механической силы кроме головы на другие системы и органы человека) и комбинированную (воздействие механической и других видов энергии - термической, лучевой, химической и т.д.).
По характеру ЧМТ разделяют на закрытую и открытую. К закрытой ЧМТ относятся повреждения головного мозга без или с повреждениями кожных покровов головы, но без повреждения апоневроза с переломами или без переломов костей черепа, но с обязательным отсутствием сообщения внутричерепного пространства с внешней средой. К открытой ЧМТ относятся наблюдения, где имеются повреждения апоневроза или сообщение внешней среды с полостью черепа. В открытой ЧМТ выделяют непроникающую (без повреждения твёрдой мозговой оболочки) и проникающую (с её повреждением) травму.
По виду повреждений мозговой ткани различают диффузные (сотрясение мозга, диффузные аксональные повреждения), очаговые (ушибы, размозжение, кровоизлияние, сдавление) и сочетанные повреждения.
Клинические формы ЧМТ базируются на виде, тяжести и морфологическом субстрате поражения мозга. Выделяют следующие клинические формы ЧМТ: сотрясение мозга, ушибы мозга различной степени тяжести (легкие, средние, тяжелые), сдавление мозга (гематомы, вдавленные переломы, напряженная пневмоцефалия и т.д.), диффузные аксональные повреждения мозга и сдавление головы.
По тяжести ЧМТ условно делят на легкую (сотрясение мозга, ушибы мозга легкой степени), среднюю (ушибы мозга средней степени тяжести) и тяжелую (ушибы мозга тяжелой степени, острые сдавления мозга, диффузные аксональные повреждения и сдавление головы).
В течении ЧМТ выделяют три периода: острый (до двух недель), промежуточный (до 6 месяцев) и отдаленный (более поздние сроки).
По исходам ЧМТ следует различать: хорошее восстановление функций (выздоровление), умеренную инвалидизацию, грубую инвалидизацию, вегетативный статус и смерть. Исходы прямо связаны с тяжестью ЧМТ, её периодом и проводимыми мероприятиями на различных этапах лечения.
Все эти принципиальные положения классификации ЧМТ являются базисными и отражают современные взгляды на травматические повреждения головного мозга. Однако, возраст пострадавших, преморбидный фон и другие сочетания факторов позволяют пользоваться такой классификацией ЧМТ с некоторыми оговорками.
Клиническая классификация ЧМТ у детей
Анатомо-физиологические особенности и своеобразия реакций растущего организма ребенка на ЧМТ обосновывают некоторые изменения в традиционной классификации ЧМТ. Отличия имеются не только в сравнении со взрослыми, но и внутри детской возрастной группы они столь разительны, что нередко проводят сопоставления новорожденных и подростков, как юношей и долгожителей. Особенности клинических проявлений и течения ЧМТ у детей во многом обусловлены огромными компенсаторными возможностями формирующихся нервных структур, готовностью внутричерепного содержимого к резким колебаниям ликворного давления и, в то же время, повышенной ранимостью и гидрофильностью мозговой ткани ребенка.
Обобщая огромный материал по ЧМТ у детей, имеющийся в литературе, и опыт собственной работы мы предлагаем следующую клиническую классификацию ЧМТ у детей, сопоставляя её с тяжестью состояния пациентов:
I. Черепно-мозговая травма легкой степени тяжести:
1. Сотрясение головного мозга.
II. Черепно-мозговая травма средне степени тяжести:
1. Ушибы головного мозга легкой-средней степени тяжести, сочетающиеся с переломами костей черепа или без них.
III. Черепно-мозговая травма тяжелой степени тяжести:
1. Ушибы головного мозга тяжелой степени тяжести.
2. Сдавление головного мозга:
а) внутричерепные гематомы (поднадкостнично-эпидуральные, эпидуральные, субдуральные, внутримозговые, внутрижелудочковые, множественные);
б) вдавленные переломы костей черепа;
В) «растущие» переломы костей черепа;
Г) гидромы;
Д) «напряженная» пневмоцефалия.
3. Диффузные аксональные повреждения мозга.
4. Длительное сдавление головы.
Главным отличием предлагаемой классификации являются перенос ушибов легкой степени тяжести в группу ЧМТ средней степени тяжести и выделение в группе ЧМТ тяжелой степени тяжести таких форм как «поднадкостнично-эпидуральные гематомы» и «растущие» переломы костей черепа, которые встречаются только в детском возрасте.
Перенос ушибов легкой степени тяжести из группы легкой ЧМТ связано с тем, что в отличие от взрослых провести клиническую дифференциальную диагностику сотрясения мозга и ушиба легкой степени тяжести практически невозможно. Критерии длительности потери сознания и глубины нарушения сознания после травмы у детей, особенно младшего возраста, являются не адекватными, т.к. у них не только легкая ЧМТ, но и ЧМТ средней степени тяжести, а подчас и даже тяжелая ЧМТ может протекать без потери сознания или этот факт не удается зафиксировать. Нередко только обнаружение переломов костей черепа и данные КТ позволяют склониться к диагнозу ушиба мозга. Только выраженность изменений стволовых вызванных потенциалов позволяют нередко различить сотрясение мозга и ушиб мозга легкой степени тяжести. Возможно, это включение в легкую ЧМТ ушибов мозга легкой степени тяжести объясняет столь высокую частоту у детей отдаленных последствий ЧМТ легкой степени тяжести, составляющую 60-80% наблюдений. Практически эти же мотивы являются основанием для объединения ушибов легкой и средней степени тяжести в одну группу.
Только в детском возрасте встречаются поднадкостнично-эпидуральные гематомы, обусловленные миграцией отломков костей, повышением внутричерепного давления и пассажем крови в эпидуральное и поднадкостничное пространство. Только у детей обнаруживаются «растущие» переломы костей черепа, возникающие при переломах с разрывом твёрдой и паутинной мозговых оболочек, поступлением ликвора в поднадкостничное пространство, «раздвиганием» костей черепа с последующим формированием экстра-интракраниальных кист и даже мозговых грыж.
Существенным моментом в диагностике, определении очерёдности и тактики лечебных мероприятий при ЧМТ является оценка тяжести состояния пострадавшего. Она определяется, главным образом, тяжестью ЧМТ, но не всегда совпадает с ней, особенно у детей. Тяжесть состояния - понятие более динамичное и во многом коррелируется с исходами лечения пострадавших. Необходимость единого подхода к оценке результатов лечения в зависимости от тяжести травмы и тяжести состояния пострадавшего обусловила появление различных количественных и качественных оценок тяжести состояния.
Ребенок не сидит на месте. Он стремится везде успеть, все познать. Их чрезмерная двигательная активность и любознательность порой удивляет взрослого человека. Они могут бегать, прыгать, танцевать по несколько часов к ряду. Детям не всегда достает жизненного опыта, чтобы оценить опасность ситуации, и поэтому травмы у них не редкость. И одни из наиболее опасных – травмы головы и головного мозга. Признаки получения детьми такого рода травм не всегда становятся заметными сразу. Часто они скрывают от родителей ушиб или попросту не акцентируют на нем внимание. Зачастую травмы головы обходятся мелкими ссадинами, синяками и шишками, но иногда несут в себе серьезные последствия.
Для того чтобы понять степень тяжести травм головного мозга, которые могут возникнуть у детей, нужно более тщательно разобраться в их разновидностях, симптомах, способах лечения. Нередко родители принимают серьезный ушиб головы своего сына или дочери за легкий удар и не обращаются в больницу, тем самым подвергая опасности своих детей.
Закрытая черепно-мозговая травма у ребенка: основные признаки и последствия
Черепно-мозговая травма (ЧМТ) может быть вызвана у детей путем падения, удара и даже резкой остановки при беге или, наоборот, неожиданного ускорения хода. Это объясняется их любознательностью, неусидчивостью, высокой двигательной активностью, а также отсутствием чувства опасности и боязни высоты. Стоит иметь в виду, что вес головы малышей относительно большой, поэтому чаще всего они падают именно вниз, даже не успев подставить руки. Свыше 90% ЧМТ у младенцев, получаются по причине невнимательности родителей. Отвернувшись всего на одну секунду, взрослый может упустить тот момент, когда малыш перевернулся с пеленального стола, упал с кровати или перекатился с дивана. Когда чадо становиться на ноги, травмы головного мозга вызывают не только падения с высоты его роста, но и с лестниц, веток деревьев, детских горок, так далее. В такой возрастной период закрытая черепно мозговая травма, случившаяся у ребенка, может быть незаметной для родителей – они об этом часто даже не подозревают. Иногда более взрослые дети сами утаивают от родителей травму, а бывает, даже не понимают того, что на самом деле с ними происходит. У детей дошкольного возраста травма головы может возникнуть даже при чрезмерном укачивании в автомобильном или железнодорожном транспорте. Следуя из вышеперечисленного, родители должны быть крайне внимательными к происходящим процессам в жизнедеятельности ребенка, чтобы вовремя обнаружить у него основные симптомы черепно-мозговой травмы.
К счастью, 90% травм мозга являются сотрясениями, которые достаточно редко несут за собой осложнения. Не стоит забывать, что головной мозг у взрослых людей и маленьких детей имеет существенные различия. Если взрослый человек испытывает при такой травме головную боль, минутную потерю сознания и даже амнезию, то признаки черепно-мозговой травмы часто малосимптомны у младенцев и немного заметны у ребенка школьного возраста. У самых маленьких можно заметить бледность кожи, отсутствие аппетита, беспокойство во сне или его отсутствие, срыгивание при кормлении. Здесь родитель должен быть предельно внимателен ко всем изменениям, происходящим с его чадом. Последствиями черепно-мозговой травмы у школьника или у ребенка 3-6 лет могут стать появление рвоты, повышенной потливости, скачки артериального давления, головная боль. Очень редко может наблюдаться посттравматическая слепота, которая длится от нескольких минут до нескольких часов, но потом пропадает сама по себе. Ее не стоит бояться и следует просто подождать. Детский организм устроен таким образом, что симптоматика может нарастать только по истечению некоторого времени, но не сразу после удара. Любая выявленная черепно-мозговая травма немедленно нуждается в лечении у детей, поэтому родителям срочно нужно обратиться к врачу.
Как определить сотрясение головного мозга у ребенка: как проявляются первые признаки
Сотрясение – это наиболее легкая травма головного мозга. В результате падения или удара по голове в головном мозге происходит нарушение микроциркуляции на уровне мелких сосудов. Возникает отек, который сдавливает ткани мозга. Если ребенок после травмы потерял сознание на какое-то время, это может свидетельствовать о наличии сотрясения головного мозга. После того как ребенок придет в себя, у него появляются такие симптомы, как головная боль, головокружение, тошнота, бледность. Еще один важный симптом - кратковременная потеря памяти. Последствия травмы сохраняются примерно в течение недели.
Основными симптомами сотрясения головного мозга у младенца и ребенка школьного возраста выступают, в первую очередь, тошнота, а также резкая слабость. Затем пострадавший становится более раздражительным, у него проявляется повышенная сонливость и усталость. Довольно редко в таком случае может возникнуть рвота или появление головной боли. Если у ребенка проявляются данные признаки сотрясения мозга, родителям лучше обратиться к невропатологу, травматологу или нейрохирургу. Специалист проведет осмотр, внимательно изучив все жалобы. При необходимости для постановки диагноза сотрясения мозга могут быть назначены дополнительные методы диагностики у ребенка. Для маленьких детей чаще всего таким способом становится нейросонография или же рентгенография. После выявленного у ребенка сотрясения мозга ему назначается лечение.
Что делать при сотрясении головного мозга у ребенка и последствия травмы
 В домашних условиях самостоятельно можно обнаружить сотрясение мозга, исходя из вышеперечисленных симптомов у своего ребенка, но вот убедиться в отсутствии трещин черепа, смещений, кровоизлияний и назначить правильное лечение будет крайне сложно, а точнее, просто невозможно. Поэтому только врач подскажет, как определить сотрясение мозга и правильно диагностировать его у ребенка. Наверное, самым лучшим методом выявления травм черепа и повреждений мозга на сегодняшний день выступает компьютерная томография. Именно КТ более эффективна, а также распространена в медицинских учреждениях.
В домашних условиях самостоятельно можно обнаружить сотрясение мозга, исходя из вышеперечисленных симптомов у своего ребенка, но вот убедиться в отсутствии трещин черепа, смещений, кровоизлияний и назначить правильное лечение будет крайне сложно, а точнее, просто невозможно. Поэтому только врач подскажет, как определить сотрясение мозга и правильно диагностировать его у ребенка. Наверное, самым лучшим методом выявления травм черепа и повреждений мозга на сегодняшний день выступает компьютерная томография. Именно КТ более эффективна, а также распространена в медицинских учреждениях.
Как только у детей проявляются первые симптомы сотрясения головного мозга, родителям необходимо дать покой пострадавшему. При появлении кровотечения из раны, нужно срочным образом обработать ее и перебинтовать. Стоит помнить, что вылечить сотрясение мозга, возникшее у детей любого возраста можно только, начав с госпитализации. В условиях стационара могут быть предотвращены осложнения сотрясения мозга, последствиями которого у ребенка могут быть гематомы внутри черепа, отеки мозга. Такие осложнения проявляются крайне редко, также они являются признаками сотрясения головного мозга, которые можно обнаружить у своего ребенка. В больнице пострадавший имеет психоэмоциональный покой за счет отсутствия любого рода активности – ни социальной, ни двигательной. Срок пребывания в медицинском учреждении зачастую ограничивается 2-4 днями. После выписки на срок 1-2 недели ему запрещено заниматься спортом, вести активный образ жизни, а также проводить много времени за просмотром телевизора и за компьютером.
Основной принцип терапии – это покой и бдительный контроль специалистов, лечение медикаментами сотрясения головного мозга у детей также имеет место быть. Чтобы исключить образование отека, пациенту прописывают мочегонные средства в сочетании с калием. При наличии головных болей назначаются анальгетики, редко выписывают антигистаминные или успокаивающие препараты.
Если вовремя не обратиться к специалисту, то у ребенка могут быть достаточно серьезные последствия сотрясения головного мозга. К ним относятся частые головные боли, периодические позывы к рвоте, раздражительность от любимых игр, нарушения сна, заторможенная реакция при выполнении повседневных заданий, метеозависимость. Наиболее опасным последствием после этой травмы может быть возникновение посткоммоционного синдрома. Иногда он может проявиться лишь спустя несколько месяцев, а у кого-то даже через пару лет. Он выражается резкой головной болью, внезапным головокружением и ухудшением зрения. Лечение данного симптома не имеет смысла. Чаще всего дети со временем просто привыкают к этим изменениям.
Вышеописанные последствия после сотрясения мозга, которые проявляются у ребенка уже после наступления травмы, ошибочно родители принимают за первые признаки сотрясения мозга, произошедшего у ребенка, поэтому очень важно не путать их, чтобы не опоздать с постановкой диагноза. Взрослым необходимо быть внимательными к состоянию здоровья и общему самочувствию своего чада. Для этого важно знать, как именно проявляется сотрясение мозга и его первые симптомы у ребенка. Если родители задержались с обращением к врачу, то пострадавшему могут быть назначены ноотропные препараты или специальные витамины.
Подведя итог, важно отметить, что сотрясения головного мозга встречаются у детей довольно часто. В основном, они не представляют опасности для дальнейшего развития, но врачебная диагностика и правильное лечение здесь необходимы для исключения негативных последствий, особенно, если полученное сотрясение происходит не впервые. Если у родителей возникает паника – они не знают, что делать при выявлении сотрясения мозга у их ребенка. Нужно обеспечить покой пострадавшему, вызвать врача или же самим обратиться в ближайшую больницу. Далее за лечение детей принимаются врачи, а родным необходимо лишь обеспечить спокойный образ жизни пострадавшему в течении как минимум недели.
Ушиб головного мозга у ребенка: основные симптомы, лечение и последствия
 Ушиб головного мозга - более серьезная травма. Часто ушибом еще называют контузию. Главным симптомом данной черепно-мозговой травмы является потеря сознания. Бывает легкой, среднетяжелой и тяжелой степени. При легком ушибе симптомы повреждения головного мозга схожи с сотрясением, но возможны сопутствующие трещины и даже мелкие переломы костей черепа. При этой травме ребенок находится без сознания обычно более получаса. После восстановления сознания наблюдается затруднение в движениях конечностей. При среднетяжелом ушибе головного мозга ребенок без сознания может находиться до нескольких часов. Симптомы нарушения функции центральной нервной системы более тяжелые. Тяжелый ушиб характеризуется резко выраженными признаками неврологических нарушений. Ребенок может находиться без сознания до нескольких суток. Возможны переломы костей черепа, наиболее тяжелые из которых открытые. Ушиб головного мозга сопровождается кровоизлиянием в пространство под мозговыми оболочками. Большое значение для выявления степени тяжести
Ушиб головного мозга - более серьезная травма. Часто ушибом еще называют контузию. Главным симптомом данной черепно-мозговой травмы является потеря сознания. Бывает легкой, среднетяжелой и тяжелой степени. При легком ушибе симптомы повреждения головного мозга схожи с сотрясением, но возможны сопутствующие трещины и даже мелкие переломы костей черепа. При этой травме ребенок находится без сознания обычно более получаса. После восстановления сознания наблюдается затруднение в движениях конечностей. При среднетяжелом ушибе головного мозга ребенок без сознания может находиться до нескольких часов. Симптомы нарушения функции центральной нервной системы более тяжелые. Тяжелый ушиб характеризуется резко выраженными признаками неврологических нарушений. Ребенок может находиться без сознания до нескольких суток. Возможны переломы костей черепа, наиболее тяжелые из которых открытые. Ушиб головного мозга сопровождается кровоизлиянием в пространство под мозговыми оболочками. Большое значение для выявления степени тяжести
ушиба головного мозга у маленького ребенка имеет место удара – лоб, центральные извилины, виски, теменная область, затылок или же основание мозга. Именно от этого зависят и нижеперечисленные симптомы.
Родителям, в первую очередь, необходимо обработать рану, если она кровоточит или же приложить лед к месту гематомы. Но как быть, если на месте ушиба мозга повреждения у ребенка не обнаружены. В таком случае взрослым нужно проявить повышенную внимательность к поведению своего малыша. Исходя из симптомов, можно определить наличие ушиба и как можно быстрее вызвать скорую помощь.
При ударе лобной доли у ребенка основными симптомами ушиба мозга могут выступать тошнота, рвота, бледность кожи лица, расширение зрачков, заторможенность речи, тяжесть дыхания. Часто может наблюдаться посинение губ, резкое увеличение шишки в месте удара, выступание крови из носа или ушей. Даже один из вышеперечисленных признаков является доказательством наличия ушиба и стать причиной вызова неотложки.
Если же пострадавший ударился затылком, то к перечисленным симптомам могут добавиться нарушение памяти, двоение в глазах (зрительные галлюцинации) и онемение конечностей. При ударе области извилин у детей тревожными симптомами ушиба головного мозга являются утрата рефлексов и появление судороги. Когда областью поражения становятся виски, могут возникнуть слуховые галлюцинации и расстройства письма. Ушибы темечка очень тяжело определить, особенно это касается младенцев, так как они проявляются тактильными расстройствами и уменьшением чувствительности. Ушибы основания мозга зачастую сопровождаются переломами костей черепа.
Сотрясение или ушиб в первое время очень сложно диагностировать, а потому обязательной является консультация со специалистом. Метод лечения ушиба существенно отличается от лечения сотрясения. Пострадавшему необходима экстренная медицинская помощь. В любом случае следует вызвать врача либо доставить ребенка в травмпункт. При переломах костей черепа или повреждениях мягких тканей надо наложить на голову стерильную бинтовую повязку, приложить пузырь со льдом к голове. Давать ребенку какие-либо лекарственные препараты не рекомендуется. Оценив степень тяжести травмы, врач решает вопрос о возможной немедленной госпитализации в отделение реанимации. При легких травмах головного мозга предписывают покой и постельный режим, а также наблюдение участкового врача. Назначают обезболивающие, успокаивающие средства, а также противорвотные. В тяжелых случаях показана срочная госпитализация со всем комплексом мер по реанимации пострадавшего ребенка. В дальнейшем врач назначает восстановительное лечение в зависимости от прогноза.
 Чтобы определить степень повреждения у ребенка и назначить должное лечение ушиба мозга, нужно оценить состояние его дыхательной и сердечнососудистой системы и произвести неврологическое обследование. Наиболее распространенными способами для постановки диагноза являются компьютерная томография, а также магнитно-резонансное обследование. Далее, в зависимости от степени тяжести ушиба, лечение может происходить двумя способами – хирургическим и терапевтическим. Первый применяется при необходимости удалить физический фактор сдавливания мозговой ткани (гематомы, костные отломки, кровоизлияния), который выполняется путем костно-пластической трепанации. Терапевтический метод – это медикаментозное лечение для устранения повышенной внутричерепной гипертензии. Нельзя забывать о профилактике, чтобы не дать возможности образоваться отеку головного мозга. Если же отек все же случился, врачи вводят гипертонические растворы в кровь или же для более длительного эффекта применяют диуретические средства. Сроки лечения колеблются от 1 до 12 месяцев, это зависит от тяжести ушиба. В таком случае рекомендовано минимум три недели соблюдение постельного режима.
Чтобы определить степень повреждения у ребенка и назначить должное лечение ушиба мозга, нужно оценить состояние его дыхательной и сердечнососудистой системы и произвести неврологическое обследование. Наиболее распространенными способами для постановки диагноза являются компьютерная томография, а также магнитно-резонансное обследование. Далее, в зависимости от степени тяжести ушиба, лечение может происходить двумя способами – хирургическим и терапевтическим. Первый применяется при необходимости удалить физический фактор сдавливания мозговой ткани (гематомы, костные отломки, кровоизлияния), который выполняется путем костно-пластической трепанации. Терапевтический метод – это медикаментозное лечение для устранения повышенной внутричерепной гипертензии. Нельзя забывать о профилактике, чтобы не дать возможности образоваться отеку головного мозга. Если же отек все же случился, врачи вводят гипертонические растворы в кровь или же для более длительного эффекта применяют диуретические средства. Сроки лечения колеблются от 1 до 12 месяцев, это зависит от тяжести ушиба. В таком случае рекомендовано минимум три недели соблюдение постельного режима.
Последствия ушиба головного мозга могут длиться у детей при хорошем исходе от 15 до 20 дней. Часто они подразделяются на внутричерепные и внечерепные. Самыми опасными являются внутричерепные – менингиты, абсцесс и энцефалиты, проявляющиеся даже по истечению трех месяцев после произошедшей травмы. Внечерепные последствия у ребенка при ушибе головного мозга – это астенический синдром (повышенная усталость, раздражительность, замкнутость), резкое повышение или понижение артериального давления, нарушение работы печени и почек, а также пневмония. Очень редко случается возникновение эпилепсии у пострадавших, такое бывает у 10-20% детей и может проявиться лишь спустя 1,5 года. К счастью, детские физиологические особенности не дают развиваться последствиям высокой степени тяжести при ушибах мозга, но это вовсе не значит, что лечением можно пренебречь. Любой удар головы требует внимательного отношения взрослых к пострадавшему, его госпитализации и безукоризненного выполнения указаний врача.
Нужно помнить, что полученная травма головы, особенно если речь идет о младенце, является необходимостью обращения к врачу. Самостоятельно вылечить ушиб дома невозможно, так как такая травма головы чревата тяжелыми последствиями.
Статья прочитана 8 263 раз(a).
Любое повреждение – это испытание для организма. Она не проходит бесследно, и не может не сопровождаться неприятными ощущениями. Особенно тяжело травмы переносят малыши, ведь их организм очень уязвим, а некоторые части тела ввиду анатомических особенностей наиболее чувствительны к повреждениям. Повреждения головы называют черепно-мозговыми травмами, сокращенно ЧМТ.
Это самая частая причина детского травматизма, она составляет около 30-40% от всех видов травм. Чаще всего ЧМТ подвержены мальчики от 3 до 7 лет. Основные причины черепно-мозговых травм у ребенка сводятся к падениям, бытовым или спортивным травмам, дорожно-транспортным происшествиям. Голова грудных малышей имеет неокрепший каркас, кости их черепа не до конца сращены. И соединяются посредством особых швов и родничков – прослоек хрящевой ткани.
Благодаря этим особенностям малышу легче было появиться на свет. Такое строение обеспечивает податливость головы при прохождении по родовым путям. Но вступая в новый мир, швы и роднички не могут быстро окостенеть до состояния взрослых. Поэтому первые года жизни ребенка наиболее опасны и уязвимы для его неокрепшей головки. Даже банальный ушиб головы может сыграть негативную роль в развитии ребенка.
Ведь по своей сути, ушиб – это дефект тканей головы, а ввиду компактного размещения мозга в черепной коробке, это поражение может затронуть и головной мозг, вызывая, в лучшем случае, его сотрясение. А в худшем, внешний ушиб может привести к противоудару, то есть внутреннему удару мозга о черепную коробку на другой стороне от приложенной силы, из-за незрелости неокрепших мозговых оболочек. Так возникают закрытые черепно-мозговые травмы. В зависимости от характера повреждения и тяжести ЧМТ выделяют следующие формы травм головного мозга:
- Сотрясение;
- Ушиб разных степеней тяжести – легкой, средней и тяжелой;
- Гематома, которая может располагаться между черепом и наружной мозговой оболочкой – эпидуральная, между внешней твердой оболочкой мозга и паутинной средней – субдуральная, и между паутинной и внутренней мягкой – субарахноидальная;
- Диффузное аксональное нарушение;
- Перелом костей свода черепа с вдавлением в мозг;
- Размозжение вещества мозга.
Травмы мозга могут привести к сдавлению его тканей, натяжению и смещению его вещества, повышению внутричерепного давления. Смещение мозговых структур приводит к разрывам ткани мозга и его сосудов, ущемлению образований мозга. Это нарушает питание головного мозга и его функцию. А повышение давления внутри черепа способствует отеку мозга и его набуханию – чрезвычайно опасному осложнению.
Именно ввиду этих анатомический особенностей, а также беззащитности младенцев, неспособности позаботиться о себе, родители должны чрезвычайно внимательно соблюдать профилактические мероприятия во избежание детских травм головы. Так, родителями положено следить за передвижением своего чада. Стремление познать окружающий мир и отсутствие понятий о том, что опасно, а что нет, играют детям не на пользу.
Стоит родителю отвести взгляд на секунду, как диван превращается в трамплин, а стол в кирпичную стену. Помимо внимательного наблюдения за ребенком, следует также аккуратно ухаживать за ним, ведь даже особенно интенсивное укачивание или активное встряхивание ребенка, может нанести вред его головке.
Симптоматическая картина ушиба головного мозга малышей
Так как мозг малыша способен быстро адаптироваться к окружающим изменениям, то есть его компенсаторные возможности значительны, симптоматическая картина ушиба может не сразу дать о себе знать. Это существенно затрудняет диагностические мероприятия и лечение. Ведь самым полезным лечебным воздействием будет скорая помощь, оказанная сразу после получения травмы, без развивающихся осложнений в виде гематом и кровоизлияний, отека мозга или инсульта.
Симптомы травмы будут мало чем отличаться от таковых у взрослых, за исключением лишь того, что ребенок не в состоянии пожаловаться вслух об этом и объяснить где у него болит. В зависимости от силы, нанесенного повреждения, внешне место удара будет разниться. Степень тяжести ушиба определяет его клинические проявления. Так, ушиб головного мозга легкой степени, который также называют контузия, может иметь следующие признаки:
- Сильная головная боль, малыш будет показывать это болезненным плачем;
- Головокружение, при этом ребенок будет плохо ориентироваться в пространстве, его движения будут нетвердыми, а взгляд не сфокусированным;
- Тошнота и рвота, не связанные с приемом пищи;
- Снижение частоты сердцебиения или наоборот, увеличение;
- Повышение артериального давления;
- Несущественный нистагм, то есть колебательное подергивание глаз.

Ушиб легкой степени имеет благоприятный исход, и обычно уже через несколько дней происходит полное восстановление сознания малыша, он снова ориентируется в пространстве. При ушибе мозга средней степени тяжести наблюдаются следующая симптоматическая картина:
- Потеря сознания на несколько минут;
- Оглушение и заторможенность ребенка;
- Речевые нарушения;
- Повышенная слабость и утомляемость;
- Сонливость;
- Сильная головная боль;
- Головокружение с дезориентацией в пространстве и времени;
- Потеря памяти о случившейся травме – ретроградная амнезия;
- Тошнота и многократная рвота;
- Нарушения в работе мимической мускулатуры;
- Нистагм и пониженная реакция зрачков на свет.
При благоприятном стечении обстоятельств и своевременно оказанной помощи, последствия ушиба пропадают через 15-20 дней. Ушиб головного мозга тяжелой степени протекает в более яркой негативной окраске. Могут наблюдаются следующие симптомы:
- Потеря сознания на пару часов;
- Нарушение сердечно-сосудистой деятельности в виде чрезмерного повышения артериального давления, увеличения или уменьшения частоты сердечных сокращений;
- Расстройства дыхательной функции;
- Гипертермия;
- Нарушение глазных функций в виде парезавзора;
- Парезы или параличи конечностей;
- Расстройства акта глотания;
- Нистагм, как одного, так и обоих глаз;
- Чрезмерное расширение или сужение зрачка;
- Судорожные припадки разной степени тяжести;
- Нарушения речи;
- Расстройства психики.
Диагностика травм головы у ребенка и их осложнения
При подозрении на ушиб головного мозга у своих детей, родителям необходимо вызывать врача. Ввиду анатомической уязвимости и склонности к осложнениям, промедление просто недопустимо. Любые ЧМТ у детей – это показание к госпитализации для достоверного анализа клинических симптомов и проведения инструментальных методов диагностики. Помимо инструментального исследования, проводят неврологический осмотр, для выявления нарушений нервной системы.
Такой осмотр включает в себя проверку чувствительности маленького пациента – болевой, тактильной, температурной. Оценивают реакцию его зрачков на свет, их размер и симметричность. Анализируют болезненность глаз малыша, определяют напряжение его затылочных мышц. Проверяют симметричность лица, анализируют наличие головной боли, головокружения, силы и тонуса конечностей.

Инструментальная диагностика включает:
- Компьютерную томографию (КТ) или магнитно-резонансную томографию (МРТ) головы – это позволяет определить мельчайшие очаги повреждений, рассмотреть мозг слой за слоем, найти гематомы или участки кровоизлияний, где бы они не прятались. Однако МРТ грудным деткам практически не проводят ввиду потребности в наркозе для обеспечения полной неподвижности ребенка;
- Рентген относится к разряду самых распространенных методов диагностики травм. Хотя рентген хорош для определения состояния костной системы, о состоянии мозга он не скажет ничего, так как он слабо визуализирует мягкие ткани;
- Эхо-энцефалоскопию, которая позволяет выявить возможное смещение мозга по отношению к костям черепа, вызванную кровоизлиянием и повышением давления внутри черепа;
- Люмбальную пункцию, направленную на поиск в ликворе следов крови, свидетельствующей о травме;
- Электроэнцефалографию (ЭЭГ) с записью биоэлектрического потенциала мозга с целью выявления нарушений проводимости;
- Офтальмоскопию, которая способна показать кровоизлияние в сетчатку глаза, являющуюся одним из осложнений ЧМТ;
- Ангиографию, направленную на выявление бессосудистой зоны, лишенной кровоснабжения из-за ЧМТ;
- Краниографию – особый вид рентгенографии черепа, применяемой при черепно-мозговых травмах;
- Нейросонографию – вид УЗИ, проводимый для самых маленьких. Это довольно простой и безболезненный метод исследования, который позволяет выявить патологические изменения в мозге детей до 2 лет. Такое возрастное ограничение связано с анатомическими особенностями детской головки. До 2 лет кости черепа не плотные и изображение при исследовании четкое, но окостенение с возрастом делает картинку размытой. Для ультразвукового метода отсутствуют противопоказания, его можно выполнить то час, и практически каждая детская больница оснащена таким прибором.
Последствия после ЧМТ можно разделить на две большие группы - внутричерепные и внечерепные. К наиболее опасным внутричерепным осложнениям относят менингиты, энцефалиты и абсцесс мозга, который может быть, как ранним и развиваться около 3 месяцев после травмы, так и поздним, отсроченным, появляющимся спустя 3 месяца после ЧМТ. Чаще всего абсцесс формируется как исход энцефалита, поэтому в своем образовании он проходит гнойно-некротическую стадию энцефалита, стадию капсулы с гноем – пиогенной и терминальную с организацией этой капсулы.

Список внечерепных осложнений представлен пневмонией, острой сердечной недостаточностью, нарушением функций печени и почек, астеническим синдромом. Этот синдром представляет собой самое частое последствие ЧМТ любых возрастов и включает в себя повышенную утомляемость, раздражительность, замкнутость.
На фоне ЧМТ может развиться и вегетодистония, которая характеризуется изменениями артериального давления как в сторону снижения, так и увеличения, а также сбоями в системе терморегуляции. Тяжелые последствия после ЧМТ возглавляет эпилепсия, которая возникает у 10-20% детей. Чаще всего она образуется в первые 18 месяцев после травмы головы. Часто у ребенка степень тяжести ЧМТ не соответствует развивающимся последствиям ввиду детских анатомо-физиологических особенностей.
Лечение ушибов головного мозга
Травмы головы требуют обязательного вызова скорой медицинской помощи. Однако, чтобы облегчить состояние ребенка, можно самостоятельно оказать ему первую помощь. При отсутствии явных повреждений покровов головы, следует приложить к месту ушиба холодный компресс. Это уменьшает болевые ощущения, снимает отечность тканей мозга и способно приостановить кровотечение за счет рефлекторного спазма сосудов, как реакция на холод.
Также кровотечение останавливают методом тампонирования. Прикладывают к месту раны сухую чистую материю, если она пропитывается кровью, накладывают новую, если по прошествии 15 минут кровотечение не уменьшилось, необходимо срочно вызывать врача, так как ребенок уже потерял много крови и продолжает терять. Соотношение потерь крови малыша и взрослого разнятся. Грудничку достаточно потерять 150-200 мл и это будет ударом для его несформированного организма.
Любая ЧМТ головы требует покоя, однако, по возможности, не следует давать ребенку уснуть следующий час после ушиба. Иначе станет невозможно определить тяжесть его состояния. Следует даже разбудить малыша среди ночи, задать ему простые вопросы или оценить его координацию. Следует обратить внимание на зрачки ребенка, если они неодинаковы по размеру, то это показатель тяжелого состояния мозга. Повторные эпизоды рвоты, также тревожный звонок для родителя. Нужно немедленно вызывать врача.

При потере сознания, следует уложить головку ребенка набок, чтобы при рвоте массы не попали ему в дыхательные пути. А при подозрении на травму позвоночника, сопряженную с ушибом головы, следует очень бережно переворачивать туловище ребенка. По возможности лучше не делать этого вовсе.
В больнице для лечения ушибов головного мозга используют как терапевтические, так и хирургические методы. В зависимости от тяжести ушиба. Терапевтическая помощь сводится к медикаментозному устранению повышенного внутричерепного давления, снятию боли и предупреждению развития отека мозга. Осложнения, возникшие при травме, такие как сдавление вещества мозга, кровоизлияния, вдавление в мозг костных отломков черепа, требуют неотложной нейрохирургической помощи.
Специфической профилактики для предотвращения травм головы у детей не существует. Нет вакцины, которая убережет малыша от ушиба, нет таблетки, которая защитит его от ЧМТ и других травм. Профилактика полностью ложится на плечи родителей и воспитателей, она складывается из контроля за своими детьми. А также за обучением их осторожности.
Ввиду особенностей анатомического строение детской головки не стоит отклонять предложение врача скорой помощи в госпитализации ребенка. Даже если его состояние кажется нормальным. Отдаленные последствия травмы головы так характерны для деток. А госпитализация в больницу позволит понаблюдать за состоянием ребенка. Внимательное оберегание здоровья своего ребенка – ключ к качественной и счастливой семейной жизни.
Видео